PHARMA JONPI .
PHARMAMAR . EL FONDO CORTO SHAW. D.E. & Co COMUNICA A LA CNMV QUE VUELVE A AMPLIAR SU APUESTA BAJISTA HASTA LOS 8,5 MILLONES DE €UROS . YA TIENE UNA POSICIÓN DEL 0,6% CON 108.000 ACCIONES DE LA COMPAÑÍA . LOS FONDOS CORTOS ENTRAN EN UN VALOR ... VENDIENDO SIEMPRE AL ALZA LAS ACCIONES QUE ALGUIEN LE PRESTA ...
26 enero 2026
IMFORTE EN LA REUNIÓN DE LA EMA HOY : NO LO TIENE NADA CLARO AÚN PARA PODER EMITIR UNA OPINIÓN ... NI POSITIVA NI NEGATIVA ... LAS DUDAS PODRÍAN SER VARIAS : NO VER CLARA LA EVIDENCIA CLÍNICA ... O EL BENEFICIO CLÍNICO REAL ... O EL DISEÑO DEL ESTUDIO , SUBGRUPOS , TOXICIDAD , COMPARADOR , ETC ... TOCA ESPERAR A LA REUNIÓN DE MARZO 2026 PARA QUE LA EMA DÉ SU OPINIÓN ... POSITIVA O NEGATIVA SOBRE IMFORTE ... VEREMOS .
IAG . QUEDAN 24 JORNADAS DE BOLSA PARA QUE COMUNIQUE LOS RESULTADOS DEL 2025 CON UN MÁS QUE POSIBLE INCREMENTO EN INGRESOS Y BENEFICIOS SUPERIORES AL 2024 /// POSIBLE INCREMENTO DEL DIVIDENDO PARA 2026 /// POSIBLE INCREMENTO DE LAS RECOMPRAS ( ENTRE 1500 Y 2000 MILL€ ) ... ¿ LA ACTUAL BAJADA EN BOLSA PODRÍA SER MUY BIEN APROVECHADA PARA POSICIONARSE DE CARA A ESTAS POSIBLES ESPECTATIVAS ... ? .
¿ TARLATAMAB / ATEZOLIZUMAB COMO POSIBLE NUEVO TRATAMIENTO DE PRIMERA LINEA DE MANTENIMIENTO SMALL CELL LUNG CANCER ? . MÁS DE 25 MESES DE OVERALL SURVIVAL ES LO QUE APORTA TARLATAMAB COMBINADO CON ATEZOLIZUMAB ... DADO QUE TARLATAMAB Y ATEZOLIZUMAB YA ESTAN APROBADOS PARA SMALL CELL LUNG CANCER ... POR EL BIEN DE L@S PACIENTES ¿ PODRIA LA USFDA EVALUAR UNA POSIBLE APROBACIÓN ACELERADA ANTE ESTOS RESULTADOS QUE SON PRÁCTICAMENTE UN 100% SUPERIORES A LOS QUE APORTA IMFORTE ( ATEZOLIZUMAB / LURBINECTEDIN ?.
LO ACABA DE PUBLICAR LA AMERICAN CANCER SOCIETY JOURNAL ... Y LO PODRÁ DECIR MÁS ALTO ... PERO NO MAS CLARO .
CON UNOS DATOS TAN CONTUNDENTES NO SERÍA DE EXTRAÑAR QUE TANTO ROCHE COMO AMGEN Y LA PROPIA USFDA ... MOVIERAN FICHA ANTES DE LO PREVISTO ... VEREMOS .
CONTUNDENTE EL POST BY AMERICAN CANCER SOCIETY DEL 3 JANUARY 2026 ... LO PUEDE DECIR MÁS ALTO ... PERO NO MÁS CLARO .
SE PUEDE YA AFIRMAR QUE TARLATAMAB SUPERA AL LURBINECTEDIN TANTO EN PRIMERA LÍNEA DE MANTENIMIENTO ... COMO EN SEGUNDA LINEA PARA EL TRATAMIENTO ESTÁNDAR DE SMALL CELL LUNG CANCER EXTENSIVE-STAGE .
23 enero 2026
IMFORTE ( ATEZOLIZUMAB / LURBINECTEDIN ) COMO TERAPIA DE MANTENIMIENTO TRAS EL TRATAMIENTO DE PRIMERA LÍNEA ( INDUCCIÓN CIN ATEZOLIZUMAB ) //...// CALENDARIO EMA PREVISTO SEGÚN LA PROPIA PHARMAMAR ... PUBLICADO EN LA PRESENTACIÓN CORPORATIVA DE ESTE MES DE ENERO 2026 ... :
El VEREDICTO DE LA AGENCIA EUROPEA DEL MEDICAMENTO ( EMA ) ESTÁ PREVISTO DURANTE EL PRIMER SEMESTRE 2026 ( POR NO DECIR SEGUNDO TRIMESTRE 2026 ) ... SEGÚN LA PRESENTACIÓN CORPORATIVA DE PHARMAMAR Del PRESENTE MES ...
Y EL ACCESO AL MERCADO LO SITÚAN YA PARA 2027 ... SIEMPRE Y CUANDO CLARO ESTÁ QUE LA EMA LO APRUEBE .
A DIFERENCIA DE LA USFDA QUE APROBÓ INFORTE CON VARIAS LIMITACIONES CLAVES ...
LA EMA EN REALIDAD LO TIENE MUY MUY MUY FACIL TANTO PARA DAR UN SI ... COMO PARA DAR UN NO ...
RAZONES , RESULTADOS , EXPECTATIVAS Y EXPLICACIÓNES ... ENCIMA DE LA MESA EN AMBOS CASOS ... CLARAS , DEMOSTRABLES , CONVINCENTES Y CONTUNDENTES PARA PODER CONCEDER TANTO UNA APROBACIÓN ... COMO UNA DENEGACIÓN ...
¿ PORQUÉ VEREDICTO SE DECANTARÁ LA AGENCIA EUROPEA DEL MEDICAMENTO ( EMA ) ... ? .
OPDIVO ( NIVOLUMAB DE BRISTOL MYERS ) TIENE AÚN LA PATENTE ACTIVA ... SIN EMBARGO ZYDUS RELIANCE HA CONSEGUIDO QUE UNA VERSIÓN BÍOSIMILAR DEL FÁRMACO ( TISHTHA ) LLEGUE AL MERCADO DE LA INDIA A UN CUARTO DEL PRECIO ACTUAL .
GENERICOS VERSUS BIOSIMILARES .
OPDIVO ( NIVOLUMAB / BRISTOL MYERS ), está Indicado Para el Tratamiento de Múltiples Cánceres, Como el Melanoma, el Cáncer de pulmón Microcítico ( SCLC ) , NSCLC Y Varios Otros .
A Medida Que un Medicamento se Acerca a su Fecha Límite de LOE, Varios Fabricantes de Medicamentos Como AMGEN y SANDOZ se están Preparando Para Unirse al Mercado con Alternativas Biosimilares Más Baratas ...
22 enero 2026
GRIFOLS CNMV . KINTBURY CAPITAL LLP AUMENTA SU POSICIÓN CORTO / BAJISTA EN EL VALOR HASTA EL 1% .
TEVIMBRA ( TISLELIZUMAB, BeOne ) ... ES LA NUEVA APUESTA EN EUROPA Y ESPAÑA COMO TRATAMIENTO DE PRIMERA LÍNEA SMALL CELL LUNG CANCER EXTENSIVE-STAGE ... POR LO QUE EUROPA NADA TIENE QUE VER CON EEUU ... TISLELIZUMAB SUPERAN AMPLIAMENTE TANTO AL ATEZOLIZUMAB COMO AL DURVALUMAB ....
THE MEDIAN OVERALL SURVIVAL ( OS ) WAS 15.5 MONTHS FOR TEVIMBRA ( TISLELIZUMAB ) WITH CHEMOTHERAPY VERSUS 13.5 MONTHS FOR PLACEBO PLUS CHEMOTHERAPY, RESULTING IN A 25% REDUCTION IN THE RISK OF DEATH .
Links :
https://elglobalfarma.com/politica/aemps-publicacion-ipt-baja-septiembre/
https://elglobalfarma.com/politica/medicamento-oncologico-ipt-2025/
IMForte Trial Showed The Efficacy Of Combining Immune Checkpoint Blockade With LURBINECTEDIN In SMALL CELL LUNG CANCER EXTENSIVE-STAGE ( ES-SCLC ) . However, There Is No Insight Into The Effect Of LURBINECTEDIN On The Immune Microenvironment In SMALL CELL LUNG CANCER ( SCLC ) .
JOURNAL THORACIC ONCOLOGY . JANUARY 2026 .
La Prestigiosa Revista ONCOLOGICA se Hace Eco de Estos Resultados Alcanzados Por los Científicos del Department of Oncological Sciences, Tisch Cancer Institute at Mount Sinai, Icahn School of Medicine at Mount Sinai, New York, NY :
El Ensayo IMForte Demostró la Eficacia de Combinar el Bloqueo de Puntos de Control Inmunitario con LURBINECTEDIN en el CÁNCER DE PULMÓN DE CÉLULAS PEQUEÑAS ... Sin Embargo, se Desconoce el Efecto de LURBINECTEDIN en el Microambiente Inmunitario del SCLC ...
*.- No Se Sabe Aún Con Precisión Cómo Afecta LURBINECTEDIN a las Células del Sistema Inmunitario Que Rodean al Tumor, Como Linfocitos, Macrófagos, Citoquinas ...
**.- Por lo Qué No se Sabe Si LURBINECTEDIN Ayuda, Perjudica o es Neutro Para la Respuesta Inmune ...
*.- LA INVESTIGACIÓN NO ESTÁ NI CONCLUIDA NI CERRADA ...
*.- ESTÁ PREVISTO IR OBTENIDO RESULTADOS DE LARGO PLAZO CONTINUAMENTE CON IMFORTE ...
*.- DE HECHO Y SEGÚN EL CLINICAL TRIALS ESTÁ PREVISTO QUÉ IMFORTE APORTE DATOS EN AGOSTO 2026 .
¿ QUÉ HACE LA FDA EN PARALELO ? :
LA APROBACIÓN NO CIERRA LA INVESTIGACIÓN, AL CONTRARIO :
LA USFDA EXIGE O RECOMIENDA :
Estudios post-aprobación .
Análisis del microambiente tumoral .
Identificación de biomarcadores .
LA USFDA PERMITE AJUSTES FUTUROS :
Subgrupos .
Nuevas indicaciones .
Cambios en la etiqueta .
IAG . BANK OF AMÉRICA Prevé Que en 2026 el Grupo Anunciará un Programa de Recompra Por 1500 Millones de euros y Que la Remuneración Total al Accionista Podría Superar el 7% Durante el Año . Además, Eleva su Valoración un 8% y Sitúa el Precio Objetivo en 6,09 euros .
CONCLUSIONES CLAVE :
IAG GANA ATRACTIVO BURSÁTIL ANTE LAS PREVISIONES DE BANK OF AMÉRICA, QUE ANTICIPA UNA RECOMPRA DE 1.500 MILLONES EN 2026 Y UN POTENCIAL ALCISTA CERCANO AL 30 % Gracias A LA MEJORA OPERATIVA Y FINANCIERA .
Las Acciones de IAG Celebran la Recomendación de BANK OF AMÉRICA .
IAG vuelve a captar la atención de los inversores ante la posibilidad de que en 2026 adopte una política de retorno al accionista más generosa .
BANK OF AMÉRICA la destaca como su opción preferida dentro del sector aéreo europeo y anticipa un programa de RECOMPRA “ PRUDENTE ” de unos 1.500 MILLONES de euros, respaldado por una fuerte Generación de caja y un balance más sólido . Se basan en la mejora de la rentabilidad operativa y en el incremento del beneficio por acción, que proyectan con una tasa de crecimiento anual del 10% entre 2024 y 2028, junto con un margen EBIT cercano al 15% . También subrayan que la compañía cotiza a un múltiplo atractivo, alrededor de 6,6 veces .
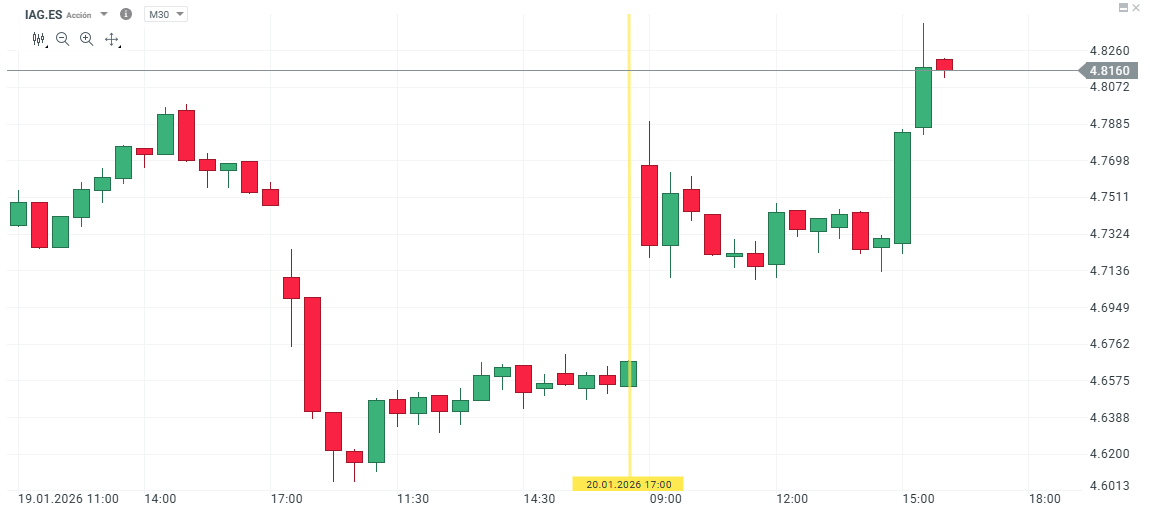
Las Accionesde IAG se disparán un 3,4% intradía hasta los 4,81 euros tras la recomendación de esta casa de análisis .
En el corto plazo, el foco está puesto en los resultados del 27 de febrero.
Tras un tercer trimestre de 2025 más flojo de lo previsto, los inversores buscan confirmar que la mejora operativa continúa y que la generación de caja es suficiente para sostener de forma estable tanto RECOMPRAS COMO DIVIDENDOS .
21 enero 2026
Dr. RAMI MANOCHAKIAN ( MAYO CLINIC ) : IMforte ( LURBINECTEDIN + ATEZOLIZUMAB ) OFRECE UN NUEVO PUNTO DE DEBATE PARA EL MANTENIMIENTO DEL SMALL CELL LUNG CANCER EXTENSIVE-STAGE , CON BENEFICIOS PARA "" ALGUNOS PACIENTES "" , PERO CON UNA TOXICIDAD NOTABLE .
Dr. Rami Manochakian is a thoracic medical Oncologist who joined Mayo Clinic in January 2017.
He earned his medical degree from the University of Aleppo in Syria.
He completed Internal Medicine residency and chief residency at the University at Buffalo, NY.
He completed Hematology/Oncology fellowship and was a chief fellow at Case Western Reserve University, Cleveland, OH .
PHARMAMAR . EL FONDO CORTO SHAW. D.E. & Co COMUNICA A LA CNMV QUE VUELVE A AMPLIAR SU APUESTA BAJISTA HASTA LOS 8,5 MILLONES DE €UROS . YA TIENE UNA POSICIÓN DEL 0,6% CON 108.000 ACCIONES DE LA COMPAÑÍA . LOS FONDOS CORTOS ENTRAN EN UN VALOR ... VENDIENDO SIEMPRE AL ALZA LAS ACCIONES QUE ALGUIEN LE PRESTA ...
EN SHAW CUENTAN CON ANALISTAS ESPECIALIZADOS EN EL SECTOR FARMACÉUTICO QUE INCLUYEN CIENTÍFIC@S , DOCTOR@S , ONCOLOG@S ...
MATEMÁTICOS , INGENIER@S Y PROGRAMADORES ADEMÁS DE FINANCIEROS ...
POR TANTO SUS VALORACIONES SON A TENER MUY EN CUENTA .
D. E. Shaw & Co. es una firma global de inversión y gestión de fondos de cobertura ( HEDGE FUND ) fundada en 1988 por David E. Shaw, un científico de la computación y exprofesor de la Universidad de Columbia .
La empresa es conocida por ser una de las pioneras en el uso de métodos cuantitativos y algorítmicos para invertir en los mercados financieros .
Utiliza modelos matemáticos, análisis estadístico y tecnología avanzada para tomar decisiones de inversión .
INFORMACIÓN CLAVE :
Nombre completo: D. E. Shaw & Co., L.P.
Fundador: David E. Shaw
Año de fundación : 1988
Sede principal : Nueva York, Estados Unidos .
Tipo de empresa : Firma privada de inversión (hedge fund / investment management firm) .
Activos bajo gestión (AUM) : Más de 60 mil millones de USD ( dato aproximado a 2024 ) .
Empleados : Más de 1,600 a nivel mundial .
Características Destacadas :
Usa tecnología avanzada y big data para encontrar oportunidades de inversión .
Emplea a muchos científicos, matemáticos, ingenieros y programadores además de financieros .
Es considerada una de las firmas más secretistas y selectivas de Wall Street .
Fue uno de los lugares donde Jeff Bezos trabajó antes de fundar Amazon .
LOS FONDOS CORTOS ENTRAN EN UN VALOR ... VENDIENDO SIEMPRE AL ALZA LAS ACCIONES QUE ALGUIEN LE PRESTA ...
TAN SOLO HAY UN FONDO BAJISTA A LA VISTA EN LA CNMV ... PERO ANALISTAS REPUTADOS COINCIDEN EN QUE PODRÍAN EXISTIR MÁS FONDOS CORTOS PRESENTES EN LA COMPAÑÍA ... AMPARADOS EN QUE LA CNMV NO LOS PUBLICITA SI NO LLEGAN AL 0,50% ...
20 enero 2026
THE @US_FDA HAS LIFTED THE CLINICAL HOLD ON MERCK / DAIICHI IFINATAMAB DERUXTECAN . ..///..: R&D FOR POTENTIAL FIRST-LINE MAINTENANCE TREATMENT OF SMALL CELL LUNG CANCER , IN COMBINATIÓN WITH ROCHE ATEZOLIZUMAB ( TECENTRIQ ) .
ROCHE Y MERCK .

ROCHE Y MERCK DAIICHI SANKYO ... TRES DE LAS MÁS GRANDES FARMACÉUTICAS GLOBALES Y QUE ACTUALMENTE APUESTAN POR ATEZOLIZUMAB Y IFINATAMAB DERUXTECAN RESPECTIVAMENTE ... COMO POSIBLE TRATAMIENTO DE PRIMERA LÍNEA DE MANTENIMIENTO SMALL CELL LUNG CANCER .
ADEMÁS IFINATAMAB DERUXTECAN TIENE EL PODER DE ACTUAR EN LA METÁSTASIS CRANEALES ( CEREBRO ) ALGO QUE LOS TRATAMIENTOS ACTUALES ... NI POR ASOMO LLEGAN AHI .
CELERIDAD TOTAL EN LAS FASES III TANTO DE PRIMERA LÍNEA , PRIMERA LÍNEA DE MANTENIMIENTO , SEGUNDA LÍNEA ... PARA EL TRATAMIENTO DE SMALL CELL LUNG CANCER EXTENSIVE-STAGE ... PARA PODER ALCANZAR EL MERCADO LO ANTES POSIBLE ...
Y APORTAR A LOS PACIENTES VIDA Y ESPERANZA DONDE EL RESTO DE TRATAMIENTOS NO LLEGAN ... O TAN SOLO APORTAN ALREDEDOR DE 12 MESES DE OVERALL SURVIVAL .
IAG VUELVE A APUNTAR ALTO .///. BANK OF AMÉRICA lo Tiene Claro y Vuela con IAG : "Es Nuestra Aerolínea Preferida " .
https://capitalmadrid.info/2026/1/20/71002/iag-vuelve-a-apuntar-alto.html
LOS EXPERTOS TÉCNICOS HAN DADO POR CONCLUIDA YA LA FASE DE CORRECCIÓN .
Y EMPIEZAN A OBSERVAR LA LLEGADA DE DINERO FRESCO HACIA EL VALOR QUE INVITA a PENSAR EN UN NUEVO IMPULSO POR ENCIMA DE LOS 5 EUROS POR ACCIÓN A CORTO Y MEDIO PLAZO .
Tras un inicio de año muy dubitativo, los operadores están volviendo a poner su punto de mira en IAG. En el mercado ha estado pesando en estas semanas atrás unos resultados del tercer trimestre muy decepcionantes con una caída del 2,4% respecto a igual período del ejercicio anterior, aunque su balanza anual sigue siendo positivo .
Decepción que ha estado animado una pequeña recogida de beneficios desde noviembre .
Un ajuste transitorio, según los analistas, ante la solidez financiera, con sólidos márgenes, y la capacidad de reacción del grupo, con grandes inversiones prevista hasta 2030 que le permitirán aprovechar los vientos a favor del sector .
Las cifras récord de tráfico aéreo tanto en los aeropuertos españoles como en los del Reino Unido, donde tiene una clara posición de liderazgo, alientan la idea de un último trimestre muy positivo para la compañía aérea hispanobritánica .
Frente a los problemas que han estado acuciando al sector como los retrasos en la entrega de aparatos o los cierres de algunas rutas por las tensiones geopolíticas, entre otro, lo cierto es que los moderados costes derivados del precio del crudo y la creciente movilidad aérea, España va a batir récord en turismo rondando los 100 millones de visitantes, permiten retomar las buenas expectativas para IAG .
De momento, la acción se mantiene sin grandes cambios en torno a los precios de principios de año con un consenso de mercado aún expectante .
En cualquier caso, los expertos técnicos han dado por concluida ya la fase de corrección provocada por los últimos resultados trimestrales y empiezan a observar la llegada de dinero fresco hacia el valor que invita a pensar en un nuevo impulso por encima de los 5 euros por acción a corto y medio plazo.
16 enero 2026
EL PANORAMA ALCISTA PARA PHARMAMAR CON LURBINECTEDIN ... PODRÍA CAMBIAR ... DE HECHO LOS ANALISTAS ESPERAN QUE LAS GANANCIAS ALCANCEN TAN SOLO LOS 260,1 MILLONES DE EUROS ( Y UN BENEFICIO POR ACCIÓN DE TAN SOLO 13,15 EUROS ) PARA SEPTIEMBRE DEL 2028 ... Y YA PONEN EN EL TABLERO DE JUEGO TANTO GENERICOS COMO BÍOSIMILARES .
OBJETIVOS PARA 2028 CON LAS ACCIONES DE PHARMAMAR :
Los Analistas Tienen un Precio Objetivo de CONSENSO de 104,6 € Para Pharma Mar, Basándose en Sus Expectativas Sobre el Crecimiento Futuro de Sus Beneficios, Márgenes de Beneficio y Otros Factores de Riesgo .
Sin Embargo, Existe Cierto Desacuerdo Entre los Analistas :
*.- Los Más OPTIMISTAS Informan de un Precio Objetivo de 118 € ...
*.- Mientras Que los Más PESIMISTAS lo Sitúan en Tan Solo 75 €. .
¿ QUE MOTIVOS HAY PARA TENER QUE ESPERAR 34 LARGOS MESES PARA PODER OBTENER TAN SOLO 13 EUROS ... ? ... ¡ SUPONIENDO ENCIMA QUE TODO SALGA RODADO ! :
***.- Los Riesgos Persistentes en Materia Regulatoria y de Acceso al Mercado en Territorios Clave ( Por Ejemplo, las Próximas Decisiones de la EMA y la FDA, los Actuales Procesos de Fijación de Precios, Reembolsos y HTA Específicos de Cada País en Europa , Japón y China ) ...
... Combinados con la Expansión de la Competencia Entre GENERICOS y BÍOSIMILARES , Podrían Inhibir la Adopción Prevista del Producto y Comprimir los Márgenes de Ingresos y Ganancias a Largo Plazo . ...




























.jpeg)





















