Copyright © 2015 American Association for Cancer Research. Citation Format: {Authors}. {Abstract title} [abstract]. In: Proceedings of the 2015 AACR-NCI-EORTC International Conference on Molecular Targets and Cancer Therapeutics;
2015 Nov 5-9 // Boston, Massachusetts. Philadelphia (PA): AACR .
Author Block: Pablo Aviles, Maria Jose Guillen, Juan Manuel Dominguez, Carlos M. Galmarini, Carmen Cuevas. PharmaMar, Colmenar Viejo, Spain .
Abstract Body:
PM050489 is a tubulin-binding agent originally isolated from the marine sponge Lithoplocamia lithistoides.
This compound binds with very high affinity to β-tubulin at a new site, disrupting the microtubule network and impairing its function during divison, which leads to mitotic aberrations.
MI130004 (a novel antibody-drug conjugate formed by PM050489, a non-hydrolysable linker and trastuzumab) was tested for its in vitro and in vivo activity against selected tumor cell lines with different levels of HER2 expression.
In vitro MI130004 showed very high potency and good selectivity for tumor cells that overexpressed HER2, namely HCC-1954 (IC50, 0.036 μg/mL), SK-BR-3 (IC50, 0.017 μg/mL) and BT-474 (IC50, 0.156 μg/mL). At the cellular level, MI130004 impaired tubulin polymerization, causing disorganization and disintegration of the microtubule network which ultimately led to mitotic failure.
Expressing HER2 cells of breast (BT-474 and JIMT-1), gastric (Gastric-008 and N87) and ovarian (SK-OV-3 and A2780cis) as well as negative HER2 breast (MDA-MB-231) and gastric (Hs748t) were subcutaneously implanted into immunosuppressed (SCID or athymic) mice. Tumor (ca. 115 mm3) bearing animals (N=10/group) were randomly allocated to receive the ADC treatments (at different doses) or the appropriate control (placebo included). Treatments were administered weekly for 5 consecutive weeks.
Tumor growth (as median/group) was calculated 2-3 times per week. Twenty-four hours after the first dose, representative tumors were dissected free and processed for HER2 expression (erb2) and chromatin organization (Hoescht 33258). The treatment with MI130004 induced a long lasting antitumor effect with statistically significant increases (P 0.05) in median survival time compared to placebo.
The highest dose of MI130004 induced complete tumor remissions in mice bearing BT-474, JIMT-1, Gastric-008, N87, SK-OV-3 and A2780cis xenografts lasting up to 120, 60, 165, 63, 237 and 231 days, respectively. Also 24-h post-dosing, MI130004 induced a dose-dependent disappearance of HER2-expressing cells as well as mitotic aberrations, this last being consistent with the mechanism of action of PM050489.
These results demonstrate that PM050489, a marine derived compound, is a novel and remarkable payload for the design of new ADCs with potential therapeutic anti-cancer properties.
IMFORTE . Desde JazzPharma Siguen Anclados en los Resultados del Corte Intermedio Realizado Por ROCHE en 2024 Cuyos Datos Fueron Presentados en ASCO25 , Revista Especializada Y en la US-FDA ... Repetidos Ya Miles de Veces Sin Variar Ni una Sola Coma ... Queda Claro Qué Nada Nuevo Tienen ... Y Eso a Fecha de Hoy Da Qué Pensar ...
09 noviembre 2015
08 noviembre 2015
Aceite de Girasol Calentado, Vinculado al Cáncer y la Demencia porque Emiten Químicos Tóxicos .
El estudio lo publica el diario británico Telegraph en su versión de hoy domingo recogiendo los datos de un estudio realizado por algunos de los mayores expertos en la materia. Cocinar con aceites vegetales emiten productos químicos vinculados al cáncer y a otras enfermedades. La recomendación es que se use aceite de oliva, o de coco, e incluso mantequilla es mejor que el aceite de girasol. Los resultados de una serie de experimentos amenazan la idea de que las aceites ricas en grasas polisaturadas como el aceite de maíz o de girasol son mejores para la salud que las grasas saturadas en los productos animales.
Científicos han encontrado que calentar los aceites vegetales hace que emitan altas concentraciones de químicos llamados aldehídos, tradicionalmente vinculados con enfermedades como el cáncer, problemas cardiacos y demencia.
Martín Grootveld, un profesor de química bioanalítica y patología química dice que su investigación mostró que la típica comida de pescado y patatas fritas freídas en aceite de girasol contenía de 100 a 200 veces más aldehídos que los límites diarios seguros indicados por la Organización Mundial de la Salud.
En contraste, calentar la mantequilla, aceite de oliva en pruebas similares, han emitido niveles muchos más bajos de Aldehídos. Incluso el aceite de coco es el más indicado por sus menores niveles de productos químicos dañinos.
...
Científicos han encontrado que calentar los aceites vegetales hace que emitan altas concentraciones de químicos llamados aldehídos, tradicionalmente vinculados con enfermedades como el cáncer, problemas cardiacos y demencia.
Martín Grootveld, un profesor de química bioanalítica y patología química dice que su investigación mostró que la típica comida de pescado y patatas fritas freídas en aceite de girasol contenía de 100 a 200 veces más aldehídos que los límites diarios seguros indicados por la Organización Mundial de la Salud.
En contraste, calentar la mantequilla, aceite de oliva en pruebas similares, han emitido niveles muchos más bajos de Aldehídos. Incluso el aceite de coco es el más indicado por sus menores niveles de productos químicos dañinos.
...
Grifols : Los resultados intermedios del estudio 'AMBAR' sobre Alzheimer apoyan su continuidad .
06.11.15 | EUROPA PRESS | MADRID .
Grifols ha presentado los resultados de un análisis intermedio de su estudio 'AMBAR', que ensaya la combinación de la extracción de plasma y su reposición con albúmina (recambio plasmático), la proteína más abundante en el plasma sanguíneo, con el objetivo de estabilizar la enfermedad de Alzheimer (EA).
Tras analizar la tolerabilidad y seguridad del tratamiento, los resultados de este análisis intermedio del estudio 'AMBAR' apoyan la continuidad del ensayo. En este sentido, los resultados ponen de manifiesto que el perfil de acontecimientos adversos presentado es el esperado y que los pacientes de Alzheimer en estadio medio-moderado que participan pueden tratarse de manera rutinaria. Es decir, que el tratamiento es factible en las condiciones del ensayo.
Los investigadores no han analizado la eficacia del tratamiento ya que se trata de un estudio ciego en el que hasta el final del ensayo no se conocerá qué pacientes han recibido tratamiento y cuáles no. Actualmente ya se han reclutado 250 pacientes y Grifols prevé presentar los resultados preliminares de 'AMBAR' en 2017.
Tal y como estaba previsto, los resultados intermedios de este ensayo clínico en fase III se han presentado en el 'VIII Congreso Internacional Clinical Trials on Alzheimer's Disease' (CTAD) celebrado en Barcelona.
'AMBAR' es un estudio internacional y multicéntrico en el que se incluirán 365 enfermos de Alzheimer en estadio leve-moderado asignados aleatoriamente a tres grupos de tratamiento más un cuarto grupo de control en 40 hospitales de España y Estados Unidos.
Grifols ha presentado los resultados de un análisis intermedio de su estudio 'AMBAR', que ensaya la combinación de la extracción de plasma y su reposición con albúmina (recambio plasmático), la proteína más abundante en el plasma sanguíneo, con el objetivo de estabilizar la enfermedad de Alzheimer (EA).
Tras analizar la tolerabilidad y seguridad del tratamiento, los resultados de este análisis intermedio del estudio 'AMBAR' apoyan la continuidad del ensayo. En este sentido, los resultados ponen de manifiesto que el perfil de acontecimientos adversos presentado es el esperado y que los pacientes de Alzheimer en estadio medio-moderado que participan pueden tratarse de manera rutinaria. Es decir, que el tratamiento es factible en las condiciones del ensayo.
Los investigadores no han analizado la eficacia del tratamiento ya que se trata de un estudio ciego en el que hasta el final del ensayo no se conocerá qué pacientes han recibido tratamiento y cuáles no. Actualmente ya se han reclutado 250 pacientes y Grifols prevé presentar los resultados preliminares de 'AMBAR' en 2017.
Tal y como estaba previsto, los resultados intermedios de este ensayo clínico en fase III se han presentado en el 'VIII Congreso Internacional Clinical Trials on Alzheimer's Disease' (CTAD) celebrado en Barcelona.
'AMBAR' es un estudio internacional y multicéntrico en el que se incluirán 365 enfermos de Alzheimer en estadio leve-moderado asignados aleatoriamente a tres grupos de tratamiento más un cuarto grupo de control en 40 hospitales de España y Estados Unidos.
Cáncer de Páncreas será el segundo Tumor más Mortal en España .
*.- Los especialistas alertan de que es una de las enfermedades con peor pronóstico y su elevada letalidad responde a la dificultad del diagnóstico .
Vida | 08/11/2015 .
(Europa Press, Madrid). El cáncer de páncreas no es de los más frecuentes en España, con 6.500 nuevos casos cada año (mientras que de otros como el de mama o el de pulmón se dan unos 25.000), pero su elevada letalidad y los avances que sí se están produciendo en otros tumores va a provocar que en los próximos 5-10 años se convierta en la segunda causa de muerte por cáncer, solo por detrás del de pulmón. "Es una emergencia sanitaria, no hay un tumor con tan mal pronóstico", ha asegurado en declaraciones a Europa Press el jefe de Servicio de Oncología Médica del Hospital Universitario Ramón y Cajal de Madrid, Alfredo Carrato, con motivo de una carrera popular organizada este domingo por la Asociación de Cáncer de Páncreas y la Asociación Española de Pancreatología con motivo del Día Mundial que se celebra el 13 de noviembre.
Actualmente, estos tumores tienen una mortalidad del 95 por ciento cinco años después del diagnóstico, ya que la supervivencia media está en unos 5-6 meses y solo uno de cada cuatro supera el año de vida. "El cáncer de páncreas está como el resto de tumores hace 30 años", ha apuntado este experto, que reconoce que el principal hándicap para no lograr mejorar su pronóstico está la dificultad de su diagnóstico, lo que hace que cuando se detecte el tumor esté muy avanzado "y ya no sea curable".
La dificultad del diagnóstico
Los síntomas son muy variados y pueden corresponderse con otras alteraciones y, según ha explicado Carrato, "eso hace que se tarde muchos meses en el diagnóstico, y eso va en contra del pronóstico del paciente". Entre los más frecuentes destacan malestar abdominal que "aparentemente no tiene gravedad", malas digestiones, diarrea o deposiciones pastosas porque la grasa no se digiere, dolor de espalda o una diabetes repentina en paciente de 45-50 años. En la mayoría de los casos, salvo el 7-8 por ciento que tienen un origen familiar por causas genéticas, su aparición obedece a múltiples factores como el tabaco, el sobrepeso u otros trastornos, lo que también impide poner en marcha programas de detección precoz como hay en otros tumores (mamografías en cáncer de mama, sangre oculta en heces en colorrectal).
Además, las pruebas que permiten detectarlo son complejas ya que es un órgano de difícil acceso y tiene en su interior enzimas digestivas, por lo que no se puede hacer biopsia desde fuera sino a través de una ecoendoscopia, cuya fiabilidad "es mucho menor". En cuanto a su tratamiento, el rápido desarrollo de la enfermedad es también un obstáculo de cara a experimentar con nuevas moléculas, ha reconocido este oncólogo.
...
Vida | 08/11/2015 .
(Europa Press, Madrid). El cáncer de páncreas no es de los más frecuentes en España, con 6.500 nuevos casos cada año (mientras que de otros como el de mama o el de pulmón se dan unos 25.000), pero su elevada letalidad y los avances que sí se están produciendo en otros tumores va a provocar que en los próximos 5-10 años se convierta en la segunda causa de muerte por cáncer, solo por detrás del de pulmón. "Es una emergencia sanitaria, no hay un tumor con tan mal pronóstico", ha asegurado en declaraciones a Europa Press el jefe de Servicio de Oncología Médica del Hospital Universitario Ramón y Cajal de Madrid, Alfredo Carrato, con motivo de una carrera popular organizada este domingo por la Asociación de Cáncer de Páncreas y la Asociación Española de Pancreatología con motivo del Día Mundial que se celebra el 13 de noviembre.
Actualmente, estos tumores tienen una mortalidad del 95 por ciento cinco años después del diagnóstico, ya que la supervivencia media está en unos 5-6 meses y solo uno de cada cuatro supera el año de vida. "El cáncer de páncreas está como el resto de tumores hace 30 años", ha apuntado este experto, que reconoce que el principal hándicap para no lograr mejorar su pronóstico está la dificultad de su diagnóstico, lo que hace que cuando se detecte el tumor esté muy avanzado "y ya no sea curable".
La dificultad del diagnóstico
Los síntomas son muy variados y pueden corresponderse con otras alteraciones y, según ha explicado Carrato, "eso hace que se tarde muchos meses en el diagnóstico, y eso va en contra del pronóstico del paciente". Entre los más frecuentes destacan malestar abdominal que "aparentemente no tiene gravedad", malas digestiones, diarrea o deposiciones pastosas porque la grasa no se digiere, dolor de espalda o una diabetes repentina en paciente de 45-50 años. En la mayoría de los casos, salvo el 7-8 por ciento que tienen un origen familiar por causas genéticas, su aparición obedece a múltiples factores como el tabaco, el sobrepeso u otros trastornos, lo que también impide poner en marcha programas de detección precoz como hay en otros tumores (mamografías en cáncer de mama, sangre oculta en heces en colorrectal).
Además, las pruebas que permiten detectarlo son complejas ya que es un órgano de difícil acceso y tiene en su interior enzimas digestivas, por lo que no se puede hacer biopsia desde fuera sino a través de una ecoendoscopia, cuya fiabilidad "es mucho menor". En cuanto a su tratamiento, el rápido desarrollo de la enfermedad es también un obstáculo de cara a experimentar con nuevas moléculas, ha reconocido este oncólogo.
...
06 noviembre 2015
Pharmamar se Posiciona tambien en la Novedosa Linea de Tratamientos Oncologicos con un Anticuerpo Conjugado . ¿ En que consiste esta Nueva tecnica ? .
PD : En el caso de PharmaMar el Anticuerpo Conjugado MI130004 está compuesto por un nuevo Inhibidor de Tubulina de Origen Marino (PM050489) que está unido de manera Covalente al Anticuerpo Anti-HER2 Trastuzumab Mediante un Linker.
*****************************************************
La Noticia saltaba al Mercado Oncologico en el 2013 ... ROCHE conseguía la Aprobación por parte de la FDA de “ KADZILA ( TDM-1 ) que se convertía en el Primer Anticuerpo Conjugado eficaz contra el Cáncer de Mama HER2 Positivo” .
Por lo tanto para intentar ver en que consiste esta nueva linea Tumoral deberemos fijarnos en el Anticueropo KADZILA :
*.- KADZILA se dice que es una especie de caballo de Troya por su modo de acción.
*.- Se trata de una combinación de dos fármacos, el anticuerpo monoclonal trastuzumab DCI , que va dirigido a las células cancerosas (la diana terapéutica) y el citostático clásico DM1, que es como la quimioterapia convencional pero que, gracias a que está dirigido por el anticuerpo monoclonal (que utilizado en solitario también es efectivo), se dirige exclusivamente a la zona afectada por la enfermedad disminuyendo la toxicidad del tratamiento.
¿Por qué representa una novedad? :
Es un fármaco que, en un solo compuesto, engloba dos moléculas y por tanto, logra una doble acción que, hasta el momento, alcanzábamos usando dos moléculas diferentes (que no son las que ahora se unen en KADZILA ).
¿Qué resultados se estan obtenido con este ADC ? :
Podemos hablar de resultados muy esperanzadores. Las mujeres que recibieron KADZILA redujeron en un 35% el riesgo de empeoramiento o muerte del paciente; eso supone que estas mujeres vivieron más tiempo sin que la enfermedad progresase: una media de 9,6 meses frente a los 6,4 meses en el grupo que recibió el tratamiento convencional basado en la administración de Capecitabina más Lapatinib (HR=0,65, P + 0.0001). Por lo tanto, este nuevo esquema podría proporcionar más opciones a aquellas pacientes que más lo necesitan tras recaída de su enfermedad.
También se han obtenido resultados de la supervivencia a un año que en pacientes que recibieron KADZILA fue del 84,7% frente al 77% del grupo de Lapatinib más Capecitabina. A los dos años, la supervivencia fue de 65,4% frente al 47,5%, respectivamente.
En cuanto a la tasa de respuesta objetiva (el porcentaje de pacientes con reducción del tamaño del tumor) fue de 43,6% en el grupo KADZILA frente al 30,8% registrado en las pacientes que recibieron Lapatinib más Capecitabina; y el periodo de tiempo que transcurrió hasta presentar síntomas también fue mayor en las tratadas con T-DM1: 7,1 meses frente a los 4,6 meses del otro grupo.
¿Cómo puede influir esto en los actuales tratamientos contra el cáncer de mama? ¿Cómo mejora o complementa a otros tratamientos? :
Este anticuerpo conjugado supone un claro avance porque disminuye la toxicidad, uno de los grandes retos de este tipo de fármacos. De hecho, en el grupo tratado con KADZILA, un número menor de pacientes experimentó efectos secundarios de grado mayor o igual a 3 frente a las que recibieron Lapatinib más Capecitabina (40,8% frente a 57%, respectivamente).
PharmaMar Presenta Nuevos Datos de la Eficacia de 'Yondelis' frente a Sarcomas de Tejidos Blandos en el Congreso CTOS que se Celebra en EEUU .
MADRID, 6 Nov. (EUROPA PRESS) -
PharmaMar ha anunciado que presentará nuevos estudios sobre la eficacia de la trabectedina, comercializado con el nombre de 'Yondelis', como tratamiento frente al sarcoma de tejidos blandos en el congreso internacional de la Sociedad Oncológica de Tejido Conectivo (CTOS, por sus siglas en inglés) que se celebra estos días en Salt Lake City (Estados Unidos).
Este encuentro reúne a expertos en oncología y científicos que trabajan por avanzar el conocimiento en torno a los aspectos biológicos de los tumores del tejido conectivo, incluyendo la investigación básica y la clínica.
En este sentido, Pharma Mar ha organizado un encuentro dirigido por el oncólogo español Javier Martín Broto, presidente del Grupo Español de Investigación en Sarcomas, para analizar la trayectoria clínica de trabectedina en el tratamiento de sarcoma de tejidos blandos desde los primeros ensayos clínicos llevados a cabo hasta su comercialización en la Unión Europea y Estados Unidos.
Hasta la fecha se han tratado aproximadamente 50.000 pacientes en todo el mundo con este fármaco antitumoral, que reduce el tamaño del tumor y disminuye su densidad, dos criterios clínicos que deben tenerse en cuenta si se valora la respuesta tumoral al tratar a los pacientes con este medicamento.
"Reconocer el tipo de respuesta con trabectedina es clave para que los oncólogos eviten interrupciones innecesarias de un tratamiento que puede resultar efectivo y cuyo beneficio clínico puede continuar después de 6 ciclos de tratamiento, en algunos casos", ha apuntado Martín Broto.
Precisamente los ensayos clínicos llevados a cabo por el Grupo francés de Sarcomas a lo largo del 2015 han determinado que "cuando el tratamiento con trabectedina continúa hasta la progresión de la enfermedad, en lugar de interrumpirse en el ciclo 6, se observa un retraso en la siguiente recaída".
PharmaMar ha anunciado que presentará nuevos estudios sobre la eficacia de la trabectedina, comercializado con el nombre de 'Yondelis', como tratamiento frente al sarcoma de tejidos blandos en el congreso internacional de la Sociedad Oncológica de Tejido Conectivo (CTOS, por sus siglas en inglés) que se celebra estos días en Salt Lake City (Estados Unidos).
Este encuentro reúne a expertos en oncología y científicos que trabajan por avanzar el conocimiento en torno a los aspectos biológicos de los tumores del tejido conectivo, incluyendo la investigación básica y la clínica.
En este sentido, Pharma Mar ha organizado un encuentro dirigido por el oncólogo español Javier Martín Broto, presidente del Grupo Español de Investigación en Sarcomas, para analizar la trayectoria clínica de trabectedina en el tratamiento de sarcoma de tejidos blandos desde los primeros ensayos clínicos llevados a cabo hasta su comercialización en la Unión Europea y Estados Unidos.
Hasta la fecha se han tratado aproximadamente 50.000 pacientes en todo el mundo con este fármaco antitumoral, que reduce el tamaño del tumor y disminuye su densidad, dos criterios clínicos que deben tenerse en cuenta si se valora la respuesta tumoral al tratar a los pacientes con este medicamento.
"Reconocer el tipo de respuesta con trabectedina es clave para que los oncólogos eviten interrupciones innecesarias de un tratamiento que puede resultar efectivo y cuyo beneficio clínico puede continuar después de 6 ciclos de tratamiento, en algunos casos", ha apuntado Martín Broto.
Precisamente los ensayos clínicos llevados a cabo por el Grupo francés de Sarcomas a lo largo del 2015 han determinado que "cuando el tratamiento con trabectedina continúa hasta la progresión de la enfermedad, en lugar de interrumpirse en el ciclo 6, se observa un retraso en la siguiente recaída".
Yondelis . Sant P. Chawla, MD, director, Sarcoma Oncology Center, discusses the potential for trabectedin as treatment of mesenchymal chondrosarcoma.
Sant P. Chawla, MD // Published Online: 6:32 PM, Thu November 5, 2015 .
Trabectedin for the Treatment of Mesenchymal Chondrosarcoma .
Mesenchymal chondrosarcoma is a very rare disease that often has a lot of potential to metastasize, Chawla says.
In this small study of fewer than 20 patients, some patients had previously failed standard chemotherapy and trabectedin did control disease in some of those patients for up to two years.
Moving forward, Chawla says, there will first need to be collaboration between institutions and pharmaceutical companies to determine if similar results have been seen before.
...
Trabectedin for the Treatment of Mesenchymal Chondrosarcoma .
Mesenchymal chondrosarcoma is a very rare disease that often has a lot of potential to metastasize, Chawla says.
In this small study of fewer than 20 patients, some patients had previously failed standard chemotherapy and trabectedin did control disease in some of those patients for up to two years.
Moving forward, Chawla says, there will first need to be collaboration between institutions and pharmaceutical companies to determine if similar results have been seen before.
...
05 noviembre 2015
Yondelis . Según el Presidente del Grupo Español de Sarcomas ( Javier Martin Broto ) " es un Exito Terapeutico que un Tumor No vuelva a Crecer ".
Yondelis tiene un valor añadido para los pacientes con sarcomas de tejido blando. «Su uso no tiene tanto impacto en la calidad de vida del paciente; no tiene una toxicidad acumulativa en distintos órganos, por lo que se puede utilizar durante un tiempo ilimitado de ciclos; no es alopécico, por lo que no produce la caída de cabello y, bien manejado el tratamiento, los pacientes pueden llevar una vida razonablemente normal», apunta Javier Martín Broto, presidente del Grupo Español de Sarcomas.
*.- El objetivo del fármaco no es reducir el volumen de este tipo de tumor, sino «controlar su crecimiento», añade Martín Broto.
*.- Es un éxito terapéutico que un tumor no vuelva a crecer.
La Agencia de Alimentos y Medicamentos de Estados Unidos (FDA) ha aprobado la comercialización de la trabectedina, fármaco de la empresa farmacéutica PharmaMar y registrado con el nombre de Yondelis, para el tratamiento de pacientes con liposarcoma (LPS) o leiomiosarcoma (LMS) –dos subtipos de sarcoma de tejidos blandos (STB)– irresecable o metastásico, que han recibido al menos un tratamiento con antraciclina.
El liposarcoma y el leiomiosarcoma representan aproximadamente el 35 por ciento de todos los casos de sarcoma de tejidos blando, de los cuales hay 50 subtipos. El primero tiene su origen en las células adiposas y aparece con mayor frecuencia en el muslo y en la cavidad abdominal, aunque puede aparecer en las células adiposas de cualquier parte del cuerpo. Mientras que el leiomiosarcoma es un tipo agresivo de sarcoma de tejidos blando que se da en el músculo liso, como puede ser el útero, el tracto gastrointestinal o el recubrimiento de los vasos sanguíneos.
Este nuevo medicamento es un agente antitumoral que se produce de manera sintética que ejerce su actividad en las células tumorales a través de la interacción con el complejo de transcripción y bloqueando la reparación de ADN, induciendo de esta manera la muerte de las células tumorales. Su aprobación se ha basado en los datos clínicos relacionados con la eficacia y la seguridad demostrados en un estudio recientemente publicado, que evaluaba trebectedina frente a dacarbacina en la población de estos pacientes.
El ensayo pivotal confirma los resultados obtenidos en estudios clínicos anteriores y proporciona una evidencia científica sobre su beneficio clínico. Este permiso de uso por parte de los americanos supone «la inclusión del fármaco en las guías terapéuticas informacionales», según explica Luis Mora, director general de PharmaMar. Además de que esta aprobación en EE UU permita «que muchos más pacientes con esta enfermedad puedan acceder a un fármaco que da respuesta a una necesidad médica no cubierta antes».
El uso de este fármaco tiene un valor añadido para los pacientes con sarcomas de tejido blando. «Su uso no tiene tanto impacto en la calidad de vida del paciente; no tiene una toxicidad acumulativa en distintos órganos, por lo que se puede utilizar durante un tiempo ilimitado de ciclos; no es alopécico, por lo que no produce la caída de cabello y, bien manejado el tratamiento, los pacientes pueden llevar una vida razonablemente normal», apunta Javier Martín Broto, presidente del Grupo Español de Sarcomas. El objetivo del fármaco no es reducir el volumen de este tipo de tumor, sino «controlar su crecimiento», añade Martín Broto. Es un éxito terapéutico que un tumor no vuelva a crecer.
Para un futuro, otras dos indicaciones adicionales se encuentran en fase de desarrollo clínico. Para el meningioma, un tipo de tumor cerebral, y para el mesotelioma, que está acabado en la fase II. Si los resultados son positivos, como indica Mora, «darán lugar a otros dosieres de registro de petición de autorización».
El fármaco de origen marino en Europa también se utiliza desde el 2009 para tratar algunos tipos de cáncer como el de ovario. Actualmente, Janssen Biotech Inc, socio de PharmaMar en EE UU, está trabajando en un ensayo clínico para una futura aprobación del fármaco en este tipo de cáncer.
Desde que el uso de la trabectedina se aprobó por primera vez en Europa en el año 2007, aproximadamente 50.000 pacientes en 80 países de Norteamérica, Europa, América del Sur y Asia ya se han beneficiado de esta terapia en todas sus indicaciones aceptadas. «La aprobación de la trabectedina en Estados Unidos permite que muchos más pacientes con esta enfermedad puedan acceder a un fármaco que da respuesta a una necesidad médica no cubierta», comenta Luis Mora.
*.- El objetivo del fármaco no es reducir el volumen de este tipo de tumor, sino «controlar su crecimiento», añade Martín Broto.
*.- Es un éxito terapéutico que un tumor no vuelva a crecer.
La Agencia de Alimentos y Medicamentos de Estados Unidos (FDA) ha aprobado la comercialización de la trabectedina, fármaco de la empresa farmacéutica PharmaMar y registrado con el nombre de Yondelis, para el tratamiento de pacientes con liposarcoma (LPS) o leiomiosarcoma (LMS) –dos subtipos de sarcoma de tejidos blandos (STB)– irresecable o metastásico, que han recibido al menos un tratamiento con antraciclina.
El liposarcoma y el leiomiosarcoma representan aproximadamente el 35 por ciento de todos los casos de sarcoma de tejidos blando, de los cuales hay 50 subtipos. El primero tiene su origen en las células adiposas y aparece con mayor frecuencia en el muslo y en la cavidad abdominal, aunque puede aparecer en las células adiposas de cualquier parte del cuerpo. Mientras que el leiomiosarcoma es un tipo agresivo de sarcoma de tejidos blando que se da en el músculo liso, como puede ser el útero, el tracto gastrointestinal o el recubrimiento de los vasos sanguíneos.
Este nuevo medicamento es un agente antitumoral que se produce de manera sintética que ejerce su actividad en las células tumorales a través de la interacción con el complejo de transcripción y bloqueando la reparación de ADN, induciendo de esta manera la muerte de las células tumorales. Su aprobación se ha basado en los datos clínicos relacionados con la eficacia y la seguridad demostrados en un estudio recientemente publicado, que evaluaba trebectedina frente a dacarbacina en la población de estos pacientes.
El ensayo pivotal confirma los resultados obtenidos en estudios clínicos anteriores y proporciona una evidencia científica sobre su beneficio clínico. Este permiso de uso por parte de los americanos supone «la inclusión del fármaco en las guías terapéuticas informacionales», según explica Luis Mora, director general de PharmaMar. Además de que esta aprobación en EE UU permita «que muchos más pacientes con esta enfermedad puedan acceder a un fármaco que da respuesta a una necesidad médica no cubierta antes».
El uso de este fármaco tiene un valor añadido para los pacientes con sarcomas de tejido blando. «Su uso no tiene tanto impacto en la calidad de vida del paciente; no tiene una toxicidad acumulativa en distintos órganos, por lo que se puede utilizar durante un tiempo ilimitado de ciclos; no es alopécico, por lo que no produce la caída de cabello y, bien manejado el tratamiento, los pacientes pueden llevar una vida razonablemente normal», apunta Javier Martín Broto, presidente del Grupo Español de Sarcomas. El objetivo del fármaco no es reducir el volumen de este tipo de tumor, sino «controlar su crecimiento», añade Martín Broto. Es un éxito terapéutico que un tumor no vuelva a crecer.
Para un futuro, otras dos indicaciones adicionales se encuentran en fase de desarrollo clínico. Para el meningioma, un tipo de tumor cerebral, y para el mesotelioma, que está acabado en la fase II. Si los resultados son positivos, como indica Mora, «darán lugar a otros dosieres de registro de petición de autorización».
El fármaco de origen marino en Europa también se utiliza desde el 2009 para tratar algunos tipos de cáncer como el de ovario. Actualmente, Janssen Biotech Inc, socio de PharmaMar en EE UU, está trabajando en un ensayo clínico para una futura aprobación del fármaco en este tipo de cáncer.
Desde que el uso de la trabectedina se aprobó por primera vez en Europa en el año 2007, aproximadamente 50.000 pacientes en 80 países de Norteamérica, Europa, América del Sur y Asia ya se han beneficiado de esta terapia en todas sus indicaciones aceptadas. «La aprobación de la trabectedina en Estados Unidos permite que muchos más pacientes con esta enfermedad puedan acceder a un fármaco que da respuesta a una necesidad médica no cubierta», comenta Luis Mora.
PharmaMar , Precio Objetivo 5,80 euros según Alvaro Aristegui de Ahorro y Corporación .
... Aprobación del Yondelis en EEUU .
«Era algo esperado porque era absurdo que no se vendiera en Estados Unidos, cuando se vende en más de 80 países. Por eso, la gente se estuvo posicionando en octubre y, después, hizo caja», explica Álvaro Arístegui, de Ahorro Corporación.
«Desde los mínimos de agosto, la acción había subido casi un 20 por ciento por las expectativas de la aprobación. Nosotros contábamos con ello y lo teníamos metido en los números», coincide Elena Fernández, de Intermoney Valores.
No obstante, varios especialistas coinciden en señalar que la compañía tiene otros catalizadores en el horizonte que sí podrían impulsar el valor en el medio plazo.
El más inmediato es la posible salida a bolsa en Wall Street, un acontecimiento que incrementará la visibilidad de la compañía entre los grandes inversores institucionales del mundo.
«Esto sería probablemente en la segunda mitad de 2016. Y sería positivo porque Estados Unidos es un mercado mucho mayor, donde hay fondos especializados en biotecnología», relata Elena Fernández.
También Arístegui cree que la cotización en Wall Street podría «ser un catalizador, pues compañías de este tipo en Estados Unidos alcanzan valoraciones muy superiores».
«Aunque la operación suponga una cierta dilución porque se hará una ampliación de capital de entre 75 y 100 millones de euros, según mis cálculos, puede ser un catalizador si ese dinero se emplea en el desarrollo de productos», dice por su parte Ana Isabel González, de Beka Finance.
Una de las medidas que la compañía ha tomado para prepararse de cara a la aventura americana es una fusión inversa con su filial de biotecnología Pharmamar (fabricante de Yondelis).
«Zeltia es un conglomerado que tiene una parte química. Ahora, la compañía quiere dejar claro que el núcleo de su empresa es el negocio biofarmacéutico», de cara a explicar mejor su negocio a los inversores en Estados Unidos relata Arístegui.
En todo caso, la medida no debe preocupar a los inversores, a los que no afectará en nada, más allá de que la compañía pasará a cotizar como Pharmamar en lugar de Zeltia, el 2 de noviembre. «Lo que se va a hacer es un canje de una acción por otra, que no tiene ningún impacto fiscal para el accionista», cuenta Ana Isabel González.
Precisamente y de cara a destacar el negocio estratégico de la compañía, una de las opciones que hay sobre la mesa es la venta del negocio de química de gran consumo, otro de los hitos que podrían impulsar el valor, según Fernández. «Creemos que sería bueno, sobre todo para salir en Estados Unidos. Porque irían como una pura «biotech» y no como una química con una parte de biotecnología», dice. Si bien, hay quien piensa que Zeltia podría encontrar dificultades para identificar a un comprador que quiera pagar un precio adecuado.
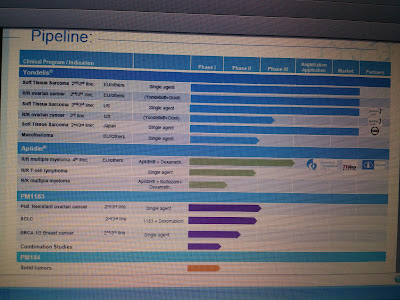
Por último, hay otro factor del que están pendientes los analistas: la cartera de nuevos fármacos, lo que los expertos llaman «pipeline» y que en fútbol se conoce como «cantera».
«Lo más interesante de la compañía está por venir. Tiene un producto, el PM1183, que está en fase III en cáncer de ovario platino-resistente. Los resultados de la fase II fueron muy positivos y hay un hueco en el mercado», relata González, quien añade que el mismo fármaco también podría emplearse en cáncer de pulmón microcítico, que supone en torno al 15-20 por ciento del cáncer de pulmón y no cuenta con tratamientos eficaces, a diferencia del de ovario. «Ahí sí que podría posicionarse fuerte. El mayor revulsivo sería éste y el mercado aún no lo ha recogido», dice.
nuevos productos
No obstante, avisa de que habrá que esperar al menos un par de años para que el fármaco llegue al mercado y, eso, suponiendo que los ensayos tengan éxito, pues hay que tener en cuenta que «todos estos desarrollos tienen un riesgo regulatorio».
Precisamente, este riesgo regulatorio es la principal dificultad a la hora de valorar este tipo de compañías, tal y como explica Arístegui: «Haces una valoración conservadora teniendo en cuenta que los medicamentos se aprueben. Pero, si finalmente se aprueban, la empresa vale mucho más y, si no se aprueban, mucho menos». Esto es lo que ha motivado tanta especulación en torno a Zeltia en los últimos años.
De cara al futuro, Arístegui recomienda comprar con un precio objetivo de 5,80 euros, muy por encima de los 4,60 del consenso de los analistas recogido por Bloomberg. Arístegui la valora así porque considera que el nuevo antitumoral tiene «incluso más potencial que Yondelis» y el mercado irá reconociéndolo, aunque no a corto plazo, cuando espera que la acción «se quede un poco parada porque las noticias relevantes ya han sido». En ese sentido, cree que una buena estrategia sería aprovechar la recogida de beneficios «para posicionarse a largo plazo».
En cambio, no todos los analistas son positivos con el valor. Felipe Echevarría, de Sabadell, por ejemplo, cree que todas estas noticias están en precio y descarta entrar en Zeltia, donde -con un precio objetivo de 4,3 euros- «no queda potencial».
«Era algo esperado porque era absurdo que no se vendiera en Estados Unidos, cuando se vende en más de 80 países. Por eso, la gente se estuvo posicionando en octubre y, después, hizo caja», explica Álvaro Arístegui, de Ahorro Corporación.
«Desde los mínimos de agosto, la acción había subido casi un 20 por ciento por las expectativas de la aprobación. Nosotros contábamos con ello y lo teníamos metido en los números», coincide Elena Fernández, de Intermoney Valores.
No obstante, varios especialistas coinciden en señalar que la compañía tiene otros catalizadores en el horizonte que sí podrían impulsar el valor en el medio plazo.
El más inmediato es la posible salida a bolsa en Wall Street, un acontecimiento que incrementará la visibilidad de la compañía entre los grandes inversores institucionales del mundo.
«Esto sería probablemente en la segunda mitad de 2016. Y sería positivo porque Estados Unidos es un mercado mucho mayor, donde hay fondos especializados en biotecnología», relata Elena Fernández.
También Arístegui cree que la cotización en Wall Street podría «ser un catalizador, pues compañías de este tipo en Estados Unidos alcanzan valoraciones muy superiores».
«Aunque la operación suponga una cierta dilución porque se hará una ampliación de capital de entre 75 y 100 millones de euros, según mis cálculos, puede ser un catalizador si ese dinero se emplea en el desarrollo de productos», dice por su parte Ana Isabel González, de Beka Finance.
Una de las medidas que la compañía ha tomado para prepararse de cara a la aventura americana es una fusión inversa con su filial de biotecnología Pharmamar (fabricante de Yondelis).
«Zeltia es un conglomerado que tiene una parte química. Ahora, la compañía quiere dejar claro que el núcleo de su empresa es el negocio biofarmacéutico», de cara a explicar mejor su negocio a los inversores en Estados Unidos relata Arístegui.
En todo caso, la medida no debe preocupar a los inversores, a los que no afectará en nada, más allá de que la compañía pasará a cotizar como Pharmamar en lugar de Zeltia, el 2 de noviembre. «Lo que se va a hacer es un canje de una acción por otra, que no tiene ningún impacto fiscal para el accionista», cuenta Ana Isabel González.
Precisamente y de cara a destacar el negocio estratégico de la compañía, una de las opciones que hay sobre la mesa es la venta del negocio de química de gran consumo, otro de los hitos que podrían impulsar el valor, según Fernández. «Creemos que sería bueno, sobre todo para salir en Estados Unidos. Porque irían como una pura «biotech» y no como una química con una parte de biotecnología», dice. Si bien, hay quien piensa que Zeltia podría encontrar dificultades para identificar a un comprador que quiera pagar un precio adecuado.
Por último, hay otro factor del que están pendientes los analistas: la cartera de nuevos fármacos, lo que los expertos llaman «pipeline» y que en fútbol se conoce como «cantera».
«Lo más interesante de la compañía está por venir. Tiene un producto, el PM1183, que está en fase III en cáncer de ovario platino-resistente. Los resultados de la fase II fueron muy positivos y hay un hueco en el mercado», relata González, quien añade que el mismo fármaco también podría emplearse en cáncer de pulmón microcítico, que supone en torno al 15-20 por ciento del cáncer de pulmón y no cuenta con tratamientos eficaces, a diferencia del de ovario. «Ahí sí que podría posicionarse fuerte. El mayor revulsivo sería éste y el mercado aún no lo ha recogido», dice.
nuevos productos
No obstante, avisa de que habrá que esperar al menos un par de años para que el fármaco llegue al mercado y, eso, suponiendo que los ensayos tengan éxito, pues hay que tener en cuenta que «todos estos desarrollos tienen un riesgo regulatorio».
Precisamente, este riesgo regulatorio es la principal dificultad a la hora de valorar este tipo de compañías, tal y como explica Arístegui: «Haces una valoración conservadora teniendo en cuenta que los medicamentos se aprueben. Pero, si finalmente se aprueban, la empresa vale mucho más y, si no se aprueban, mucho menos». Esto es lo que ha motivado tanta especulación en torno a Zeltia en los últimos años.
De cara al futuro, Arístegui recomienda comprar con un precio objetivo de 5,80 euros, muy por encima de los 4,60 del consenso de los analistas recogido por Bloomberg. Arístegui la valora así porque considera que el nuevo antitumoral tiene «incluso más potencial que Yondelis» y el mercado irá reconociéndolo, aunque no a corto plazo, cuando espera que la acción «se quede un poco parada porque las noticias relevantes ya han sido». En ese sentido, cree que una buena estrategia sería aprovechar la recogida de beneficios «para posicionarse a largo plazo».
En cambio, no todos los analistas son positivos con el valor. Felipe Echevarría, de Sabadell, por ejemplo, cree que todas estas noticias están en precio y descarta entrar en Zeltia, donde -con un precio objetivo de 4,3 euros- «no queda potencial».
Una gota de sangre para predecir la respuesta al tratamiento en el cáncer de próstata .
*.- La rutina habitual es realizar una biopsia para ver ciertas mutaciones, una prueba invasiva, molesta y no exenta de riesgos.
*.- La biopsia líquida permite acercar la medicina a las características de cada paciente
MARÍA VALERIO - 04/11/2015 .
Hace unos años parecía sólo un sueño, un deseo más cercano al laboratorio que a la cama de los pacientes. Sin embargo, poco a poco, la llamada biopsia líquida va ofreciendo resultados tangibles y todo indica que este análisis de sangre para evaluar sobre la marcha la progresión del cáncer será un aliado más de los oncólogos en pocos años.
El último peldaño en la ascensión de esta técnica se acaba de publicar en las páginas de la revista Science Traslational Medicine y demuestra que también podría ayudar a los pacientes con cáncer de próstata.
Mediante un simple análisis de sangre, la biopsia líquida busca fragmentos de ADN de células tumorales que han ido a parar al torrente sanguíneo, desprendidos desde el tumor original. Hasta ahora, se ha demostrado con éxito que puede emplearse en pacientes con cáncer de pulmón y de colon, incluso de mama (aunque de manera más experimental). Con los nuevos resultados obtenidos por científicos británicos e italianos, el cáncer de próstata se suma también a esta lista.
Como explica a EL MUNDO el doctor Gerhardt Attard, del Instituto de Investigación del Cáncer (ICR) de Londres y principal autor del estudio, "ya habíamos publicado los resultados de la biopsia líquida en cáncer de próstata el año pasado, pero ésta es quizás la evaluación más completa y ha demostrado su utilidad clínica".
Concretamente, los científicos evaluaron 274 muestras de sangre procedentes de 97 pacientes con un tumor en la próstata (tratados tanto en el Hospital Royal Marsden de Londres como en el de Trento, en Italia). Sus resultados demostraron que, incluso antes de iniciar el tratamiento, el ADN tumoral presente en su sangre permitía predecir qué pacientes responderían a la terapia hormonal. Y, viceversa, cuáles no lo harían y, por lo tanto, deberían recibir otro tratamiento alternativo más adecuado para su tipo de cáncer.
...
*.- La biopsia líquida permite acercar la medicina a las características de cada paciente
MARÍA VALERIO - 04/11/2015 .
Hace unos años parecía sólo un sueño, un deseo más cercano al laboratorio que a la cama de los pacientes. Sin embargo, poco a poco, la llamada biopsia líquida va ofreciendo resultados tangibles y todo indica que este análisis de sangre para evaluar sobre la marcha la progresión del cáncer será un aliado más de los oncólogos en pocos años.
El último peldaño en la ascensión de esta técnica se acaba de publicar en las páginas de la revista Science Traslational Medicine y demuestra que también podría ayudar a los pacientes con cáncer de próstata.
Mediante un simple análisis de sangre, la biopsia líquida busca fragmentos de ADN de células tumorales que han ido a parar al torrente sanguíneo, desprendidos desde el tumor original. Hasta ahora, se ha demostrado con éxito que puede emplearse en pacientes con cáncer de pulmón y de colon, incluso de mama (aunque de manera más experimental). Con los nuevos resultados obtenidos por científicos británicos e italianos, el cáncer de próstata se suma también a esta lista.
Como explica a EL MUNDO el doctor Gerhardt Attard, del Instituto de Investigación del Cáncer (ICR) de Londres y principal autor del estudio, "ya habíamos publicado los resultados de la biopsia líquida en cáncer de próstata el año pasado, pero ésta es quizás la evaluación más completa y ha demostrado su utilidad clínica".
Concretamente, los científicos evaluaron 274 muestras de sangre procedentes de 97 pacientes con un tumor en la próstata (tratados tanto en el Hospital Royal Marsden de Londres como en el de Trento, en Italia). Sus resultados demostraron que, incluso antes de iniciar el tratamiento, el ADN tumoral presente en su sangre permitía predecir qué pacientes responderían a la terapia hormonal. Y, viceversa, cuáles no lo harían y, por lo tanto, deberían recibir otro tratamiento alternativo más adecuado para su tipo de cáncer.
...
Un gusano transmite su cáncer a los humanos .
Médicos de Colombia y EE UU alertan hoy de que un parásito puede transmitir el cáncer a personas. El único caso conocido sucedió en Medellín (Colombia), con un paciente cuyo sistema inmune estaba debilitado por el VIH. Los médicos han tardado tres años en convencerse de que las extrañas formaciones celulares que veían en sus pulmones y otros órganos eran tumores causados por células de gusano.
“Nos quedamos muy sorprendidos" al ver "gusanos planos creciendo dentro de una persona que básicamente sufrían cáncer y este se expandió al paciente causándole la enfermedad”, ha explicado Atis Muehlenbachs, patólogo del Centro de Control de Enfermedades de EE UU (CDC). Su equipo describe hoy este salto entre especies del cáncer en la revista especializada New England Journal of Medicine.
El hallazgo despierta la duda de si hay más casos, especialmente en países en desarrollo donde tanto las infecciones con parásitos como la incidencia del sida y otras enfermedades crean el caldo de cultivo perfecto, según explica el CDC en una nota de prensa.
El gusano en cuestión (Hymenolepis nana) es un primo hermano de la tenia. Mide unos tres centímetros y se engancha a las paredes del intestino delgado. Se calcula que hay unas 75 millones de personas infectadas en todo el mundo, la mayoría en países en desarrollo. Generalmente la infección no causa síntomas, pero en casos en los que el sistema inmune está debilitado por otras causas, como la infección con el VIH, la historia puede ser muy diferente.
...
“Nos quedamos muy sorprendidos" al ver "gusanos planos creciendo dentro de una persona que básicamente sufrían cáncer y este se expandió al paciente causándole la enfermedad”, ha explicado Atis Muehlenbachs, patólogo del Centro de Control de Enfermedades de EE UU (CDC). Su equipo describe hoy este salto entre especies del cáncer en la revista especializada New England Journal of Medicine.
El hallazgo despierta la duda de si hay más casos, especialmente en países en desarrollo donde tanto las infecciones con parásitos como la incidencia del sida y otras enfermedades crean el caldo de cultivo perfecto, según explica el CDC en una nota de prensa.
El gusano en cuestión (Hymenolepis nana) es un primo hermano de la tenia. Mide unos tres centímetros y se engancha a las paredes del intestino delgado. Se calcula que hay unas 75 millones de personas infectadas en todo el mundo, la mayoría en países en desarrollo. Generalmente la infección no causa síntomas, pero en casos en los que el sistema inmune está debilitado por otras causas, como la infección con el VIH, la historia puede ser muy diferente.
...
04 noviembre 2015
PharmaMar Trata de Consolidar Una Linea Polar en los 4 euros . Post by Invertiryespecular.com
Publicado el 4 de noviembre de 2015 .
Ya debéis saber de tantas veces que lo decimos que una línea polar es aquel nivel de precio que ejerce de resistencia y luego de soporte por lo tanto marca las consolidaciones y niveles presentes y futuros de los precios. Por lo tanto son niveles que cuando se pierden suponen un deterioro para la serie o activo en cuestión y cuando se confirman una revalorización técnica que la hace merecedora de la confianza del inversor.
Pharma mar ex-Zeltia trata de establecer una en la zona de los 4 euros …
...
Ya debéis saber de tantas veces que lo decimos que una línea polar es aquel nivel de precio que ejerce de resistencia y luego de soporte por lo tanto marca las consolidaciones y niveles presentes y futuros de los precios. Por lo tanto son niveles que cuando se pierden suponen un deterioro para la serie o activo en cuestión y cuando se confirman una revalorización técnica que la hace merecedora de la confianza del inversor.
Pharma mar ex-Zeltia trata de establecer una en la zona de los 4 euros …
...
Crean prueba bucal para detectar predisposición al cáncer de mama .
México, 3 Nov (Notimex).-
Un médico de la Universidad Autónoma de Nayarit (UAN) desarrolló una prueba para detectar una predisposición al cáncer de mama a través de micronúcleos en las células de la mucosa bucal.
La prueba funciona como un biomarcador potencial de riesgo para la detección oportuna de este padecimiento, dijo el jefe del Departamento de Investigación en la Unidad Académica de Medicina de la UAN, Aurelio Flores García, en una entrevista con la Agencia Informativa del Consejo Nacional de Ciencia y Tecnología (Conacyt).
“Se toma una muestra de células exfoliadas de mucosa bucal por medio de un portaobjetos de bordes romos, se realiza un frotis que se fija en etanol. Posteriormente se hace una tinción con naranja de acridina y, finalmente, se hace un conteo de micronúcleos en un microscopio de fluorescencia”, explicó el investigador.
Los micronúcleos son fragmentos de cromosomas o cromosomas completos que al momento de dividirse una célula generan dos células anormales en su material genético, y que de manera ordinaria el cuerpo tiene mecanismos para eliminarlas, detalló Flores García.
Sin embargo, una repetición de estos eventos puede dar lugar a la creación de una célula cancerosa, a partir de la cual se genera cualquier tipo de cáncer, señaló.
...
Un médico de la Universidad Autónoma de Nayarit (UAN) desarrolló una prueba para detectar una predisposición al cáncer de mama a través de micronúcleos en las células de la mucosa bucal.
La prueba funciona como un biomarcador potencial de riesgo para la detección oportuna de este padecimiento, dijo el jefe del Departamento de Investigación en la Unidad Académica de Medicina de la UAN, Aurelio Flores García, en una entrevista con la Agencia Informativa del Consejo Nacional de Ciencia y Tecnología (Conacyt).
“Se toma una muestra de células exfoliadas de mucosa bucal por medio de un portaobjetos de bordes romos, se realiza un frotis que se fija en etanol. Posteriormente se hace una tinción con naranja de acridina y, finalmente, se hace un conteo de micronúcleos en un microscopio de fluorescencia”, explicó el investigador.
Los micronúcleos son fragmentos de cromosomas o cromosomas completos que al momento de dividirse una célula generan dos células anormales en su material genético, y que de manera ordinaria el cuerpo tiene mecanismos para eliminarlas, detalló Flores García.
Sin embargo, una repetición de estos eventos puede dar lugar a la creación de una célula cancerosa, a partir de la cual se genera cualquier tipo de cáncer, señaló.
...
Nivolumab antes y después de la cirugía . Primer ensayo con inmunoterapia en el tumor cerebral más agresivo .
*.- 29 españoles probarán un fármaco aprobado para melanoma .
*.- Se les administrará el fármaco antes y después de la cirugía
MARÍA VALERIO - Madrid // 04/11/2015 .
El glioblastoma multiforme es considerado el tumor cerebral más agresivo y es que, pese a que se logre extirpar con éxito en la cirugía, la mayor parte de los pacientes acaba sufriendo una recaída en poco tiempo. Para tratar de frenar ese curso natura de la enfermedad, 29 pacientes españoles van a iniciar en la Clínica Universidad de Navarra un ensayo clínico con un fármaco que ya se está administrando con éxito en casos de melanoma.
Por primera vez, este ensayo clínico va a tratar este agresivo cáncer cerebral con un fármaco inmunoterápico, que trata de 'emplear' las propias defensas del organismo para que sean ellas las que ataquen a las células tumorales. Nivolumab, que así se llama el medicamento, ya está autorizado para pacientes con cáncer de piel y para ciertos tipos de cáncer de pulmón.
...
*.- Se les administrará el fármaco antes y después de la cirugía
MARÍA VALERIO - Madrid // 04/11/2015 .
El glioblastoma multiforme es considerado el tumor cerebral más agresivo y es que, pese a que se logre extirpar con éxito en la cirugía, la mayor parte de los pacientes acaba sufriendo una recaída en poco tiempo. Para tratar de frenar ese curso natura de la enfermedad, 29 pacientes españoles van a iniciar en la Clínica Universidad de Navarra un ensayo clínico con un fármaco que ya se está administrando con éxito en casos de melanoma.
Por primera vez, este ensayo clínico va a tratar este agresivo cáncer cerebral con un fármaco inmunoterápico, que trata de 'emplear' las propias defensas del organismo para que sean ellas las que ataquen a las células tumorales. Nivolumab, que así se llama el medicamento, ya está autorizado para pacientes con cáncer de piel y para ciertos tipos de cáncer de pulmón.
...
03 noviembre 2015
Descubrimiento Israelí podría revertir el daño del Alzheimer .
Así, una investigación realizada por un equipo de la Universidad de Tel Aviv puede mostrar el camino para proteger las células del daño causado por la enfermedad de Alzheimer, e incluso daños que la enfermedad causa antes del tratamiento.
El método consiste en una proteína similar a una que protege al cerebro de daños, pero que no está presente en los pacientes de Alzheimer. Qué causa la enfermedad de Alzheimer es todavía un misterio, pero las condiciones que conducen a la demencia asociada a la enfermedad son muy claras para los científicos. Acumulaciones de placa en neuronas matan a las células del cerebro en los enfermos de Alzheimer, lo que conduce a la degeneración de la función cognitiva y la pérdida de memoria asociadas con la enfermedad.
Uno de los objetivos más importantes de la investigación de Alzheimer ha sido la de encontrar formas de proteger a las células del cerebro de estas placas seniles y ovillos neurofibrilares. En un estudio publicado en la edición de mayo de la Revista Enfermedad de Alzheimer, la Universidad de Tel Aviv, la profesora Illana Gozes describe cómo NAP, (un fragmento de una proteína esencial para la formación del cerebro), ha mostrado en estudios anteriores que protege el funcionamiento cognitivo. La pérdida de NAP expone las células al daño físico que con el tiempo las destruye, pero la aplicación de proteínas con propiedades de NAP las hace saludables de nuevo. Es sólo una proteína que Gozes y su equipo han descubierto. La investigación, dijo, podría eventualmente conducir al desarrollo de medicamentos para tratar la enfermedad de Alzheimer. “Hace varios años descubrimos que NAP mostró eficacia en la Fase 2 de ensayos clínicos en pacientes con deterioro cognitivo leve, un precursor de la enfermedad de Alzheimer. Ahora, estamos investigando si hay otras secuencias NAP en otras proteínas. “NAP, también conocido como davunetide, es un péptido ácido de ocho aminoácidos que ha mostrado generar neuroprotección en varios ensayos con seres humanos. NAP deriva de la proteína de la actividad neuroprotectora (ADNP), una molécula que es esencial para la formación del cerebro. “NAP opera a través de la estabilización de los microtúbulos (tubos dentro de la célula que mantienen la forma celular).
...
El método consiste en una proteína similar a una que protege al cerebro de daños, pero que no está presente en los pacientes de Alzheimer. Qué causa la enfermedad de Alzheimer es todavía un misterio, pero las condiciones que conducen a la demencia asociada a la enfermedad son muy claras para los científicos. Acumulaciones de placa en neuronas matan a las células del cerebro en los enfermos de Alzheimer, lo que conduce a la degeneración de la función cognitiva y la pérdida de memoria asociadas con la enfermedad.
Uno de los objetivos más importantes de la investigación de Alzheimer ha sido la de encontrar formas de proteger a las células del cerebro de estas placas seniles y ovillos neurofibrilares. En un estudio publicado en la edición de mayo de la Revista Enfermedad de Alzheimer, la Universidad de Tel Aviv, la profesora Illana Gozes describe cómo NAP, (un fragmento de una proteína esencial para la formación del cerebro), ha mostrado en estudios anteriores que protege el funcionamiento cognitivo. La pérdida de NAP expone las células al daño físico que con el tiempo las destruye, pero la aplicación de proteínas con propiedades de NAP las hace saludables de nuevo. Es sólo una proteína que Gozes y su equipo han descubierto. La investigación, dijo, podría eventualmente conducir al desarrollo de medicamentos para tratar la enfermedad de Alzheimer. “Hace varios años descubrimos que NAP mostró eficacia en la Fase 2 de ensayos clínicos en pacientes con deterioro cognitivo leve, un precursor de la enfermedad de Alzheimer. Ahora, estamos investigando si hay otras secuencias NAP en otras proteínas. “NAP, también conocido como davunetide, es un péptido ácido de ocho aminoácidos que ha mostrado generar neuroprotección en varios ensayos con seres humanos. NAP deriva de la proteína de la actividad neuroprotectora (ADNP), una molécula que es esencial para la formación del cerebro. “NAP opera a través de la estabilización de los microtúbulos (tubos dentro de la célula que mantienen la forma celular).
...
02 noviembre 2015
Pharma Mar Asegura su Ebitda con Royalties ( Rondarían los 25 Millones Anuales ) y Además Tiene 39 Millones en Caja que le Permiten Presentarse “Guapa” en el Nasdaq .
Lunes 2 de Noviembre de 2015 // Marcos Celada
*.- Las Aprobaciones de Yondelis en Japón y EEUU le pueden suponer 25 Millones Anuales .
*.- Zeltia se Reinventa en Pharmamar tras asegurar su Ebitda con Royalties .
*.- Tiene 39 Millones en Caja que le permiten Presentarse “Guapa” en el Nasdaq .
Zeltia ya es historia. Ha estrenado noviembre absorbida por su antigua filial farmacéutica, Pharmamar, que es la que ahora cotiza como propietaria de todos los activos y pasivos de Zeltia. A nivel contable este cambio no tiene efecto alguno en las cuentas del grupo. Pero a efectos de imagen, y posibilidades de financiación, sobre todo internacionales, la operación es muy importante. A todo ello se suma la reciente aprobación de su medicamento Yondelis para ciertos tratamientos de cáncer en EEUU y Japón, lo que le garantiza un nivel mínimo de beneficios vía royalties.
El último tropiezo con esta patente le hizo perder los 6 euros por acción hace seis años. ¿Volverá a recuperarlos?
Era su asignatura pendiente y lo ha logrado. Entrar en el mercado estadounidense de los productos anticancerígenos es casi un seguro de vida, por dos cosas: una, que supone el 45% del mercado mundial de este tipo de medicamentos.
Otro, que cuando un fármaco se comienza a administrar en los hospitales estadounidenses las ventas en Europa suelen subir alrededor de un 20% por el efecto de confianza cruzada que supone la doble aprobación por la EMEA (autoridad europea de medicamentos) y su colega de EEUU, la FAD.
Para Pharmamar esto no es ninguna broma. En 2014, según datos del grupo, Yondelis logró unas ventas netas de 76,5 millones de euros en el continente europeo, cifra que se verá incrementada algo este año 2015. Si los cálculos de los analistas se cumplen, para 2016 y los años sucesivos, las ventas de Yondelis en Europa podrían superar ya los 90 millones de euros, con un incremento de entre doce y quince millones anuales. A diferencia de otro tipo de industrias, en la farmacéutica, los costes importantes son los de investigación, con lo que cuando las ventas del fármaco aumentan los costes de fabricación son marginales y el incremento de facturación va casi íntegro al beneficio de explotación.
Esto es importante, pero está sin confirmar. Lo que sí es comprobable ya es el ingreso de sus primeros royalties importantes por la comercialización de Yondelis en los dos mercados más importantes del mundo en productos contra el cáncer: EEUU y Japón. El mercado nipón, que supone un 12% del mundial, abrió la puerta al fármaco de Pharmamar en septiembre. Y eso le va a suponer antes de final de año un ingreso directo de unos nueve millones de euros por royalties directos y a través de la multinacional Johnson & Johnson, cuya división de farmacia Janssen es la encargada de comercializar Yondelis en EEUU.
Margen para el I+D
La apertura del mercado estadounidense tras la aprobación otorgada por la FAD a finales de octubre le supone otro ingreso inmediato de nueve millones de euros y otro recurrente de entre 11 y 19 millones anuales por royalties en los próximos ejercicios, dependiendo del nivel efectivo de prescripciones que se realicen de este medicamento. Los ingresos recurrentes del mercado japonés podrían situarse a su vez en cifras algo más modestas, pero importantes, de entre dos y cuatro millones anuales por el Yondelis.
Todas estas cifras lo que hacen es asegurar un nivel de beneficio bruto de explotación (Ebitda) similar al actual para las próximos anos con niveles de inversión en I+D también similares a los de 2015 que son de los más altos de su historia, ya que tiene en desarrollo y ensayo nuevas aplicaciones del propio Yondelis y de otros fármacos para cánceres tan comunes como el de ovario y el de mama, aparte del sarcoma.
De hecho, por ejemplo, en las cifras a 30 de septiembre último, el grupo consolidado había visto caer su Ebitda de 25,6 a 16,6 millones de euros, debido a un incremento de 8,7 millones en la inversión en I+D que ha pasado de 37 a 45,7 millones en los nueve primeros meses de 2015. Los cobros inmediatos que va a recibir Pharmamar por la aprobación de Yondelis en Japón y EEUU van a sumar 18 millones de euros que harán subir su Ebitda a una cifra seguramente superior a los 25 millones de 2014.
Los nuevos ingresos recurrentes le garantizan un futuro a corto plazo sin sobresaltos financieros a actividad constante, pero el mundo de las empresas farmacéuticas es cualquier cosa menos constante. Su vida depende de nuevos descubrimientos que puedan comercializarse de forma masiva y que compensen el esfuerzo de inversión realizado con anterioridad. En previsión de que tales circunstancias pueden volver a darse en el seno del grupo, el máximo responsable del mismo, José María Fernández Sousa, decidió reorganizar su estructura. Las experiencias de desplomes en Bolsa por falta de capacidad financiera le han hecho aprender y ahora ha decidido dar la vuelta al negocio. Bueno, más que al negocio, a su puesta en escena.
La Fusión
Hasta ahora, Zeltia era un grupo comandado por la matriz del mismo nombre que nació como empresa química tradicional y luego agregó el negocio que era la gran pasión de su presidente, la biofarmacia. De Zeltia son marcas muy famosas, por ejemplo, la gama de insecticidas ZZ y la de pinturas y protectores de madera Xilazel. Zeltia vivió en Bolsa su momento de mayor esplendor entre 1998 y el año 2000, cuando comenzaron a culminar con éxito algunos de sus ensayos sobre fármacos contra el cáncer.
Las cifras no dejan lugar a dudas: la primera cotización de 1998 fue el equivalente a 30 céntimos de euro (entonces se cotizaba en pesetas) y cerró el año 2000 en el entorno de los 12 euros. La subida había sido del 4.000 por ciento. Pero duró poco.
En 2003 llegaron las primeras dudas serias sobre la aceptación de los fármacos por parte de las autoridades sanitarias. Sin el certificado de aprobación no hay ventas y la investigación no puede ser tirada por la borda. Hay que seguir. En julio de aquel año, después de las calabazas dadas por la EMEA a Yondelis, la cotización perdía el listón de los seis euros.
Nunca llegó a recuperarse del todo de aquel golpe. En 2007 alcanzó los ocho euros, pero en 2009 llegó un nuevo varapalo de la FDA, que siguió sin considerar medicamento al Yondelis y obligó a Pharmamar a repetir las pruebas clínicas de fase III. La acción volvió a caer desde los casi seis a los tres euros. Y así hasta ahora, cuando ha comenzado a subir y se ha estabilizado en torno a los cuatro euros en las últimas semanas.
Entre medias de ambos batacazos, y con el fin de poder seguir con las investigaciones, Zeltia tuvo que realizar una ampliación de capital en 2005. Quería arrancar a los inversores cien millones de euros a 6,05 euros por acción. No lo logró del todo. La colocación, dirigida por HSBC, sólo consiguió 65 millones (el 65%) y con eso tuvo que tirar.
Pero ahora, tras la entrada de su medicamento con más historia en los mercados comerciales de Japón y EEUU, Zeltia se ha dejado absorber por su filial Pharmamar en una operación que técnicamente se denomina fusión inversa, porque es la filial la que se come a la matriz.
Como Zeltia tenía el cien por cien de Pharmamar y la consolidaba íntegramente, la fusión no altera ni una coma las cifras consolidadas del grupo. Las acciones de Zeltia se han convertido en las de Pharmamar y a efectos contables o hay ningún cambio más. Pero la nueva empresa tiene entre sus proyectos más inmediatos comenzar a cotizar en el Nasdaq de la Bolsa de Nueva York. Y allí no es lo mismo llegar con una empresa de pinturas e insecticidas que tiene una filial de farmacia, que justo al revés. Ahora la que cotizará será una compañía de biofarmacia que tiene una filial de química de gran consumo. Algo mucho más parecido a lo que hacen las multinacionales farmacéuticas.
Hacia el Nasdaq
Las cifras ya daban cuenta de ese cambio. En las correspondientes a los tres primeros trimestres de 2015, por ejemplo, el Ebitda del negocio de fármacos ya era el triple que el de la química de gran consumo, y ello a pesar de la caída registrada por el beneficio de explotación de farmacia debido a la mayor inversión en I+D.
Ahora, tras el cambio en la estructura y la salida a cotizar en el Nasdaq, Pharmamar tendrá más fácil obtener recursos de los mercados, ya sea mediante la emisión de bonos o, en último caso, mediante ampliaciones de capital, que ahora serán hechas por la matriz para sí misma, y no como antes que Zeltia tenía que pedir dinero para su filial farmacéutica.
Zeltia colocó en julio pasado una emisión de bonos por una cuantía de 17 millones de euros, con un tipo del 4,5% anual y vencimiento a doce años, que le permiten respirar sin tener que acudir a por más financiación bancaria. A 30 de septiembre pasado, su deuda financiera neta era de 59 millones de euros ( 2,2 veces el Ebitda anual) y contaba con una caja disponible de 39 millones de euros.
Todas estas cifras parecen confirmar que la nueva Pharmamar prepara en firme su salida al Nasdaq con garantías. Las cifras de 2015 y los avances en sus investigaciones puede que hagan de palanca para su cotización.
*.- Las Aprobaciones de Yondelis en Japón y EEUU le pueden suponer 25 Millones Anuales .
*.- Zeltia se Reinventa en Pharmamar tras asegurar su Ebitda con Royalties .
*.- Tiene 39 Millones en Caja que le permiten Presentarse “Guapa” en el Nasdaq .
Zeltia ya es historia. Ha estrenado noviembre absorbida por su antigua filial farmacéutica, Pharmamar, que es la que ahora cotiza como propietaria de todos los activos y pasivos de Zeltia. A nivel contable este cambio no tiene efecto alguno en las cuentas del grupo. Pero a efectos de imagen, y posibilidades de financiación, sobre todo internacionales, la operación es muy importante. A todo ello se suma la reciente aprobación de su medicamento Yondelis para ciertos tratamientos de cáncer en EEUU y Japón, lo que le garantiza un nivel mínimo de beneficios vía royalties.
El último tropiezo con esta patente le hizo perder los 6 euros por acción hace seis años. ¿Volverá a recuperarlos?
Era su asignatura pendiente y lo ha logrado. Entrar en el mercado estadounidense de los productos anticancerígenos es casi un seguro de vida, por dos cosas: una, que supone el 45% del mercado mundial de este tipo de medicamentos.
Otro, que cuando un fármaco se comienza a administrar en los hospitales estadounidenses las ventas en Europa suelen subir alrededor de un 20% por el efecto de confianza cruzada que supone la doble aprobación por la EMEA (autoridad europea de medicamentos) y su colega de EEUU, la FAD.
Para Pharmamar esto no es ninguna broma. En 2014, según datos del grupo, Yondelis logró unas ventas netas de 76,5 millones de euros en el continente europeo, cifra que se verá incrementada algo este año 2015. Si los cálculos de los analistas se cumplen, para 2016 y los años sucesivos, las ventas de Yondelis en Europa podrían superar ya los 90 millones de euros, con un incremento de entre doce y quince millones anuales. A diferencia de otro tipo de industrias, en la farmacéutica, los costes importantes son los de investigación, con lo que cuando las ventas del fármaco aumentan los costes de fabricación son marginales y el incremento de facturación va casi íntegro al beneficio de explotación.
Esto es importante, pero está sin confirmar. Lo que sí es comprobable ya es el ingreso de sus primeros royalties importantes por la comercialización de Yondelis en los dos mercados más importantes del mundo en productos contra el cáncer: EEUU y Japón. El mercado nipón, que supone un 12% del mundial, abrió la puerta al fármaco de Pharmamar en septiembre. Y eso le va a suponer antes de final de año un ingreso directo de unos nueve millones de euros por royalties directos y a través de la multinacional Johnson & Johnson, cuya división de farmacia Janssen es la encargada de comercializar Yondelis en EEUU.
Margen para el I+D
La apertura del mercado estadounidense tras la aprobación otorgada por la FAD a finales de octubre le supone otro ingreso inmediato de nueve millones de euros y otro recurrente de entre 11 y 19 millones anuales por royalties en los próximos ejercicios, dependiendo del nivel efectivo de prescripciones que se realicen de este medicamento. Los ingresos recurrentes del mercado japonés podrían situarse a su vez en cifras algo más modestas, pero importantes, de entre dos y cuatro millones anuales por el Yondelis.
Todas estas cifras lo que hacen es asegurar un nivel de beneficio bruto de explotación (Ebitda) similar al actual para las próximos anos con niveles de inversión en I+D también similares a los de 2015 que son de los más altos de su historia, ya que tiene en desarrollo y ensayo nuevas aplicaciones del propio Yondelis y de otros fármacos para cánceres tan comunes como el de ovario y el de mama, aparte del sarcoma.
De hecho, por ejemplo, en las cifras a 30 de septiembre último, el grupo consolidado había visto caer su Ebitda de 25,6 a 16,6 millones de euros, debido a un incremento de 8,7 millones en la inversión en I+D que ha pasado de 37 a 45,7 millones en los nueve primeros meses de 2015. Los cobros inmediatos que va a recibir Pharmamar por la aprobación de Yondelis en Japón y EEUU van a sumar 18 millones de euros que harán subir su Ebitda a una cifra seguramente superior a los 25 millones de 2014.
Los nuevos ingresos recurrentes le garantizan un futuro a corto plazo sin sobresaltos financieros a actividad constante, pero el mundo de las empresas farmacéuticas es cualquier cosa menos constante. Su vida depende de nuevos descubrimientos que puedan comercializarse de forma masiva y que compensen el esfuerzo de inversión realizado con anterioridad. En previsión de que tales circunstancias pueden volver a darse en el seno del grupo, el máximo responsable del mismo, José María Fernández Sousa, decidió reorganizar su estructura. Las experiencias de desplomes en Bolsa por falta de capacidad financiera le han hecho aprender y ahora ha decidido dar la vuelta al negocio. Bueno, más que al negocio, a su puesta en escena.
La Fusión
Hasta ahora, Zeltia era un grupo comandado por la matriz del mismo nombre que nació como empresa química tradicional y luego agregó el negocio que era la gran pasión de su presidente, la biofarmacia. De Zeltia son marcas muy famosas, por ejemplo, la gama de insecticidas ZZ y la de pinturas y protectores de madera Xilazel. Zeltia vivió en Bolsa su momento de mayor esplendor entre 1998 y el año 2000, cuando comenzaron a culminar con éxito algunos de sus ensayos sobre fármacos contra el cáncer.
Las cifras no dejan lugar a dudas: la primera cotización de 1998 fue el equivalente a 30 céntimos de euro (entonces se cotizaba en pesetas) y cerró el año 2000 en el entorno de los 12 euros. La subida había sido del 4.000 por ciento. Pero duró poco.
En 2003 llegaron las primeras dudas serias sobre la aceptación de los fármacos por parte de las autoridades sanitarias. Sin el certificado de aprobación no hay ventas y la investigación no puede ser tirada por la borda. Hay que seguir. En julio de aquel año, después de las calabazas dadas por la EMEA a Yondelis, la cotización perdía el listón de los seis euros.
Nunca llegó a recuperarse del todo de aquel golpe. En 2007 alcanzó los ocho euros, pero en 2009 llegó un nuevo varapalo de la FDA, que siguió sin considerar medicamento al Yondelis y obligó a Pharmamar a repetir las pruebas clínicas de fase III. La acción volvió a caer desde los casi seis a los tres euros. Y así hasta ahora, cuando ha comenzado a subir y se ha estabilizado en torno a los cuatro euros en las últimas semanas.
Entre medias de ambos batacazos, y con el fin de poder seguir con las investigaciones, Zeltia tuvo que realizar una ampliación de capital en 2005. Quería arrancar a los inversores cien millones de euros a 6,05 euros por acción. No lo logró del todo. La colocación, dirigida por HSBC, sólo consiguió 65 millones (el 65%) y con eso tuvo que tirar.
Pero ahora, tras la entrada de su medicamento con más historia en los mercados comerciales de Japón y EEUU, Zeltia se ha dejado absorber por su filial Pharmamar en una operación que técnicamente se denomina fusión inversa, porque es la filial la que se come a la matriz.
Como Zeltia tenía el cien por cien de Pharmamar y la consolidaba íntegramente, la fusión no altera ni una coma las cifras consolidadas del grupo. Las acciones de Zeltia se han convertido en las de Pharmamar y a efectos contables o hay ningún cambio más. Pero la nueva empresa tiene entre sus proyectos más inmediatos comenzar a cotizar en el Nasdaq de la Bolsa de Nueva York. Y allí no es lo mismo llegar con una empresa de pinturas e insecticidas que tiene una filial de farmacia, que justo al revés. Ahora la que cotizará será una compañía de biofarmacia que tiene una filial de química de gran consumo. Algo mucho más parecido a lo que hacen las multinacionales farmacéuticas.
Hacia el Nasdaq
Las cifras ya daban cuenta de ese cambio. En las correspondientes a los tres primeros trimestres de 2015, por ejemplo, el Ebitda del negocio de fármacos ya era el triple que el de la química de gran consumo, y ello a pesar de la caída registrada por el beneficio de explotación de farmacia debido a la mayor inversión en I+D.
Ahora, tras el cambio en la estructura y la salida a cotizar en el Nasdaq, Pharmamar tendrá más fácil obtener recursos de los mercados, ya sea mediante la emisión de bonos o, en último caso, mediante ampliaciones de capital, que ahora serán hechas por la matriz para sí misma, y no como antes que Zeltia tenía que pedir dinero para su filial farmacéutica.
Zeltia colocó en julio pasado una emisión de bonos por una cuantía de 17 millones de euros, con un tipo del 4,5% anual y vencimiento a doce años, que le permiten respirar sin tener que acudir a por más financiación bancaria. A 30 de septiembre pasado, su deuda financiera neta era de 59 millones de euros ( 2,2 veces el Ebitda anual) y contaba con una caja disponible de 39 millones de euros.
Todas estas cifras parecen confirmar que la nueva Pharmamar prepara en firme su salida al Nasdaq con garantías. Las cifras de 2015 y los avances en sus investigaciones puede que hagan de palanca para su cotización.
31 octubre 2015
Pharma Mar Estrena Nueva Website , Nuevos Objetivos y Nuevos Retos ... Que Según Luis Mora Pasan por Salir a Cotizar en el Nasdaq y Comercializar Directamente en EEUU .
"La Estrategia que acompaña a la Fusión inversa es Comercializar Directamente en EE UU" .
Link Entrevista : MARTA rIESGO entrevista a Luis Mora ( Director General de Pharma Mar ) para @ElGlobalNet .
Desde el lunes 2 de noviembre Zeltia pasará a cotizar como PharmaMar. Es el fin de un proceso de fusión inversa que la compañía anunció hace varios meses.
Luis Mora, director general de PharmaMar explica los objetivos y retos de este proceso.
Pregunta. En unas horas Zeltia pasará a cotizar en bolsa como PharmaMar. ¿Cómo ha transcurrido este proceso?
Respuesta. Fue una decisión estratégica de la compañía. Es un proceso básicamente legal y administrativo. El día 30 dejan de cotizar las acciones como Zeltia y el 2 de noviembre ya cotizarán las de PharmaMar, con un canje de uno a uno.
P. ¿Qué objetivos se buscan con esta fusión?
R. Es un paso previo para, en un futuro, salir a cotizar al Nasdaq. El mercado bursátil natural de las empresas biotech es el americano, que es donde hay más de 200 compañías cotizando. Es un mercado donde valoran muy bien no solo lo que tienes en el mercado, sino el desarrollo que va a llegar. La valoración de estos compuestos que están en desarrollo no se hace igual en Europa que en Estados Unidos. Además este proceso viene acompañado por una estrategia, que es la de comercializar nosotros directamente en EE UU.
P. Y este proceso viene acompañado de la aprobación de Yondelis por la FDA, ¿no?
R. Yondelis es el primer producto español aprobado por la FDA. Un mes antes anunciamos la aprobación en Japón. La oncología es el foco estratégico y en cinco años queremos tener tres productos y cinco o seis indicaciones en el mercado.
P. ¿En qué fármacos están trabajando?
R. Con Yondelis la EORTC está haciendo un ensayo para meningioma, y nosotros estamos haciendo otro de mesotelioma. Con Aplidin acabamos el reclutamiento del ensayo pivotal en verano y tendremos los topline en el primer trimestre del año que viene. Otro compuesto clave es el PM1183; hemos empezado el ensayo de registro para un tipo de cáncer de ovario platino resistente. El ensayo pivotal está en marcha y va mejor de lo previsto y en diciembre de este año empezaremos otro ensayo pivotal para cáncer de pulmón de célula pequeña. Además en Fase II estamos en cáncer de mama y en cáncer de endometrio. El último compuesto es el PM60184, del que estamos diseñando la fase II.
P. Dentro del área de oncología se centran también en enfermedades huérfanas ¿Es fácil investigar en este campo?
R. Ha habido un avance importante, pero todavía hay grandes diferencias entre la FDA y la EMA. En indicaciones donde la incidencia es muy baja, mientras que por la FDA puedes hacer un ensayo o registro de un solo brazo con un número de pacientes limitado, la EMA te pide el ensayo randomizado, y eso es inviable. Es uno de los grandes problemas que hay para enfermedades ultra huérfanas. Por otro lado tienes una ventaja, que es una extensión de exclusividad que pasa de 7 a 10 años. En EE UU pasas de 5 a 7 años, pero aquí cuando investigas una enfermedad huérfana el 50 por ciento de la inversión es tax credit y allí también está el premium pricing.
...
Link Entrevista : MARTA rIESGO entrevista a Luis Mora ( Director General de Pharma Mar ) para @ElGlobalNet .
Desde el lunes 2 de noviembre Zeltia pasará a cotizar como PharmaMar. Es el fin de un proceso de fusión inversa que la compañía anunció hace varios meses.
Luis Mora, director general de PharmaMar explica los objetivos y retos de este proceso.
Pregunta. En unas horas Zeltia pasará a cotizar en bolsa como PharmaMar. ¿Cómo ha transcurrido este proceso?
Respuesta. Fue una decisión estratégica de la compañía. Es un proceso básicamente legal y administrativo. El día 30 dejan de cotizar las acciones como Zeltia y el 2 de noviembre ya cotizarán las de PharmaMar, con un canje de uno a uno.
P. ¿Qué objetivos se buscan con esta fusión?
R. Es un paso previo para, en un futuro, salir a cotizar al Nasdaq. El mercado bursátil natural de las empresas biotech es el americano, que es donde hay más de 200 compañías cotizando. Es un mercado donde valoran muy bien no solo lo que tienes en el mercado, sino el desarrollo que va a llegar. La valoración de estos compuestos que están en desarrollo no se hace igual en Europa que en Estados Unidos. Además este proceso viene acompañado por una estrategia, que es la de comercializar nosotros directamente en EE UU.
P. Y este proceso viene acompañado de la aprobación de Yondelis por la FDA, ¿no?
R. Yondelis es el primer producto español aprobado por la FDA. Un mes antes anunciamos la aprobación en Japón. La oncología es el foco estratégico y en cinco años queremos tener tres productos y cinco o seis indicaciones en el mercado.
P. ¿En qué fármacos están trabajando?
R. Con Yondelis la EORTC está haciendo un ensayo para meningioma, y nosotros estamos haciendo otro de mesotelioma. Con Aplidin acabamos el reclutamiento del ensayo pivotal en verano y tendremos los topline en el primer trimestre del año que viene. Otro compuesto clave es el PM1183; hemos empezado el ensayo de registro para un tipo de cáncer de ovario platino resistente. El ensayo pivotal está en marcha y va mejor de lo previsto y en diciembre de este año empezaremos otro ensayo pivotal para cáncer de pulmón de célula pequeña. Además en Fase II estamos en cáncer de mama y en cáncer de endometrio. El último compuesto es el PM60184, del que estamos diseñando la fase II.
P. Dentro del área de oncología se centran también en enfermedades huérfanas ¿Es fácil investigar en este campo?
R. Ha habido un avance importante, pero todavía hay grandes diferencias entre la FDA y la EMA. En indicaciones donde la incidencia es muy baja, mientras que por la FDA puedes hacer un ensayo o registro de un solo brazo con un número de pacientes limitado, la EMA te pide el ensayo randomizado, y eso es inviable. Es uno de los grandes problemas que hay para enfermedades ultra huérfanas. Por otro lado tienes una ventaja, que es una extensión de exclusividad que pasa de 7 a 10 años. En EE UU pasas de 5 a 7 años, pero aquí cuando investigas una enfermedad huérfana el 50 por ciento de la inversión es tax credit y allí también está el premium pricing.
...
30 octubre 2015
¡¡¡ Zeltia Adios ... Hola PharmaMar !!! .
29 Octubre 2015 - 17,35 horas
Termina hoy su Andadura con el Exito más Importante y Esperado ... la Aprobación del Yondelis en Estados Unidos ... asi como unas imnmejorables espectativas que deja en manos de PharmaMar como Cabeza de Grupo ... y con la mirada puesta en Estados Unidos en donde tiene previsto salir a cotizar el proximo año ... un Pais en que por fin conoce y reconoce la labor y las especatativas reales de PharmaMar .
Recientemente se han cumplido 75 años de una organización, una empresa española relacionada con el sector de la salud. Un entorno de investigación eminentemente vanguardista que desde España está exportando productos y servicios innovadores a países de medio mundo. La internacionalización es su línea fundamental de expansión y los procesos de I+D conforman el eje central de su idiosincrasia y razón de ser.
Desde knowi pensamos que ejemplos como este son los que contribuyen a que nuestro país figure hoy en los rankings internacionales en una situación preponderante y deberían verse impulsados y favorecidos desde los gobiernos que hoy tenemos y puedan venir en el futuro. Un país que no apuesta por su futuro, no tiene futuro, y la innovación es la clave de Sol de ese futuro prometedor que todos anhelamos.
La sociedad se fundó el 3 de agosto de 1939 en Vigo. Desde sus comienzos el Grupo Zeltia estuvo ligado a la innovación, siendo su objetivo inicial el de explotar la flora medicinal de nuestro país y los productos opoterápicos, procedentes de glándulas de animales, destacando rápidamente como primera productora nacional de alcaloides del cornezuelo de centeno, así como de extractos hepáticos.
En tres años, 1942, Zeltia cuenta con un importante grupo de científicos encabezados por el profesor Calvet y también con un Comité Científico Asesor del que formaban parte destacados catedráticos de las Facultades de Ciencias, Farmacia y Medicina de la Universidad de Santiago de Compostela. El equipo de síntesis química dirigido por el profesor Calvet sintetizó el dicloro-difenil-tricloroetano (DDT), iniciándose así un nuevo camino dentro de la fabricación de nuestros productos pesticidas e insecticidas.
En 1945 Zeltia funda y adquiere el 23% de la empresa Antibióticos S.A, líder en el campo de la fermentación, exportadora por excelencia y suministradora en el mercado farmacéutico nacional e internacional.
En la década de los cincuenta, Zeltia S.A., renueva su equipo técnico, amplía su gama de productos con algunos de origen extranjero, iniciando así relaciones científicas y comerciales con firmas como las británicas Imperial Chemical Industries (ICI) o Cooper McDougall ¬ Robertson Limited.
El campo de actividades de Zeltia se amplía dando lugar a su estructuración en cuatro divisiones: División Médica, Agroquímicos, Productos insecticidas de uso doméstico y División Veterinaria.
En 1964 Zeltia ya comienza a apostar por la internacionalización, ya que constituye, en asociación con empresas británicas líderes en sus sectores, tres nuevas compañías: Zeltia Agraria (en asociación con ICI-Pharmaceuticals) dedicada a tratar problemas de la agricultura; ICI Farma (en asociación con ICI-Pharmaceuticals), dedicada al desarrollo y fabricación de productos farmacéuticos, y Cooper Zeltia (en asociación con Cooper McDougall & Robertson Ltd.), dedicada a la fabricación de productos insecticidas de uso doméstico e industrial y de productos farmacológicos y biológicos de uso veterinario. Las tres 4 divisiones hasta entonces existentes se integran en estas tres compañías.
El año 1986 será clave para el Grupo Zeltia ya que se funda PharmaMar, pionera en la actividad de desarrollo de fármacos de origen marino en el ámbito mundial. Le sigue la fundación de PharmaGen dedicada al análisis del ADN determinación de paternidades, análisis forense y realización de kits de diagnóstico. En el 2002 se acomete la fusión por absorción de Genómica, S.A. por PharmaGen, S.A. quien tomará el nombre de la primera. En este mismo año se lanza una nueva marca al mercado en español, “Xylazel”, que abarca una gama de productos novedosos, especializaos en el cuidado y protección de la madera.
En el 2003 Zelnova adquiere de la empresa española “Thomil” sus marcas líderes en el mercado e incorpora a su catálogo productos y marcas de limpieza de hogar tan conocidas como Hechicera, Bonacera, Baldosinin, Briflor, Kliner y Duende.
En el 2006 nace Sylentis como spin-off de GENOMICA, convirtiéndose en la empresa más joven del grupo. Su principal objetivo es posicionarse como empresa de referencia dentro del sector de nuevas terapias basadas en la tecnología del ARNi y, en especial, dentro de las enfermedades oculares, inflamatorias y neurodegenerativas.
Uno de los hitos más relevantes para el grupo tuvo lugar en el año 2007, cuando la Comisión Europea concede a PharmaMar la autorización para la comercialización del primer antitumoral de origen marino a nivel mundial y el primer anticancerígeno de origen español. Esta autorización fue concedida para el tratamiento del sarcoma de tejidos blandos en la Unión Europea.
En el 2009 el primer fármaco de origen marino comercializado por PharmaMar recibe una nueva autorización por parte de la Comisión Europea para el tratamiento del cáncer de ovario recurrente platino-sensible.
En el 2012 la internacionalización del Grupo es uno de los ejes centrales del negocio y se inauguran dos oficinas comerciales de PharmaMar en Europa, en concreto en Italia (Milán) y Alemania (Berlín)y en 2015 abre oficina en Londres . Xylazel lanza su línea de productos “Aire Sano” orientados al cuidado de la salud de los usuarios de sus pinturas.
En definitiva, como se puede apreciar en este breve resumen un periplo cargado de riesgo, de ilusión, de iniciativas disruptivas y de una apuesta decidida por un entorno, el de la investigación en el ámbito de la salud que conlleva procesos de desarrollo muy prolongados cargados de incertidumbre, tratando de encontrar soluciones para problemas hoy todavía no resueltos como es el caso del cáncer.
¡¡¡ Adios Zeltia ... Hola PharmaMar !!!
Termina hoy su Andadura con el Exito más Importante y Esperado ... la Aprobación del Yondelis en Estados Unidos ... asi como unas imnmejorables espectativas que deja en manos de PharmaMar como Cabeza de Grupo ... y con la mirada puesta en Estados Unidos en donde tiene previsto salir a cotizar el proximo año ... un Pais en que por fin conoce y reconoce la labor y las especatativas reales de PharmaMar .
Recientemente se han cumplido 75 años de una organización, una empresa española relacionada con el sector de la salud. Un entorno de investigación eminentemente vanguardista que desde España está exportando productos y servicios innovadores a países de medio mundo. La internacionalización es su línea fundamental de expansión y los procesos de I+D conforman el eje central de su idiosincrasia y razón de ser.
Desde knowi pensamos que ejemplos como este son los que contribuyen a que nuestro país figure hoy en los rankings internacionales en una situación preponderante y deberían verse impulsados y favorecidos desde los gobiernos que hoy tenemos y puedan venir en el futuro. Un país que no apuesta por su futuro, no tiene futuro, y la innovación es la clave de Sol de ese futuro prometedor que todos anhelamos.
La sociedad se fundó el 3 de agosto de 1939 en Vigo. Desde sus comienzos el Grupo Zeltia estuvo ligado a la innovación, siendo su objetivo inicial el de explotar la flora medicinal de nuestro país y los productos opoterápicos, procedentes de glándulas de animales, destacando rápidamente como primera productora nacional de alcaloides del cornezuelo de centeno, así como de extractos hepáticos.
En tres años, 1942, Zeltia cuenta con un importante grupo de científicos encabezados por el profesor Calvet y también con un Comité Científico Asesor del que formaban parte destacados catedráticos de las Facultades de Ciencias, Farmacia y Medicina de la Universidad de Santiago de Compostela. El equipo de síntesis química dirigido por el profesor Calvet sintetizó el dicloro-difenil-tricloroetano (DDT), iniciándose así un nuevo camino dentro de la fabricación de nuestros productos pesticidas e insecticidas.
En 1945 Zeltia funda y adquiere el 23% de la empresa Antibióticos S.A, líder en el campo de la fermentación, exportadora por excelencia y suministradora en el mercado farmacéutico nacional e internacional.
En la década de los cincuenta, Zeltia S.A., renueva su equipo técnico, amplía su gama de productos con algunos de origen extranjero, iniciando así relaciones científicas y comerciales con firmas como las británicas Imperial Chemical Industries (ICI) o Cooper McDougall ¬ Robertson Limited.
El campo de actividades de Zeltia se amplía dando lugar a su estructuración en cuatro divisiones: División Médica, Agroquímicos, Productos insecticidas de uso doméstico y División Veterinaria.
En 1964 Zeltia ya comienza a apostar por la internacionalización, ya que constituye, en asociación con empresas británicas líderes en sus sectores, tres nuevas compañías: Zeltia Agraria (en asociación con ICI-Pharmaceuticals) dedicada a tratar problemas de la agricultura; ICI Farma (en asociación con ICI-Pharmaceuticals), dedicada al desarrollo y fabricación de productos farmacéuticos, y Cooper Zeltia (en asociación con Cooper McDougall & Robertson Ltd.), dedicada a la fabricación de productos insecticidas de uso doméstico e industrial y de productos farmacológicos y biológicos de uso veterinario. Las tres 4 divisiones hasta entonces existentes se integran en estas tres compañías.
El año 1986 será clave para el Grupo Zeltia ya que se funda PharmaMar, pionera en la actividad de desarrollo de fármacos de origen marino en el ámbito mundial. Le sigue la fundación de PharmaGen dedicada al análisis del ADN determinación de paternidades, análisis forense y realización de kits de diagnóstico. En el 2002 se acomete la fusión por absorción de Genómica, S.A. por PharmaGen, S.A. quien tomará el nombre de la primera. En este mismo año se lanza una nueva marca al mercado en español, “Xylazel”, que abarca una gama de productos novedosos, especializaos en el cuidado y protección de la madera.
En el 2003 Zelnova adquiere de la empresa española “Thomil” sus marcas líderes en el mercado e incorpora a su catálogo productos y marcas de limpieza de hogar tan conocidas como Hechicera, Bonacera, Baldosinin, Briflor, Kliner y Duende.
En el 2006 nace Sylentis como spin-off de GENOMICA, convirtiéndose en la empresa más joven del grupo. Su principal objetivo es posicionarse como empresa de referencia dentro del sector de nuevas terapias basadas en la tecnología del ARNi y, en especial, dentro de las enfermedades oculares, inflamatorias y neurodegenerativas.
Uno de los hitos más relevantes para el grupo tuvo lugar en el año 2007, cuando la Comisión Europea concede a PharmaMar la autorización para la comercialización del primer antitumoral de origen marino a nivel mundial y el primer anticancerígeno de origen español. Esta autorización fue concedida para el tratamiento del sarcoma de tejidos blandos en la Unión Europea.
En el 2009 el primer fármaco de origen marino comercializado por PharmaMar recibe una nueva autorización por parte de la Comisión Europea para el tratamiento del cáncer de ovario recurrente platino-sensible.
En el 2012 la internacionalización del Grupo es uno de los ejes centrales del negocio y se inauguran dos oficinas comerciales de PharmaMar en Europa, en concreto en Italia (Milán) y Alemania (Berlín)y en 2015 abre oficina en Londres . Xylazel lanza su línea de productos “Aire Sano” orientados al cuidado de la salud de los usuarios de sus pinturas.
En definitiva, como se puede apreciar en este breve resumen un periplo cargado de riesgo, de ilusión, de iniciativas disruptivas y de una apuesta decidida por un entorno, el de la investigación en el ámbito de la salud que conlleva procesos de desarrollo muy prolongados cargados de incertidumbre, tratando de encontrar soluciones para problemas hoy todavía no resueltos como es el caso del cáncer.
¡¡¡ Adios Zeltia ... Hola PharmaMar !!!
Yondelis Slowed the Progression of the Sarcoma by 50 percent Compared with the Comparator Chemotherapy . “Yondelis fills a void where there have been no other therapies specifically for these types of soft tissue sarcoma,” said Dr. Ryan. “It will set the new bar against which future treatments in this setting will be compared.”
OHSU has hand in newly approved cancer therapy .
Dr. Christopher Ryan led OHSU's participation in the Yondelis trial.
A newly FDA-approved treatment for soft tissue sarcoma cancers offers the hope of “progression-free” survival for patients living with this rare or “orphan” disease.
So said Dr. Christopher Ryan, a researcher at the Oregon Health & Science University Knight Cancer Institute who led the institution's participation in a trial for the drug called Yondelis. Some 116 patients were drawn from the Institute, starting in 2006.
Enlarge Dr. Christopher Ryan led OHSU's participation in the Yondelis trial.
“Yondelis fills a void where there have been no other therapies specifically for these types of soft tissue sarcoma,” said Dr. Ryan. “It will set the new bar against which future treatments in this setting will be compared.”
Sarcomas are so rare that the condition is called a “referral disease,” leading patients seeking treatment to national cancer centers like OHSU. “Progression-free survival” describes positive results leading to an enhanced quality and quantity of life for those with inoperable, metastasized or otherwise incurable conditions.
“Yondelis slowed the progression of the sarcoma by 50 percent compared with the comparator chemotherapy, as twice as many patients treated with Yondelis had shrinkage of tumors,” said Ryan, who is a medical oncologist.
Yondelis (or trabectedin), a chemotherapy marketed by Janssen Biotech, Inc., is for the treatment of specific soft tissue sarcomas that cannot be removed by surgery or are metastatic and have spread to organs. The treatment is approved for patients who previously received chemotherapy that contained anthracycline.
“I am inspired by patients who received breakthrough treatments in clinical trials before those treatments were widely available,” said Dr. Ryan. “I’m also just as inspired by patients who, in their struggle with cancer, make decisions to try new treatments, not only to help themselves but to help others.
It’s very gratifying.” .
Dr. Christopher Ryan led OHSU's participation in the Yondelis trial.
A newly FDA-approved treatment for soft tissue sarcoma cancers offers the hope of “progression-free” survival for patients living with this rare or “orphan” disease.
So said Dr. Christopher Ryan, a researcher at the Oregon Health & Science University Knight Cancer Institute who led the institution's participation in a trial for the drug called Yondelis. Some 116 patients were drawn from the Institute, starting in 2006.
Enlarge Dr. Christopher Ryan led OHSU's participation in the Yondelis trial.
“Yondelis fills a void where there have been no other therapies specifically for these types of soft tissue sarcoma,” said Dr. Ryan. “It will set the new bar against which future treatments in this setting will be compared.”
Sarcomas are so rare that the condition is called a “referral disease,” leading patients seeking treatment to national cancer centers like OHSU. “Progression-free survival” describes positive results leading to an enhanced quality and quantity of life for those with inoperable, metastasized or otherwise incurable conditions.
“Yondelis slowed the progression of the sarcoma by 50 percent compared with the comparator chemotherapy, as twice as many patients treated with Yondelis had shrinkage of tumors,” said Ryan, who is a medical oncologist.
Yondelis (or trabectedin), a chemotherapy marketed by Janssen Biotech, Inc., is for the treatment of specific soft tissue sarcomas that cannot be removed by surgery or are metastatic and have spread to organs. The treatment is approved for patients who previously received chemotherapy that contained anthracycline.
“I am inspired by patients who received breakthrough treatments in clinical trials before those treatments were widely available,” said Dr. Ryan. “I’m also just as inspired by patients who, in their struggle with cancer, make decisions to try new treatments, not only to help themselves but to help others.
It’s very gratifying.” .
Descubren un nuevo gen del Cáncer de Tiroides .
Europa Press - 30/10/2015 .
Investigadores de la Clínica Cleveland, en Estados Unidos, han descubierto un nuevo gen asociado con el síndrome de Cowden, una enfermedad hereditaria que lleva a altos riesgos de cáncer de tiroides, mama y otros tipos de cáncer, y un subconjunto de cánceres no heredados de la tiroides, como se revela este jueves en la versión online de American Journal of Human Genetics.
El cáncer de tiroides, el cáncer más común de las glándulas endocrinas, es el cáncer de más rápido aumento en las mujeres y el segundo que más crece en los hombres en Estados Unidos. El nuevo gen, SEC23B, descubierto por Charis Eng, presidente fundador del Instituto de Medicina Genómica del Instituto de Investigación Lerner de la Clínica Cleveland y director del Centro de Genética Personalizada, codifica una proteína implicada en el transporte de todas las proteínas dentro de las células.
...
Investigadores de la Clínica Cleveland, en Estados Unidos, han descubierto un nuevo gen asociado con el síndrome de Cowden, una enfermedad hereditaria que lleva a altos riesgos de cáncer de tiroides, mama y otros tipos de cáncer, y un subconjunto de cánceres no heredados de la tiroides, como se revela este jueves en la versión online de American Journal of Human Genetics.
El cáncer de tiroides, el cáncer más común de las glándulas endocrinas, es el cáncer de más rápido aumento en las mujeres y el segundo que más crece en los hombres en Estados Unidos. El nuevo gen, SEC23B, descubierto por Charis Eng, presidente fundador del Instituto de Medicina Genómica del Instituto de Investigación Lerner de la Clínica Cleveland y director del Centro de Genética Personalizada, codifica una proteína implicada en el transporte de todas las proteínas dentro de las células.
...
Los 118 agentes que con seguridad provocan cáncer y entre los que no está la carne roja .
Tras el anuncio de la Organización Mundial de la Salud en el que alertaba que las carnes rojas y las carnes procesadas eran un factor de cáncer, la Agencia Internacional para la Investigación del Cáncer de la OMS (IARC) ha publicado un listado completo de todos los compuestos, agentes y factores que, con seguridad, causan cáncer a los humanos.
Además la IARC ha publicado una lista paralela con aquellos agentes que "probablemente" o "posiblemente" puedan producir cáncer, entre los que se encuentran las carnes procesadas.
La IARC subdivide el primer listado entre circunstancias generales de exposición, agentes y mezclas. En la primera categoría se engloban: consumo habitual de tabaco, tabaquismo pasivo, exposición a lámparas y camas solares, arsénico en el agua potable, y diferentes ocupaciones profesionales (reparación y fabricación de calzado, fabricación de muebles, pintor, deshollinador, herrero, etc...).
En la segunda categoría, el de las mezclas carcinógenas, destacan las bebidas alcohólicas, las carnes procesadas ,las emisiones domésticas de carbón, el humo del diésel, los medicamentos con fenacetina o nuez de areca.
La última categoría, los agentes, se completa con una serie de sustancias químicas: algunos anticonceptivos hormonales, la contaminación aérea, la radiación solar y ultravioleta o la radiación ionizante (rayos gamma o rayos X).
Hay que destacar, que todos los elementos potencialmente cancerígenos, dependen de su grado de riesgo y del tiempo y lugar de exposición. El listado completo de los agentes cancerígenos se puede consultar en la página web de la IARC.
Además la IARC ha publicado una lista paralela con aquellos agentes que "probablemente" o "posiblemente" puedan producir cáncer, entre los que se encuentran las carnes procesadas.
La IARC subdivide el primer listado entre circunstancias generales de exposición, agentes y mezclas. En la primera categoría se engloban: consumo habitual de tabaco, tabaquismo pasivo, exposición a lámparas y camas solares, arsénico en el agua potable, y diferentes ocupaciones profesionales (reparación y fabricación de calzado, fabricación de muebles, pintor, deshollinador, herrero, etc...).
En la segunda categoría, el de las mezclas carcinógenas, destacan las bebidas alcohólicas, las carnes procesadas ,las emisiones domésticas de carbón, el humo del diésel, los medicamentos con fenacetina o nuez de areca.
La última categoría, los agentes, se completa con una serie de sustancias químicas: algunos anticonceptivos hormonales, la contaminación aérea, la radiación solar y ultravioleta o la radiación ionizante (rayos gamma o rayos X).
Hay que destacar, que todos los elementos potencialmente cancerígenos, dependen de su grado de riesgo y del tiempo y lugar de exposición. El listado completo de los agentes cancerígenos se puede consultar en la página web de la IARC.
29 octubre 2015
Sandra Ortega Mera, una de las hijas del fundador de Inditex, Amancio Ortega, tendrá una participación indirecta del 5% de PharmaMar. CNMV - 19:38. . ZELTIA, S.A. Transformaciones, fusiones, escisiones y disoluciones. .
Fusión por absorción de Zeltia, S.A. por Pharma Mar, S.A.: Documento equivalente al folleto informativo (artículo 26.1.d) del Real Decreto 1310/2005, de 4 de noviembre)
MADRID, 29 (EUROPA PRESS).
Sandra Ortega Mera, una de las hijas del fundador de Inditex, Amancio Ortega, tendrá una participación indirecta del 5% de PharmaMar a través de Rosp Corunna, propietaria del 100% de Rosp Corunna Participaciones Empresariales, de acuerdo con el folleto informativo remitido por Zeltia a la Comisión Nacional del Mercado de Valores (CNMV).
Por su parte, el presidente de Zeltia, José María Fernández Sousa-Faro, dispondrá de una participación del 11,082% una vez que concluya la fusión de la compañía con su filial y ostentará el mismo cargo en la empresa resultante, que llevará el nombre de PharmaMar.
En concreto, Fernández Sousa-Faro contará con una participación directa del 6,422% del capital social de la compañía y con una indirecta del 4,66%, que ostentará a través de su cónyuge, Montserrat Andrade Detrell.
...
http://www.cnmv.es/portal/HR/verDoc.axd?t={148ce6b6-2d4b-43d3-870e-01fefeee299c}
MADRID, 29 (EUROPA PRESS).
Sandra Ortega Mera, una de las hijas del fundador de Inditex, Amancio Ortega, tendrá una participación indirecta del 5% de PharmaMar a través de Rosp Corunna, propietaria del 100% de Rosp Corunna Participaciones Empresariales, de acuerdo con el folleto informativo remitido por Zeltia a la Comisión Nacional del Mercado de Valores (CNMV).
Por su parte, el presidente de Zeltia, José María Fernández Sousa-Faro, dispondrá de una participación del 11,082% una vez que concluya la fusión de la compañía con su filial y ostentará el mismo cargo en la empresa resultante, que llevará el nombre de PharmaMar.
En concreto, Fernández Sousa-Faro contará con una participación directa del 6,422% del capital social de la compañía y con una indirecta del 4,66%, que ostentará a través de su cónyuge, Montserrat Andrade Detrell.
...
http://www.cnmv.es/portal/HR/verDoc.axd?t={148ce6b6-2d4b-43d3-870e-01fefeee299c}
PharmaMar . Sus Acciones Empezarán a Cotizar en el Ibex Medium Cap el Próximo 2 de Noviembre según ha informado el Comité Asesor Técnico del Ibex.
MADRID, 28 Oct. (EUROPA PRESS) -
Las acciones de PharmaMar empezarán a cotizar en el Ibex Medium Cap el próximo 2 de noviembre, una vez concluido el proceso de fusión inversa con su matriz Zeltia, que será excluida de este índice, según ha informado el comité asesor técnico del Ibex.
El número de acciones a efecto del cálculo de los índices en PharmaMar será de algo más de 222,2 millones de títulos, con un coeficiente flotante del 100%.
Este ajuste de exclusión e inclusión de los valores en el índice se realizará al cierre de la sesión anterior a la fecha efectiva de la fusión, prevista para el 2 de noviembre.
La realización del ajuste está condicionada a la admisión a cotización del valor PharmaMar en el sistema de interconexión bursátil en la fecha prevista.
Esta operación de fusión inversa, en la que Zeltia se convierte en la sociedad absorbida, tiene como finalidad aglutinar en una sola sociedad las capacidades de gestión del grupo en las fases de investigación, desarrollo, fabricación, comercialización y distribución de sus productos.
El objetivo fundamental de la fusión es hacer cotizar de forma directa el principal negocio del grupo, la oncología, y aportar flexibilidad a la sociedad resultante para llevar a cabo nuevas operaciones corporativas, como la solicitud de cotización en el mercado de capitales americano.
Las acciones de PharmaMar empezarán a cotizar en el Ibex Medium Cap el próximo 2 de noviembre, una vez concluido el proceso de fusión inversa con su matriz Zeltia, que será excluida de este índice, según ha informado el comité asesor técnico del Ibex.
El número de acciones a efecto del cálculo de los índices en PharmaMar será de algo más de 222,2 millones de títulos, con un coeficiente flotante del 100%.
Este ajuste de exclusión e inclusión de los valores en el índice se realizará al cierre de la sesión anterior a la fecha efectiva de la fusión, prevista para el 2 de noviembre.
La realización del ajuste está condicionada a la admisión a cotización del valor PharmaMar en el sistema de interconexión bursátil en la fecha prevista.
Esta operación de fusión inversa, en la que Zeltia se convierte en la sociedad absorbida, tiene como finalidad aglutinar en una sola sociedad las capacidades de gestión del grupo en las fases de investigación, desarrollo, fabricación, comercialización y distribución de sus productos.
El objetivo fundamental de la fusión es hacer cotizar de forma directa el principal negocio del grupo, la oncología, y aportar flexibilidad a la sociedad resultante para llevar a cabo nuevas operaciones corporativas, como la solicitud de cotización en el mercado de capitales americano.
Nadia Badri ( VicePresidenta de Asuntos Médicos de Pharma Mar ) Entrevista . “Blue Technology. Un Modelo de Desarrollo e Innovación para Identificar Nuevos Medicamentos y Dianas Terapéuticas Procedentes del Mar” .
Nadia Badri es licenciada en Medicina por al Universidad de Argel. Comenzó su carrera como responsable de la unidad de quimioterapia del centro Pierre et Marie Curie en Argel y posteriormente continuó su trayectoria profesional en la industria farmacéutica ejerciendo diferentes posiciones de relevancia. Ha sido Directora de Asuntos Médicos de Oncología en AstraZeneca (Bélgica), Responsable de área del equipo de Hematología y Oncología en Janssen Cilag Europa, Oriente Medio y África; Directora Médica Internacional de Oncología en Aventis Pharma International (Francia) y responsable de Asuntos Médicos Globales de Oncología en Aventis (antiguamente Rhone Poulenc-Rorer) entre otros cargos.
En esta entrevista Nadia Badri aborda la importancia de la colaboración entre la industria farmacéutica y las Administraciones para poder impulsar la innovación y sostenibilidad del SNS. Destaca en este sentido los Acuerdos de Riesgo Compartido como una herramienta que facilite el acceso de los tratamientos a los pacientes.
El Modelo de innovación de PharmaMar se basa en la fuente de la que extraen ideas y soluciones, el mar. Este concepto de “Blue Biotechnology” se fundamenta en identificar moléculas sintetizadas por microorganismos marinos, siendo esta vía una clara oportunidad para abordar nuevas terapias para el cáncer. Una vez identificada la posible droga, ésta se sintetiza de forma química en el laboratorio para preservar y conservar la vida marina.
Los principales retos para PharmaMar son anticiparse a las tendencias del mercado oncológico, y adelantarse a los competidores desarrollando estrategias que mejoren el acceso de los tratamientos a los pacientes así como la optimización de costes.
“The relationship between payers and the pharmaceutical industry is changing. Both parties know they need to reach agreements to support
both innovation and sustainability. In Spain, they are already moving forward in this direction, as exemplified by the Risk Sharing Agreements” .
Why PharmaMar has an innovate Health Model of business and why is it so different to other Pharma?
PharmaMar has become a fully integrated company from R&D to the market, and this has been possible, in part, because of our business model. One of our differentiating characteristics is the root of our research and our products, the sea. Another feature is that even though we are a biotech, we
are a profitable company. This has been the result of successfully forming a sales force all over Europe that commercializes our first drug approved in the EU, YONDELIS®, and establishing important partnerships worldwide. We also have a robust pipeline of investigational drugs that are showing
remarkable clinical results in different tumor types that are currently under investigation.
An efficient and smooth-running organization that aims to optimize every process has made this possible.
“We are leaders in the development of anticancer drugs of marine origin, because our drug discovery process starts the moment our marine scientists
identify the new species that will allow us to identify novel molecules”
“It will be important for us to anticipate future trends in the oncology market and better understand the approaches of our competitors to be up-to-speed on developing strategies to improve patient access and optimize costs”
As a medium-size biopharmaceutical company, we have the flexibility to establish well-developed strategies without delay to meet the demands of a competitive market. In contrast to big pharma, we can exploit this capacity to adapt to unexpected changes and tackle challenges that suddenly arise, leveraging the streamlined communication between departments. This sense of teamwork allows the Company to cope with various challenges in due course and to implement the same strategy across different areas.
...
En esta entrevista Nadia Badri aborda la importancia de la colaboración entre la industria farmacéutica y las Administraciones para poder impulsar la innovación y sostenibilidad del SNS. Destaca en este sentido los Acuerdos de Riesgo Compartido como una herramienta que facilite el acceso de los tratamientos a los pacientes.
El Modelo de innovación de PharmaMar se basa en la fuente de la que extraen ideas y soluciones, el mar. Este concepto de “Blue Biotechnology” se fundamenta en identificar moléculas sintetizadas por microorganismos marinos, siendo esta vía una clara oportunidad para abordar nuevas terapias para el cáncer. Una vez identificada la posible droga, ésta se sintetiza de forma química en el laboratorio para preservar y conservar la vida marina.
Los principales retos para PharmaMar son anticiparse a las tendencias del mercado oncológico, y adelantarse a los competidores desarrollando estrategias que mejoren el acceso de los tratamientos a los pacientes así como la optimización de costes.
“The relationship between payers and the pharmaceutical industry is changing. Both parties know they need to reach agreements to support
both innovation and sustainability. In Spain, they are already moving forward in this direction, as exemplified by the Risk Sharing Agreements” .
Why PharmaMar has an innovate Health Model of business and why is it so different to other Pharma?
PharmaMar has become a fully integrated company from R&D to the market, and this has been possible, in part, because of our business model. One of our differentiating characteristics is the root of our research and our products, the sea. Another feature is that even though we are a biotech, we
are a profitable company. This has been the result of successfully forming a sales force all over Europe that commercializes our first drug approved in the EU, YONDELIS®, and establishing important partnerships worldwide. We also have a robust pipeline of investigational drugs that are showing
remarkable clinical results in different tumor types that are currently under investigation.
An efficient and smooth-running organization that aims to optimize every process has made this possible.
“We are leaders in the development of anticancer drugs of marine origin, because our drug discovery process starts the moment our marine scientists
identify the new species that will allow us to identify novel molecules”
“It will be important for us to anticipate future trends in the oncology market and better understand the approaches of our competitors to be up-to-speed on developing strategies to improve patient access and optimize costs”
As a medium-size biopharmaceutical company, we have the flexibility to establish well-developed strategies without delay to meet the demands of a competitive market. In contrast to big pharma, we can exploit this capacity to adapt to unexpected changes and tackle challenges that suddenly arise, leveraging the streamlined communication between departments. This sense of teamwork allows the Company to cope with various challenges in due course and to implement the same strategy across different areas.
...
Pfizer y Allergan Negocian crear la mayor empresa Farmacéutica del Mundo .
POR M.L. Verbo // 29/10/2015 .
La farmacéutica Pfizer y el fabricante de botox Allergan están considerando una fusión que podría dar lugar a la mayor farmacéutica del mundo, valorada en 300.000 millones de dólares (unos 272.000 millones de euros).
Ian Read, el consejero delegado de Pfizer, habría contactado recientemente a su compatriota en Allergan, Brent Sauders, para proponerle la fusión de ambas compañías, según fuentes cercanas a la operación consultadas por 'The Wall Street Journal'. No obstante, estas conversaciones estarían en una etapa muy preliminar.
...
La farmacéutica Pfizer y el fabricante de botox Allergan están considerando una fusión que podría dar lugar a la mayor farmacéutica del mundo, valorada en 300.000 millones de dólares (unos 272.000 millones de euros).
Ian Read, el consejero delegado de Pfizer, habría contactado recientemente a su compatriota en Allergan, Brent Sauders, para proponerle la fusión de ambas compañías, según fuentes cercanas a la operación consultadas por 'The Wall Street Journal'. No obstante, estas conversaciones estarían en una etapa muy preliminar.
...
Los oncólogos denuncian diferencias en el acceso a tratamientos según las Comunidades Autonomas . Post by Celtia .
LAURA TARDÓN - 28/10/2015 .
España Autoriza un Farmaco ... que no llegara a todas las Mujeres .
No se cumple el principio de equidad en el acceso a fármacos en los distintos centros de oncología de las 17 Comunidades Autónomas. Así lo confirma un estudio que acaba de presentar la Sociedad Española de Oncología Médica (SEOM) durante el XV congreso que está celebrando estos días en Madrid.
Una vez que un medicamento se aprueba por las agencias oficiales (EMA y AEMPS), comienza un procedimiento estándar hasta que finalmente llega al hospital. Antes de la primera prescripción debe fijarse el precio de reembolso. Por desgracia, no existe inmediatez entre estos dos pasos. Pero la variabilidad en este tiempo de espera dependiendo las autonomías e incluso de los propios centros hospitalarios es notable.
Según los datos del estudio de la SEOM, con Ipilimubab (tratamiento para el melanoma avanzado en adultos), la media de meses que transcurren hasta el acceso final oscila entre los ocho en Andalucía hasta los 27 en Asturias. Con Nab-Paclitaxel (para el cáncer de mama metastásico), entre los 17 meses en Aragón y los 58 meses en Castilla y León. Un tercer ejemplo es el Denosumab (para la prevención de eventos relacionados con el esqueleto en adultos con metástasis óseas de tumores sólidos), que tarda entre tres meses en Cataluña o la Comunidad Valenciana y los 24 meses en Andalucía.
...
España Autoriza un Farmaco ... que no llegara a todas las Mujeres .
No se cumple el principio de equidad en el acceso a fármacos en los distintos centros de oncología de las 17 Comunidades Autónomas. Así lo confirma un estudio que acaba de presentar la Sociedad Española de Oncología Médica (SEOM) durante el XV congreso que está celebrando estos días en Madrid.
Una vez que un medicamento se aprueba por las agencias oficiales (EMA y AEMPS), comienza un procedimiento estándar hasta que finalmente llega al hospital. Antes de la primera prescripción debe fijarse el precio de reembolso. Por desgracia, no existe inmediatez entre estos dos pasos. Pero la variabilidad en este tiempo de espera dependiendo las autonomías e incluso de los propios centros hospitalarios es notable.
Según los datos del estudio de la SEOM, con Ipilimubab (tratamiento para el melanoma avanzado en adultos), la media de meses que transcurren hasta el acceso final oscila entre los ocho en Andalucía hasta los 27 en Asturias. Con Nab-Paclitaxel (para el cáncer de mama metastásico), entre los 17 meses en Aragón y los 58 meses en Castilla y León. Un tercer ejemplo es el Denosumab (para la prevención de eventos relacionados con el esqueleto en adultos con metástasis óseas de tumores sólidos), que tarda entre tres meses en Cataluña o la Comunidad Valenciana y los 24 meses en Andalucía.
...
¿Cómo saber en qué órgano hará Metástasis el cáncer? . Hallan las primeras etiquetas Moleculares que lo Advierten . Post by Celtia .
MADRID, 28 Oct. (EUROPA PRESS) -
Científicos del Centro Nacional de Investigaciones Oncológicas (CNIO) han participado en un estudio internacional en el que se han detectado las primeras 'etiquetas' moleculares del cáncer que indican en qué órgano puede reproducirse y producir una metástasis.
En concreto, según los resultados del trabajo que publica la revista 'Nature', han descubierto que los tumores primarios envían sondas mensajeras capaces de transformar el ambiente en los órganos metastásicos, de forma que se vuelva acogedor para las células tumorales. Además, llevan distintas 'etiquetas' moleculares que, a modo de código postal, les permiten anidar en órganos específicos.
...
Científicos del Centro Nacional de Investigaciones Oncológicas (CNIO) han participado en un estudio internacional en el que se han detectado las primeras 'etiquetas' moleculares del cáncer que indican en qué órgano puede reproducirse y producir una metástasis.
En concreto, según los resultados del trabajo que publica la revista 'Nature', han descubierto que los tumores primarios envían sondas mensajeras capaces de transformar el ambiente en los órganos metastásicos, de forma que se vuelva acogedor para las células tumorales. Además, llevan distintas 'etiquetas' moleculares que, a modo de código postal, les permiten anidar en órganos específicos.
...
28 octubre 2015
PM01183 . Datos Presentados en el Congreso ESGO recien celebrado en NICE del 24 al 27 Octubre 2015 . PM01183 es " 150 Veces mas Potente " que Topotecan ( GSK ) en Pacientes Cancer de Ovario Resistentes - Refractario a Platino .
LURBINECTEDIN (PM01183) EFFICACY IN PLATINUM-RESISTANT/REFRACTORY OVARIAN CANCER (PRROC) PATIENTS CORRELATES WITH DRUG EXPOSURE USING PHARMACOKINETIC/PHARMACODYNAMIC (PK/PD) MODELLING .
Background:
PM01183 showed improved efficacy over topotecan in 81 PRROC patients in a randomized phase II trial [Poveda et al. 50th ASCO Annual Meeting 2014 .
Myelosuppression was manageable although dose-limiting.
Neutropenia was correlated with PM01183 area under the curve (AUC) as seen in prior Phase I studies.
Methods:
PRROC consenting patients with + 3 prior chemotherapy lines, adequate organ function and ECOG=0-2 were treated until progression or unacceptable toxicity with either PM01183 at 7 mg every three weeks (q3w) or topotecan on days (D)1-5 q3w or on D1, 8, 15 every four weeks in an IRB/IEC approved clinical trial. Primary endpoint was response rate (RR); secondary endpoints included progression-free-survival (PFS), overall-survival (OS), safety and PK/PD correlations. PK/PD modelling was used to link PM01183 plasma concentrations with changes over time of CA-125/tumor size and severity of neutropenia. An Emax-sigmoid model fits to determine the potency of each drug.
Results :
Calculated potency modelled as half maximal effective concentration (EC50) was 0.03/4.57 µg/L for PM01183/topotecan, respectively. The typical PM01183 PK-profile was well above this efficacy threshold during all the cycle. The model predicts that PM01183 given at 3.2 mg/m² q3w will still result in active plasma concentrations during all the cycle, while grade 4 neutropenia would be reduced by =20%.
Conclusions:
PM01183 is an Active Drug, Approximately 150 Times more Potent than Topotecan, in PRROC Patients. PK/PD models provide a suitable method to optimize the PM01183 benefit/risk ratio. A randomized phase III study in PRROC is underway to confirm these promising results.
****************************************************************************
Nombre Genérico: Topotecán .
Nombre Comercial: Hycamptin® .
Farmaceutica : GlaxoSmithKline ( GSK ) .
El Topotecán es un fármaco de quimioterapia anticanceroso ("antineoplásico" o "citotóxico"). Este medicamento se clasifica como un "inhibidor de la topoisomerasa 1".
Para qué se utiliza este fármaco:
Este medicamento se utiliza para tratar el cáncer de ovarios cuando ya han fallado otros tratamientos .
Background:
PM01183 showed improved efficacy over topotecan in 81 PRROC patients in a randomized phase II trial [Poveda et al. 50th ASCO Annual Meeting 2014 .
Myelosuppression was manageable although dose-limiting.
Neutropenia was correlated with PM01183 area under the curve (AUC) as seen in prior Phase I studies.
Methods:
PRROC consenting patients with + 3 prior chemotherapy lines, adequate organ function and ECOG=0-2 were treated until progression or unacceptable toxicity with either PM01183 at 7 mg every three weeks (q3w) or topotecan on days (D)1-5 q3w or on D1, 8, 15 every four weeks in an IRB/IEC approved clinical trial. Primary endpoint was response rate (RR); secondary endpoints included progression-free-survival (PFS), overall-survival (OS), safety and PK/PD correlations. PK/PD modelling was used to link PM01183 plasma concentrations with changes over time of CA-125/tumor size and severity of neutropenia. An Emax-sigmoid model fits to determine the potency of each drug.
Results :
Calculated potency modelled as half maximal effective concentration (EC50) was 0.03/4.57 µg/L for PM01183/topotecan, respectively. The typical PM01183 PK-profile was well above this efficacy threshold during all the cycle. The model predicts that PM01183 given at 3.2 mg/m² q3w will still result in active plasma concentrations during all the cycle, while grade 4 neutropenia would be reduced by =20%.
Conclusions:
PM01183 is an Active Drug, Approximately 150 Times more Potent than Topotecan, in PRROC Patients. PK/PD models provide a suitable method to optimize the PM01183 benefit/risk ratio. A randomized phase III study in PRROC is underway to confirm these promising results.
****************************************************************************
Nombre Genérico: Topotecán .
Nombre Comercial: Hycamptin® .
Farmaceutica : GlaxoSmithKline ( GSK ) .
El Topotecán es un fármaco de quimioterapia anticanceroso ("antineoplásico" o "citotóxico"). Este medicamento se clasifica como un "inhibidor de la topoisomerasa 1".
Para qué se utiliza este fármaco:
Este medicamento se utiliza para tratar el cáncer de ovarios cuando ya han fallado otros tratamientos .
27 octubre 2015
Yondelis Prostata . Results Showed that Trabectedin inhibits Cellular Proliferation and Accelerates Apoptotic Events in Prostate CSCs; and may be a Potential Effective Therapeutic Agent Against Prostate Cancer .
Enhanced G2/M Arrest, Caspase Related Apoptosis and Reduced E-Cadherin Dependent Intercellular Adhesion by Trabectedin in Prostate Cancer Stem Cells.
Acikgoz E1, Guven U2, Duzagac F2, Uslu R3, Kara M4, Soner BC5, Oktem G1.
Abstract :
Trabectedin (Yondelis, ET-743) is a marine-derived tetrahydroisoquinoline alkaloid. It is originally derived from the Caribbean marine tunicate Ecteinascidia turbinata and currently produced synthetically. Trabectedin is active against a variety of tumor cell lines growing in culture.
The present study focused on the effect of trabectedin in cell proliferation, cell cycle progression, apoptosis and spheroid formation in prostate cancer stem cells (CSCs). Cluster of differentiation (CD) 133+high/CD44+high prostate CSCs were isolated from the DU145 and PC-3 human prostate cancer cell line through flow cytometry.
We studied the growth-inhibitory effects of trabectedin and its molecular mechanisms on human prostate CSCs and non-CSCs. DU-145 and PC-3 CSCs were treated with 0.1, 1, 10 and 100 nM trabectedin for 24, 48 and 72 h and the growth inhibition rates were examined using the sphere-forming assay. Annexin-V assay and immunofluorescence analyses were performed for the detection of the cell death. Concentration-dependent effects of trabectedin on the cell cycle were also evaluated.
The cells were exposed to the different doses of trabectedin for 24, 48 and 72 h to evaluate the effect of trabectedin on the number and diameter of spheroids. According to the results, trabectedin induced cytotoxicity and apoptosis at the IC50 dose, resulting in a significant increase expression of caspase-3, caspase-8, caspase-9, p53 and decrease expression of bcl-2 in dose-dependent manner.
Cell cycle analyses revealed that trabectedin induces dose-dependent G2/M-phase cell cycle arrest, particularly at high-dose treatments. Three-dimensional culture studies showed that trabectedin reduced the number and diameter of spheroids of DU145 and PC3 CSCs.
Furthermore, we have found that trabectedin disrupted cell-cell interactions via E-cadherin in prostasphere of DU-145 and PC-3 CSCs.
Our results showed that trabectedin inhibits cellular proliferation and accelerates apoptotic events in prostate CSCs; and may be a potential effective therapeutic agent against prostate cancer.
Acikgoz E1, Guven U2, Duzagac F2, Uslu R3, Kara M4, Soner BC5, Oktem G1.
Abstract :
Trabectedin (Yondelis, ET-743) is a marine-derived tetrahydroisoquinoline alkaloid. It is originally derived from the Caribbean marine tunicate Ecteinascidia turbinata and currently produced synthetically. Trabectedin is active against a variety of tumor cell lines growing in culture.
The present study focused on the effect of trabectedin in cell proliferation, cell cycle progression, apoptosis and spheroid formation in prostate cancer stem cells (CSCs). Cluster of differentiation (CD) 133+high/CD44+high prostate CSCs were isolated from the DU145 and PC-3 human prostate cancer cell line through flow cytometry.
We studied the growth-inhibitory effects of trabectedin and its molecular mechanisms on human prostate CSCs and non-CSCs. DU-145 and PC-3 CSCs were treated with 0.1, 1, 10 and 100 nM trabectedin for 24, 48 and 72 h and the growth inhibition rates were examined using the sphere-forming assay. Annexin-V assay and immunofluorescence analyses were performed for the detection of the cell death. Concentration-dependent effects of trabectedin on the cell cycle were also evaluated.
The cells were exposed to the different doses of trabectedin for 24, 48 and 72 h to evaluate the effect of trabectedin on the number and diameter of spheroids. According to the results, trabectedin induced cytotoxicity and apoptosis at the IC50 dose, resulting in a significant increase expression of caspase-3, caspase-8, caspase-9, p53 and decrease expression of bcl-2 in dose-dependent manner.
Cell cycle analyses revealed that trabectedin induces dose-dependent G2/M-phase cell cycle arrest, particularly at high-dose treatments. Three-dimensional culture studies showed that trabectedin reduced the number and diameter of spheroids of DU145 and PC3 CSCs.
Furthermore, we have found that trabectedin disrupted cell-cell interactions via E-cadherin in prostasphere of DU-145 and PC-3 CSCs.
Our results showed that trabectedin inhibits cellular proliferation and accelerates apoptotic events in prostate CSCs; and may be a potential effective therapeutic agent against prostate cancer.
26 octubre 2015
PM01183 y Yondelis Presentan Nuevos Datos en el Tratamiento de Cáncer de Ovario en el Congreso ESGO que se Celebra en Nice del 24 al 27 Octubre 2015 .
24 y 25 de Octubre es el Turno del Yondelis ... Diez sus Presentaciones que vienen a Ratificar e incluso Mejorar el porque esta Aprobado en Más de 70 Paises en esta Indicación Ginecologica .
El 26 de Octubre es el Turno del PM01183 ... Con una sola Presentación en Principio .
Chapeau ... los Datos que Presentan del PM01183 en este Congreso en Mujeres con Cáncer de Ovario Resistente a los Platinos .
PM01183 esta Ya en Fase III de Registro para la Indicación de Cáncer de Ovario y este mismo año se Iniciara otra Fase III en el Tratamiento de Cáncer de Pulmón ( SCLC ) .
"" Palabras Mayores con este Farmaco "" .
Cada vez más claro el porque PharmaMar se va a Cotizar al Nasdaq en cuanto pueda .
El 26 de Octubre es el Turno del PM01183 ... Con una sola Presentación en Principio .
Chapeau ... los Datos que Presentan del PM01183 en este Congreso en Mujeres con Cáncer de Ovario Resistente a los Platinos .
PM01183 esta Ya en Fase III de Registro para la Indicación de Cáncer de Ovario y este mismo año se Iniciara otra Fase III en el Tratamiento de Cáncer de Pulmón ( SCLC ) .
"" Palabras Mayores con este Farmaco "" .
Cada vez más claro el porque PharmaMar se va a Cotizar al Nasdaq en cuanto pueda .
Fernández Sousa : « Estamos Descubriendo Nuevas Formas de Atacar al Cáncer ». Pharma Mar Atesora 160.000 Organismos Marinos ,1291 Patentes y Cuatro Potentes Medicamentos contra el Cáncer ... uno de ellos , el PM01183 , Podría ser un Blockbuster contra el Cáncer de Pulmón .
N. RAMÍREZ DE CASTRO / MADRID // 25/10/2015 .
Su empresa PharmaMar ha pasado de ser un quebradero de cabeza a la mina de oro del grupo. Estados Unidos acaba de abrir su mercado a Yondelis, el primer fármaco español contra el cáncer y el primero extraído del fondo marino.
El año en que España anunciaba su entrada en el Mercado Común Europeo, José María Fernández Sousa (Madrid, 1945) confió su destino al mar. Con Zeltia, la empresa familiar, fundó PharmaMar para lanzarse a la búsqueda de soluciones contra el cáncer en el fondo marino. Era una apuesta de riesgo y una locura para muchos. Fernández Sousa solo pensaba en optar por un camino diferente. «Además, si se habían encontrado medicinas en organismos terrestres, ¿por qué no íbamos a hallarlos en el mar, donde vive el 80% de los seres vivos del planeta?». Ahora la compañía atesora una colección de 160.000 organismos marinos, 1.291 patentes y cuatro potentes medicamentos contra el cáncer. Uno de ellos es Yondelis, la estrella de la compañía, que acaba de acceder a Estados Unidos, el principal mercado farmacéutico mundial.
—Yondelis ya se vendía en 78 países, ¿qué ventajas supone la luz verde de la FDA, la agencia del medicamento estadounidense?
—Representa un salto cualitativo importante porque Estados Unidos representa el 47% de todo el mercado oncológico mundial. Con la autorización de la FDA, «Yondelis» aparecerá en las guías internacionales de oncología y cualquier oncólogo del mundo podrá tener referencias del medicamento, ejerza en la India o en Columbia. El fármaco ya está aprobado en Europa y Japón, con lo cual ya abarcamos casi todo el mundo. Solo nos falta China y Australia como mercados importantes.
—¿Este es el fin de una carrera de obstáculos que empezó hace más de veinte años o prefiere pensar en este proceso como una maratón?
—Hoy el registro de muchos fármacos es una carrera de obstáculos. Hay que hacer muchos estudios previos para conseguir que se aprueben. La media en oncología suele ser de unos 14 años. En el caso de Yondelis en Estados Unidos, quizá ha sido un poco más largo de lo que esperábamos porque se intentó una estrategia mixta para obtener la aprobación. Primero para el tratamiento de un tipo de cáncer en ovario y después en sarcoma de tejidos blandos. En el de ovario no se obtuvieron malos resultados, aunque la supervivencia no fue estadísticamente significativa. Estados Unidos lo rechazó en 2009 y ahora hemos conseguido permiso para el tratamiento del sarcoma.
—En 2003, Europa también dijo no. ¿Este último fue el peor bache de la compañía?
—Sí, sin duda.
—¿Y pensó en tirar la toalla y probar con otra molécula?
—No, nosotros creíamos en el fármaco. Pero fue muy duro. La decisión europea nos obligó a hacer un recorte en la plantilla de cien personas. Fue un batacazo que nos obligó a abandonar el desarrollo de otros fármacos. Yondelis era muy importante para nosotros. Finalmente, se aprobó en Europa en 2007 y se convirtió en el primer medicamento español que aprobaba la Unión Europea por procedimiento centralizado. Era también la primera vez en el mundo que se aprobaba un antitumoral marino. De alguna manera hemos sido la primera compañía que ha apostado por el mar por la búsqueda de antitumorales en el mar.
—Ahora ya no lo son, otras empresas siguen sus pasos. ¿Lo interpretan como un espaldarazo a su trabajo o ven con recelo la competencia?
—Al contrario, nos gustaría que hubiera más farmacéuticas para reforzar la idea de que en el mar puede haber soluciones para muchas enfermedades, no solo para el cáncer. Nosotros tenemos ya catalogados organismos de todos los mares del mundo. De Indonesia, Noruega, el Mediterráneo, del Polo Norte, del Sur...No tentemos competencia.
—«Yondelis», es el fármaco estrella, pero solo es eficaz en tumores raros. ¿Esperan aún un superventas, un «blockbuster»?
—Yondelis funciona en sarcoma de tejidos blandos, en algunos tipos de ovarios y en mesotelioma, todas indicaciones huérfanas. Pero tenemos otras moléculas que sí pueden ser un «blockbuster», como el PM1183 contra el cáncer de pulmón.
—¿Cuántas veces ha escuchado a lo largo de su carrera: “Sousa por qué se empeña en el mar”?
—Era un empeño deliberado. Yo antes trabajé en antibióticos e intentaba hacer como el resto de las farmacéuticas, buscar tratamientos de origen terrestre, pero todo lo que encontrábamos estaba ya descubierto. Había que hacer algo nuevo y el mar era una oportunidad nueva. La lógica decía que si se habían encontrado excelentes medicinas naturales, como la penicilina o la misma aspirina en organismos terrestres, ¿por qué no íbamos a encontrarlos en el mar, si el 80% de los seres vivos son organismos marinos?
—¿Y por qué cáncer?
—Porque había una necesidad terapéutica y porque el cáncer es mucho más que una enfermedad, son doscientas diferentes. Para vencerlas necesitamos un gran arsenal terapéutico. Una solución para cada tipo de cáncer de mama, de pulmón, de riñón... Por eso pensamos que había una oportunidad. Además haciendo foco en cáncer las moléculas que pudiéramos encontrar en organismos marinos no tendrían por qué competir unas contra otras. De todas formas, Zeltia también fundó la compañía Noscira para buscar soluciones contra el alzhéimer, pero no tuvimos éxito. La lucha contra el alzhéimer es más difícil que la del cáncer porque se conoce menos. Sin embargo, frente a los tumores estamos encontrando muy buenas actividades en organismos marinos. Lo que hacemos es seleccionar para desarrollo clínico aquellas moléculas que funcionan de forma diferente a todo lo conocido. Estamos descubriendo nuevas formas de atacar a la célula tumoral, al cáncer.
—Al estar tan vinculado profesionalmente a esta enfermedad, ¿le tiene más miedo que a otras dolencias?
—No, yo ya he tenido varios tumores de piel, son epiteliomas basocelulares que se eliminan con cirugía. Ya me han quitado unos diez y ahora estoy citado para quitarme más. Así que huyo del sol, cuando voy a la playa estoy siempre a la sombra. Nunca he fumado y si hay algo que puede provocarlo, siempre intento evitarlo. No le tengo miedo, aunque sé que todos estamos en esa lotería.
—Con su experiencia y la escasez de fármacos para luchar contra bacterias resistentes, ¿no ha pensado en buscar nuevos antibióticos?
—Estamos seguros de que en el mar puede haber nuevos antibióticos. Y también de que en las muestras que tenemos recolectadas en todos los océanos, podemos encontrar actividad antibiótica. Tenemos 160.000 muestras, la mayor colección del mundo. Ahí solo hemos buscado actividad antitumoral, pero estamos seguros de que podríamos encontrar antibióticos, antiinflamatorios, antifúngicos... El problema es que el precio de un antibiótico no paga el coste de su investigación y desarrollo.
—La última estrella del tratamiento del cáncer es la inmunoterapia, conseguir que nuestras defensas luchen contra el tumor. ¿Cree en ella?
—La inmunoterapia ahora está de moda. Parece que funciona en algunos tumores de pulmón y en melanoma, pero no creo que sea una solución para todo como algunos creen.
*****************************************************
Zeltia se llamará PharmaMar a partir del próximo 2 de noviembre .
N. R. C. MADRID .
Zeltia es un grupo de empresas que agrupa a cinco firmas del sector químico, farmacéutico y biotecnológico: PharmaMar (antitumorales de origen marino), Zelnova (insecticidas y ambientadores), Genómica (análisis de ADN), Sylentis ( fármacos basados en silenciamiento génico) y Xylazel (protectores de madera y metales). Fernández Sousa, el mayor accionista, recuerda cómo «algunos no entendían que tiráramos el dinero en la pequeña PharmaMar. Ahora el 95% del valor de Zeltia está en Pharmamar y es la empresa conocida a nivel internacional». Tanto que el pequeño se comerá al gigante y la filial absorberá a Zeltia.
Desde el 2 de noviembre, el Grupo Zeltia pasará a llamarse PharmaMar. Con este nombre comenzará a cotizar en la bolsa madrileña el 2 de noviembre. Y el próximo año podría empeza a cotizar en el Nasdaq de Nueva York .
Su empresa PharmaMar ha pasado de ser un quebradero de cabeza a la mina de oro del grupo. Estados Unidos acaba de abrir su mercado a Yondelis, el primer fármaco español contra el cáncer y el primero extraído del fondo marino.
El año en que España anunciaba su entrada en el Mercado Común Europeo, José María Fernández Sousa (Madrid, 1945) confió su destino al mar. Con Zeltia, la empresa familiar, fundó PharmaMar para lanzarse a la búsqueda de soluciones contra el cáncer en el fondo marino. Era una apuesta de riesgo y una locura para muchos. Fernández Sousa solo pensaba en optar por un camino diferente. «Además, si se habían encontrado medicinas en organismos terrestres, ¿por qué no íbamos a hallarlos en el mar, donde vive el 80% de los seres vivos del planeta?». Ahora la compañía atesora una colección de 160.000 organismos marinos, 1.291 patentes y cuatro potentes medicamentos contra el cáncer. Uno de ellos es Yondelis, la estrella de la compañía, que acaba de acceder a Estados Unidos, el principal mercado farmacéutico mundial.
—Yondelis ya se vendía en 78 países, ¿qué ventajas supone la luz verde de la FDA, la agencia del medicamento estadounidense?
—Representa un salto cualitativo importante porque Estados Unidos representa el 47% de todo el mercado oncológico mundial. Con la autorización de la FDA, «Yondelis» aparecerá en las guías internacionales de oncología y cualquier oncólogo del mundo podrá tener referencias del medicamento, ejerza en la India o en Columbia. El fármaco ya está aprobado en Europa y Japón, con lo cual ya abarcamos casi todo el mundo. Solo nos falta China y Australia como mercados importantes.
—¿Este es el fin de una carrera de obstáculos que empezó hace más de veinte años o prefiere pensar en este proceso como una maratón?
—Hoy el registro de muchos fármacos es una carrera de obstáculos. Hay que hacer muchos estudios previos para conseguir que se aprueben. La media en oncología suele ser de unos 14 años. En el caso de Yondelis en Estados Unidos, quizá ha sido un poco más largo de lo que esperábamos porque se intentó una estrategia mixta para obtener la aprobación. Primero para el tratamiento de un tipo de cáncer en ovario y después en sarcoma de tejidos blandos. En el de ovario no se obtuvieron malos resultados, aunque la supervivencia no fue estadísticamente significativa. Estados Unidos lo rechazó en 2009 y ahora hemos conseguido permiso para el tratamiento del sarcoma.
—En 2003, Europa también dijo no. ¿Este último fue el peor bache de la compañía?
—Sí, sin duda.
—¿Y pensó en tirar la toalla y probar con otra molécula?
—No, nosotros creíamos en el fármaco. Pero fue muy duro. La decisión europea nos obligó a hacer un recorte en la plantilla de cien personas. Fue un batacazo que nos obligó a abandonar el desarrollo de otros fármacos. Yondelis era muy importante para nosotros. Finalmente, se aprobó en Europa en 2007 y se convirtió en el primer medicamento español que aprobaba la Unión Europea por procedimiento centralizado. Era también la primera vez en el mundo que se aprobaba un antitumoral marino. De alguna manera hemos sido la primera compañía que ha apostado por el mar por la búsqueda de antitumorales en el mar.
—Ahora ya no lo son, otras empresas siguen sus pasos. ¿Lo interpretan como un espaldarazo a su trabajo o ven con recelo la competencia?
—Al contrario, nos gustaría que hubiera más farmacéuticas para reforzar la idea de que en el mar puede haber soluciones para muchas enfermedades, no solo para el cáncer. Nosotros tenemos ya catalogados organismos de todos los mares del mundo. De Indonesia, Noruega, el Mediterráneo, del Polo Norte, del Sur...No tentemos competencia.
—«Yondelis», es el fármaco estrella, pero solo es eficaz en tumores raros. ¿Esperan aún un superventas, un «blockbuster»?
—Yondelis funciona en sarcoma de tejidos blandos, en algunos tipos de ovarios y en mesotelioma, todas indicaciones huérfanas. Pero tenemos otras moléculas que sí pueden ser un «blockbuster», como el PM1183 contra el cáncer de pulmón.
—¿Cuántas veces ha escuchado a lo largo de su carrera: “Sousa por qué se empeña en el mar”?
—Era un empeño deliberado. Yo antes trabajé en antibióticos e intentaba hacer como el resto de las farmacéuticas, buscar tratamientos de origen terrestre, pero todo lo que encontrábamos estaba ya descubierto. Había que hacer algo nuevo y el mar era una oportunidad nueva. La lógica decía que si se habían encontrado excelentes medicinas naturales, como la penicilina o la misma aspirina en organismos terrestres, ¿por qué no íbamos a encontrarlos en el mar, si el 80% de los seres vivos son organismos marinos?
—¿Y por qué cáncer?
—Porque había una necesidad terapéutica y porque el cáncer es mucho más que una enfermedad, son doscientas diferentes. Para vencerlas necesitamos un gran arsenal terapéutico. Una solución para cada tipo de cáncer de mama, de pulmón, de riñón... Por eso pensamos que había una oportunidad. Además haciendo foco en cáncer las moléculas que pudiéramos encontrar en organismos marinos no tendrían por qué competir unas contra otras. De todas formas, Zeltia también fundó la compañía Noscira para buscar soluciones contra el alzhéimer, pero no tuvimos éxito. La lucha contra el alzhéimer es más difícil que la del cáncer porque se conoce menos. Sin embargo, frente a los tumores estamos encontrando muy buenas actividades en organismos marinos. Lo que hacemos es seleccionar para desarrollo clínico aquellas moléculas que funcionan de forma diferente a todo lo conocido. Estamos descubriendo nuevas formas de atacar a la célula tumoral, al cáncer.
—Al estar tan vinculado profesionalmente a esta enfermedad, ¿le tiene más miedo que a otras dolencias?
—No, yo ya he tenido varios tumores de piel, son epiteliomas basocelulares que se eliminan con cirugía. Ya me han quitado unos diez y ahora estoy citado para quitarme más. Así que huyo del sol, cuando voy a la playa estoy siempre a la sombra. Nunca he fumado y si hay algo que puede provocarlo, siempre intento evitarlo. No le tengo miedo, aunque sé que todos estamos en esa lotería.
—Con su experiencia y la escasez de fármacos para luchar contra bacterias resistentes, ¿no ha pensado en buscar nuevos antibióticos?
—Estamos seguros de que en el mar puede haber nuevos antibióticos. Y también de que en las muestras que tenemos recolectadas en todos los océanos, podemos encontrar actividad antibiótica. Tenemos 160.000 muestras, la mayor colección del mundo. Ahí solo hemos buscado actividad antitumoral, pero estamos seguros de que podríamos encontrar antibióticos, antiinflamatorios, antifúngicos... El problema es que el precio de un antibiótico no paga el coste de su investigación y desarrollo.
—La última estrella del tratamiento del cáncer es la inmunoterapia, conseguir que nuestras defensas luchen contra el tumor. ¿Cree en ella?
—La inmunoterapia ahora está de moda. Parece que funciona en algunos tumores de pulmón y en melanoma, pero no creo que sea una solución para todo como algunos creen.
*****************************************************
Zeltia se llamará PharmaMar a partir del próximo 2 de noviembre .
N. R. C. MADRID .
Zeltia es un grupo de empresas que agrupa a cinco firmas del sector químico, farmacéutico y biotecnológico: PharmaMar (antitumorales de origen marino), Zelnova (insecticidas y ambientadores), Genómica (análisis de ADN), Sylentis ( fármacos basados en silenciamiento génico) y Xylazel (protectores de madera y metales). Fernández Sousa, el mayor accionista, recuerda cómo «algunos no entendían que tiráramos el dinero en la pequeña PharmaMar. Ahora el 95% del valor de Zeltia está en Pharmamar y es la empresa conocida a nivel internacional». Tanto que el pequeño se comerá al gigante y la filial absorberá a Zeltia.
Desde el 2 de noviembre, el Grupo Zeltia pasará a llamarse PharmaMar. Con este nombre comenzará a cotizar en la bolsa madrileña el 2 de noviembre. Y el próximo año podría empeza a cotizar en el Nasdaq de Nueva York .
Suscribirse a:
Entradas (Atom)