En Medio de las crecientes preocupaciones sobre el uso y los posibles beneficios de la terapia con plasma de convalecencia , un grupo de investigación en los Estados Unidos ha identificado tres anticuerpos humanos (Abs) que, cuando se combinan, demuestran ambas propiedades supresoras virales sólidas contra todos los coronavirus 2 (síndrome respiratorio agudo agudo severo probado) ( SARS-CoV-2) Variantes preocupantes (VoC) in vitro y profunda eficacia antiviral in vivo .
Estos Abs recombinantes, identificados inicialmente a partir del plasma de pacientes convalecientes de la enfermedad por coronavirus 19 (COVID-19), se unen a tres epítopos no superpuestos en el dominio de unión al receptor (RBD), y cada uno ejerce una potente actividad antiviral por sí mismo.
Una versión preimpresa del trabajo de investigación está disponible en el servidor bioRxiv * mientras el artículo se somete a revisión por pares.
Necesidad de una terapia Covid-19 eficaz
La pandemia de COVID-19 sigue planteando desafíos sanitarios y económicos extraordinarios en todo el mundo. Aunque se han lanzado muchas vacunas preventivas, todavía existen preocupaciones de protección debido a la vacilación de la vacuna, un aumento en las variantes resistentes a las vacunas novedosas, insuficiencia inmunológica u otros déficits en la respuesta inmunitaria.
La terapia con plasma de convalecencia que proporciona inmunización pasiva se ha utilizado en todo el mundo para tratar a pacientes hospitalizados con COVID-19 y prevenir la progresión de la enfermedad. Sin embargo, aumenta la incertidumbre con respecto a la eficacia del plasma, ya que los ensayos controlados aleatorios han proporcionado resultados mixtos con respecto a los beneficios de supervivencia del plasma convaleciente.
Las mutaciones en la proteína pico (S) del SARS-CoV-2 han dado como resultado cepas variantes más infecciosas o más virulentas. Además, informes recientes han demostrado que las terapias con Ab que contienen cócteles de uno o dos Ab pueden generar mutantes de escape después de algunos pases.
Por lo tanto, el equipo enfatiza el desarrollo de un cóctel de Ab robusto que contiene al menos tres Abs para proporcionar una medida antiviral eficaz para prevenir la generación de variantes de escape viral.
El cóctel Three-Ab, IMM-BCP-01, muestra un fuerte efecto antiviral con cargas virales iniciales más altas
Utilizando un interrogatorio imparcial de una biblioteca de Abs antivirales derivados del paciente, el equipo ha identificado tres Abs complementarios, IMM20190, IMM20184 e IMM20253, que tienen fuertes efectos antivirales cuando se combinan.
El tratamiento con uno o dos de esta combinación de Ab condujo a una fuerte eliminación viral de los pulmones cuando se administró a hámsteres dorados sirios 6 horas después de la exposición al SARS-CoV-2. Sin embargo, el aclaramiento viral más robusto se observó con el cóctel de tres Ab.
El cóctel IMM-BCP-01 también redujo el título viral en los pulmones de animales infectados con una carga viral inicial 10 veces mayor que la reportada en otros estudios. Además, el cóctel IMM-BCP-01 que comprende los tres Abs en proporciones equimolares (1: 1: 1) logró el nivel más constante de eliminación viral.
Se alcanzaron niveles eficaces de IgG en sangre con niveles de dosis tan bajos como 0,1 mg cada uno y los datos sugieren que dosis tan bajas como 0,1 mg de cada Ab (dosis total de 0,3 mg) son eficaces tanto en el entorno profiláctico como en el de tratamiento.
El equipo también observó una clara respuesta dependiente de la dosis contra los aislamientos de referencia (WA1 / 2020) y Beta (B.1.351) in vivo , en contraste con los informes anteriores de respuesta estancada en el modelo de infección de hámster.
El Cóctel Ab Neutraliza sinérgicamente las variantes del SARS-CoV-2 de una manera dependiente de la dosis
IMM-BCP-01 también supera a S309, el clon parental de VIR-7831 (usado clínicamente para el tratamiento con COVID-19, tanto contra el pseudovirus Delta como contra un pseudovirus de referencia cuando se prueba en ensayos de neutralización de pseudovirus.IMM-BCP-01 fue capaz de neutralizar pseudovirus correspondientes a una gama de VoC y variantes de interés (VoI) de una manera dependiente de la dosis. Curiosamente, el cóctel de tres Ab mostró un modesto aumento en la potencia contra los pseudovirus Delta (B.1.617.2), Lambda (C. 37) y Epsilon (B.1.429), en comparación con los pseudovirus de referencia .
Notablemente, en las pruebas con aislados de virus intactos, el equipo observó una potencia equivalente o mejor del cóctel IMM-BCP-01 frente a la referencia WA1 / 2020, BavPat (D614G), Alpha (B.1.1.7), Beta (B.1.351). ) y variantes Gamma (P.1) en comparación con el correspondiente ensayo de neutralización de pseudovirus.
La combinación de cóctel de tres Ab también indujo un efecto sinérgico de una manera dependiente de la dosis.
El Cóctel de anticuerpos induce respuestas efectoras sinérgicas in vitro
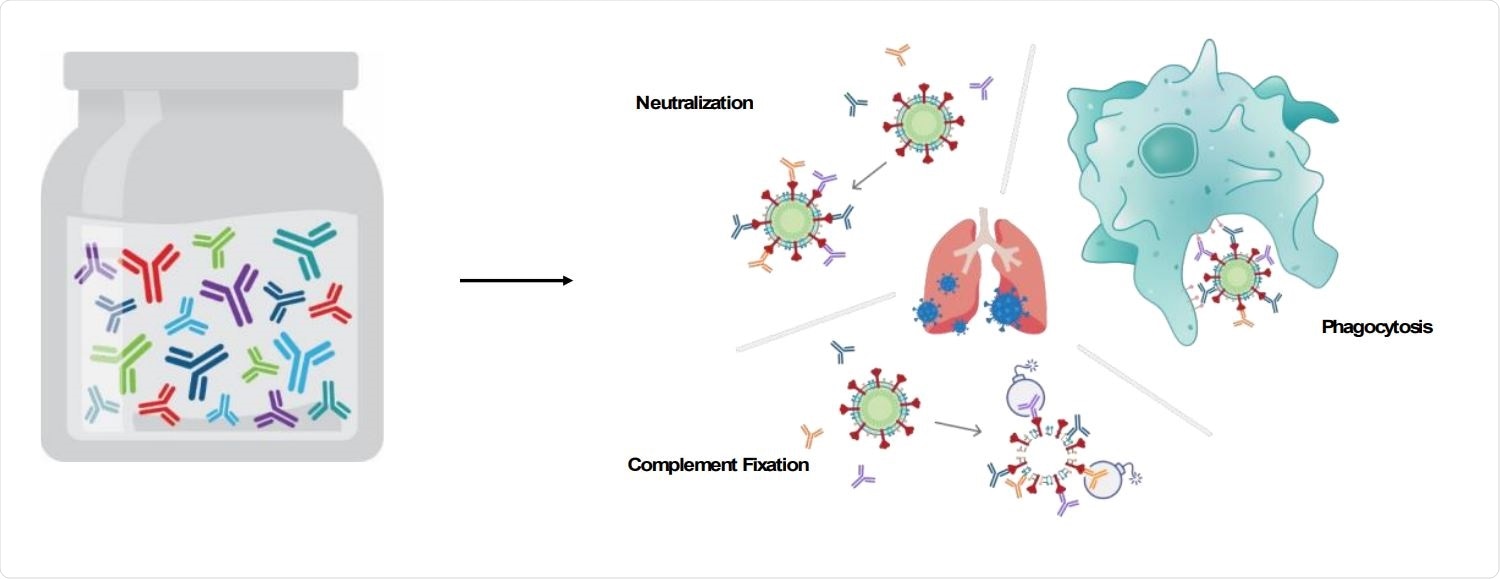
La función efectora intacta es necesaria para una eliminación viral sólida en modelos animales de COVID-19. Utilizando ensayos estándar in vitro, el equipo observó que el cóctel IMM-BCP-01 Ab induce una respuesta oligoclonal a la proteína de pico que activa funciones efectoras productivas mediadas por Fc, como la fagocitosis y la citotoxicidad celular dependiente de anticuerpos de activación de la vía del complemento clásica (ADCC). El equipo atribuye esta respuesta a los dominios Fc de IgG1 intactos en los Abs contribuyentes y a la unión no competitiva al RBD.
La eficacia en múltiples variantes de SARS-CoV-2 se atribuye a la unión de Ab a epítopos conservados que no compiten
El agrupamiento de epítopos y el escaneo de alanina identificaron epítopos únicos, no superpuestos para cada uno de los tres anticuerpos que no competían por los sitios de unión.
Un anticuerpo exhibe un epítopo compuesto que bloquea la unión de ACE2. El segundo anticuerpo une dos proteínas Spike . El tercero neutraliza el virus uniéndose a un epítopo conservado fuera del sitio de unión de ACE2. IMM20190 interactúa con 10 residuos de aminoácidos en el RBD, de los cuales ocho se conservan en todos los CDC VoC. IMM20184 también se une a los residuos de aminoácidos en el núcleo RBD completamente conservado entre todos los COV del SARS-CoV-2, incluida la variante Delta. Solo dos residuos son críticos para la unión de IMM20253, que nuevamente se conservan entre todos los COV.
El ensayo de inhibición del receptor basado en ELISA demostró que IMM20184 inhibió de forma más potente la unión de ACE2 a las tres variantes de RBD (referencia [Wuhan / Washington], Alpha o el Reino Unido [B.1.1.7] y Beta o SA [B.1.351] probado, seguido por IMM20190 e IMM20253. Sin embargo, el efecto inhibidor del cóctel IMM-BCP-01 fue más pronunciado que el efecto de cada anticuerpo individual.