P.J.: De Aprobarse Yondelis tanto en EEUU como en Japón ... J&J Y Taiho Primero Deberan Comprar a PharmaMar el Principio Activo de " Yondelis " ... Segundo : por cada Venta que Realizen pagar los Correspondientes Royaltys ... Tercero : Tambien J&J Y Taiho en Cuantito se Apruebe Yondelis deberan Pagar a PharmaMar xx.xxx.xxx Millones por Hito Coseguido .
*******************************************
PharmaMar Supera Inspección de la FDA para Fabricar el Principio Activo de 'Yondelis' .
31/07/2015 ( EUROPA PRESS // CNMV )) .-
PharmaMar, filial de Zeltia, ha superado la inspección de la Agencia del Medicamento estadounidense (FDA, por sus siglas en inglés) para fabricar la trabectedina, el principio activo de 'Yondelis', ha informado este viernes la sociedad a la Comisión Nacional del Mercado de Valores (CNMV).
De esta forma, PharmaMar mantiene la calificación de fabricante para Estados Unidos que le fue concedida en septiembre de 2009.
La inspección de la FDA estadounidense sobre el sistema de calidad y el proceso de fabricación de la trabectedina tuvo lugar durante el segundo trimestre del año en las instalaciones de PharmaMar en Colmenar Viejo (Madrid).
31 julio 2015
Zeltia . Según el último Informe Publicado por Edison Healthare ... Calculan un Ebitda para este año 2015 de 32 Millones de euros ... Logicamente Estiman un Segundo Semestre Muy Distinto al Primero .
Zeltia S.A.
Edison Healthcare Insight // July 2015 .
Published by Edison Investment Research .
INVESTMENT SUMMARY :
Zeltia is focused on the potentially high-growth marine oncology activities of its PharmaMar business and plans to conduct a reverse-merger whereby PharmaMar would absorb Zeltia, in advance of seeking a US IPO.
PharmaMar has built a pipeline of first-in-class cancer drugs for development with strategic partners.
Zeltia’s FY14 results highlighted ongoing revenue (+6% to €149.7m) and profit (EBITDA €25.7m, +8%) growth, with Yondelis remaining the key contributor.
Further potential catalysts in 2015 include fresh Yondelis approvals for soft tissue sarcoma in the US (PDUFA in October) and Japan (Q315); Aplidin Phase III data in multiple myeloma (Q415); and a Phase III study initiation for PM01183 (2nd generation Yondelis) in small cell lung cancer (SCLC).
INDUSTRY OUTLOOK :
Repositioning the group behind the PharmaMar name and conducting a US IPO could be transformational. The oncology portfolio has been validated through multiple global partnerships, eg J&J in the US and Taiho in Japan (over Yondelis) and Chugai in certain EU countries (for Aplidin).
Y/E Dec // Revenue // EBITDA
--------------- €m) ------- (€m)
2013 ------- 141.8 ------ 23.8
2014 ------- 149.7 ------ 25.7
2015e ------ 164.3 ------ 32,0
Edison Healthcare . Analyst : Christian Glennie .
Edison Healthcare Insight // July 2015 .
Published by Edison Investment Research .
INVESTMENT SUMMARY :
Zeltia is focused on the potentially high-growth marine oncology activities of its PharmaMar business and plans to conduct a reverse-merger whereby PharmaMar would absorb Zeltia, in advance of seeking a US IPO.
PharmaMar has built a pipeline of first-in-class cancer drugs for development with strategic partners.
Zeltia’s FY14 results highlighted ongoing revenue (+6% to €149.7m) and profit (EBITDA €25.7m, +8%) growth, with Yondelis remaining the key contributor.
Further potential catalysts in 2015 include fresh Yondelis approvals for soft tissue sarcoma in the US (PDUFA in October) and Japan (Q315); Aplidin Phase III data in multiple myeloma (Q415); and a Phase III study initiation for PM01183 (2nd generation Yondelis) in small cell lung cancer (SCLC).
INDUSTRY OUTLOOK :
Repositioning the group behind the PharmaMar name and conducting a US IPO could be transformational. The oncology portfolio has been validated through multiple global partnerships, eg J&J in the US and Taiho in Japan (over Yondelis) and Chugai in certain EU countries (for Aplidin).
Y/E Dec // Revenue // EBITDA
--------------- €m) ------- (€m)
2013 ------- 141.8 ------ 23.8
2014 ------- 149.7 ------ 25.7
2015e ------ 164.3 ------ 32,0
Edison Healthcare . Analyst : Christian Glennie .
30 julio 2015
Yondelis Ovario , Nueva Espectativa según Publican Cientificos Chinos . Combined Trabectedin and Anti-PD1 Antibody Produces a Synergistic Antitumor Effect in a Murine Model of Ovarian Cancer .
Journal of Translational Medicine // Published: 29 July 2015 // © 2015 Guo et al.
Zhiqiang Guo1*, Haolin Wang2, Fandong Meng3, Jie Li1 and Shulan Zhang1 .
Abstract
Monoclonal antibodies (mAb) that block programmed death (PD)-1 signaling pathway hold great potential as a novel cancer immunotherapy. Recent evidence suggests that combining with conventional, targeted or other immunotherapies, these mAb can induce synergistic antitumor responses. In this study, we investigated whether Trabectedin (ET-743), a novel anticancer agent currently used for treating relapsed ovarian cancer, can synergize with anti (α)-PD-1 mAb to increase antitumor activity in the murine ID8 ovarian cancer model.
Methods
Mice with established peritoneal ID8 tumor were treated with either single or combined Trabectedin and α-PD-1 mAb, their overall survival was recorded; tumor-associated immune cells and immune gene expression in tumors from treated mice were analyzed by flow cytometry and quantitative RT-PCR, respectively, and antigen-specific immunity of effector CD8 + T cells was evaluated by ELISA and cytotoxicity assay. In addition, the effect of Trabectedin on tumoral PD-L1 expression was analyzed by both flow cytometry and immunofluorescence staining.
Results
Though single treatment showed a modest antitumor effect in mice bearing 10-day-established ID8 tumor, combined Trabectedin and α-PD-1 mAb treatment induced a strong antitumor immune response, leading to a significant tumor regression with half of mice tumor-free 90 days after tumor inoculation. Mechanistic investigation revealed that combination treatment induces a systemic tumor-specific immunity with an indispensable role of both CD4 + and CD8 + T cells, and effector CD8 + T cells exhibited the antigen-specific cytokine secretion and cytotoxicity upon tumor antigen stimulation; additionally, combination treatment increased the IFN-γ-producing effector T cells and decreased the immunosuppressive cells in peritoneal cavity; accordingly, it enhanced the expression of Th1-associated immune-stimulating genes while reducing the transcription of regulatory/suppressive immune genes, reshaping tumor microenvironment from a immunosuppressive to a stimulatory state. Finally, in vivo Trabectedin treatment has been shown to induce IFN-γ-dependent PD-L1 expression within tumor, possibly constituting a mechanistic basis for its synergistic antitumor effect with α-PD-1 mAb therapy.
Conclusion
This study provides the evidence that α-PD-1 mAb can produce a synergistic antitumor efficacy when combined with Trabectedin, a clinically available anticancer agent, supporting a direct translation of this combination strategy in clinic for the treatment of ovarian cancer.
Zhiqiang Guo1*, Haolin Wang2, Fandong Meng3, Jie Li1 and Shulan Zhang1 .
Abstract
Monoclonal antibodies (mAb) that block programmed death (PD)-1 signaling pathway hold great potential as a novel cancer immunotherapy. Recent evidence suggests that combining with conventional, targeted or other immunotherapies, these mAb can induce synergistic antitumor responses. In this study, we investigated whether Trabectedin (ET-743), a novel anticancer agent currently used for treating relapsed ovarian cancer, can synergize with anti (α)-PD-1 mAb to increase antitumor activity in the murine ID8 ovarian cancer model.
Methods
Mice with established peritoneal ID8 tumor were treated with either single or combined Trabectedin and α-PD-1 mAb, their overall survival was recorded; tumor-associated immune cells and immune gene expression in tumors from treated mice were analyzed by flow cytometry and quantitative RT-PCR, respectively, and antigen-specific immunity of effector CD8 + T cells was evaluated by ELISA and cytotoxicity assay. In addition, the effect of Trabectedin on tumoral PD-L1 expression was analyzed by both flow cytometry and immunofluorescence staining.
Results
Though single treatment showed a modest antitumor effect in mice bearing 10-day-established ID8 tumor, combined Trabectedin and α-PD-1 mAb treatment induced a strong antitumor immune response, leading to a significant tumor regression with half of mice tumor-free 90 days after tumor inoculation. Mechanistic investigation revealed that combination treatment induces a systemic tumor-specific immunity with an indispensable role of both CD4 + and CD8 + T cells, and effector CD8 + T cells exhibited the antigen-specific cytokine secretion and cytotoxicity upon tumor antigen stimulation; additionally, combination treatment increased the IFN-γ-producing effector T cells and decreased the immunosuppressive cells in peritoneal cavity; accordingly, it enhanced the expression of Th1-associated immune-stimulating genes while reducing the transcription of regulatory/suppressive immune genes, reshaping tumor microenvironment from a immunosuppressive to a stimulatory state. Finally, in vivo Trabectedin treatment has been shown to induce IFN-γ-dependent PD-L1 expression within tumor, possibly constituting a mechanistic basis for its synergistic antitumor effect with α-PD-1 mAb therapy.
Conclusion
This study provides the evidence that α-PD-1 mAb can produce a synergistic antitumor efficacy when combined with Trabectedin, a clinically available anticancer agent, supporting a direct translation of this combination strategy in clinic for the treatment of ovarian cancer.
Yondelis Nueva Espectativa . Existe ya Prueba de Concepto de que Trabectedin Puede Actuar de Policia Bueno y Cargarse a los Policias Corruptos ( Fagocitos ) que en lugar de Atacar a la celulas Cancerigenas ... Permiten que estas Crezcan y se expandan ( Metastasis ) .
P.J. : Datos que demuestran la actividad específica de 'Yondelis' sobre el microambiente tumoral, concretamente reduciendo los macrófagos asociados al tumor.
Así, además de inducir la muerte de las células tumorales, 'Yondelis' actúa deplecionando los macrófagos asociados al tumor. Estas células, que normalmente forman parte del sistema inmunológico, tienen en el tumor una actividad protumoral ya que liberan una serie de factores que estimulan la división de las células tumorales así como la formación de neovasos.
Al inducir la muerte de éstas células, 'Yondelis' inhibe esta actividad protumoral y disminuye la secreción de los factores estimulantes del crecimiento tumoral. Este mecanismo de acción es particular a 'Yondelis' y no se observa con ninguna de los otros agentes antitumorales estudiados.
**************************************************
Phagocytes as Corrupted Policemen in Cancer-Related Inflammation.
July 2015
Bonavita E1, Galdiero MR2, Jaillon S1, Mantovani A3.
Author information1IRCCS Istituto Clinico Humanitas, Rozzano, Italy.2IRCCS Istituto Clinico Humanitas, Rozzano, Italy; Division of Clinical Immunology and Allergy, University of Naples Federico II, Naples, Italy.3IRCCS Istituto Clinico Humanitas, Rozzano, Italy; Humanits University, Rozzano, Italy.
Abstract :
Inflammation is a key component of the tumor microenvironment. Tumor-associated macrophages (TAMs) and tumor-associated neutrophils (TANs) are prototypic inflammatory cells in cancer-related inflammation. Macrophages provide a first line of resistance against infectious agents but in the ecological niche of cancer behave as corrupted policemen. TAMs promote tumor growth and metastasis by direct interactions with cancer cells, including cancer stem cells, as well as by promoting angiogenesis and tissue remodeling and suppressing effective adaptive immunity. In addition, the efficacy of chemotherapy, radiotherapy, and checkpoint blockade inhibitors is profoundly affected by regulation of TAMs. In particular, TAMs can protect and rescue tumor cells from cytotoxic therapy by orchestrating a misguided tissue repair response. Following extensive preclinical studies, there is now proof of concept that targeting tumor-promoting macrophages by diverse strategies (e.g., Trabectedin, anti-colony-stimulating factor-1 receptor antibodies) can result in antitumor activity in human cancer and further studies are ongoing. Neutrophils have long been overlooked as a minor component of the tumor microenvironment, but there is evidence for an important role of TANs in tumor progression. Targeting phagocytes (TAMs and TANs) as corrupted policemen in cancer may pave the way to innovative therapeutic strategies complementing cytoreductive therapies and immunotherapy
Así, además de inducir la muerte de las células tumorales, 'Yondelis' actúa deplecionando los macrófagos asociados al tumor. Estas células, que normalmente forman parte del sistema inmunológico, tienen en el tumor una actividad protumoral ya que liberan una serie de factores que estimulan la división de las células tumorales así como la formación de neovasos.
Al inducir la muerte de éstas células, 'Yondelis' inhibe esta actividad protumoral y disminuye la secreción de los factores estimulantes del crecimiento tumoral. Este mecanismo de acción es particular a 'Yondelis' y no se observa con ninguna de los otros agentes antitumorales estudiados.
**************************************************
Phagocytes as Corrupted Policemen in Cancer-Related Inflammation.
July 2015
Bonavita E1, Galdiero MR2, Jaillon S1, Mantovani A3.
Author information1IRCCS Istituto Clinico Humanitas, Rozzano, Italy.2IRCCS Istituto Clinico Humanitas, Rozzano, Italy; Division of Clinical Immunology and Allergy, University of Naples Federico II, Naples, Italy.3IRCCS Istituto Clinico Humanitas, Rozzano, Italy; Humanits University, Rozzano, Italy.
Abstract :
Inflammation is a key component of the tumor microenvironment. Tumor-associated macrophages (TAMs) and tumor-associated neutrophils (TANs) are prototypic inflammatory cells in cancer-related inflammation. Macrophages provide a first line of resistance against infectious agents but in the ecological niche of cancer behave as corrupted policemen. TAMs promote tumor growth and metastasis by direct interactions with cancer cells, including cancer stem cells, as well as by promoting angiogenesis and tissue remodeling and suppressing effective adaptive immunity. In addition, the efficacy of chemotherapy, radiotherapy, and checkpoint blockade inhibitors is profoundly affected by regulation of TAMs. In particular, TAMs can protect and rescue tumor cells from cytotoxic therapy by orchestrating a misguided tissue repair response. Following extensive preclinical studies, there is now proof of concept that targeting tumor-promoting macrophages by diverse strategies (e.g., Trabectedin, anti-colony-stimulating factor-1 receptor antibodies) can result in antitumor activity in human cancer and further studies are ongoing. Neutrophils have long been overlooked as a minor component of the tumor microenvironment, but there is evidence for an important role of TANs in tumor progression. Targeting phagocytes (TAMs and TANs) as corrupted policemen in cancer may pave the way to innovative therapeutic strategies complementing cytoreductive therapies and immunotherapy
29 julio 2015
PM01183 Completa la Fase I para el Tratamiento de Leucemia . Clinical Study of PM01183 in Patients With Acute Leukemia or Relapsed/Refractory Myelodysplastic Syndrome .
*.- Health Authority: United States: Food and Drug Administration .
*.- This study has been completed .
*.- Sponsor: PharmaMar .
*.- Last updated: July 27, 2015 .
*.- Last verified: July 2015 .
Enrollment: 45
Study Start Date: May 2011
Study Completion Date: July 2015
Primary Completion Date: July 2015 (Final data collection date for primary outcome measure)
*.- Locations :
* United States, Minnesota
Rochester, Minnesota, United States, 55905
* United States, Texas
Houston, Texas, United States, 77030
*.- This study has been completed .
*.- Sponsor: PharmaMar .
*.- Last updated: July 27, 2015 .
*.- Last verified: July 2015 .
Enrollment: 45
Study Start Date: May 2011
Study Completion Date: July 2015
Primary Completion Date: July 2015 (Final data collection date for primary outcome measure)
*.- Locations :
* United States, Minnesota
Rochester, Minnesota, United States, 55905
* United States, Texas
Houston, Texas, United States, 77030
Las Ventas Netas de Yondelis® Crecen un 11,4% hasta los 43,6 millones durante el primer semestre 2015 . La fecha límite (PDUFA date) para la potencial aprobación de Yondelis® en EEUU por parte de la FDA es el 24 de Octubre 2015.
El Grupo Zeltia Registra unas Ventas Netas de 84,4 Millones de Euros (+7,8%) .
Las Ventas Netas de Yondelis® Crecen un 11,4% Hasta los 43,6 Millones.
EL EBITDA del Grupo ha sido de 9,5 millones de euros, después de incrementar el gasto en I+D en un 28%, reflejando el avance clínico de la cartera de productos.
Madrid, 28 de Julio del 2015:
El grupo Zeltia ha registrado unas ventas netas totales durante la primera mitad del año de 84,4 millones de euros, cifra que supone un incremento del 7,8% con respecto al mismo periodo del año anterior. Por segmentos, durante los seis primeros meses del año, el área de biofarmacia ha registrado unas ventas de 46,6 millones de euros (+11,8%), de los que 43,6 millones de euros corresponden a las ventas de Yondelis®. Esto supone un crecimiento de las ventas de Yondelis® de un 11,4% con respecto al primer semestre del año pasado. Parte de este crecimiento se corresponde a la venta de materia prima a Janssen Products LP que ha sido de 3,3 millones de euros.
Por su parte, el segmento de química de gran consumo ha registrado unas ventas netas de 37 millones de euros (+3%) frente a los 36 millones registrados en el mismo periodo del año anterior.
El grupo Zeltia ha registrado en los primeros seis meses del año un EBITDA de 9,5 millones de euros frente a los 22 millones que registró el mismo periodo del año anterior. Dos factores marcan principalmente esta diferencia en el EBITDA con respecto al primer semestre del año pasado. Por un lado se ha producido un incremento en el gasto en I+D en este primer semestre del año como consecuencia de los diferentes avances clínicos de la cartera de productos en oncología. En este sentido, la compañía comunicó recientemente la finalización del reclutamiento del ensayo en fase III con Aplidina para el tratamiento de mieloma múltiple y se espera finalizar el año con dos ensayos en fase III en marcha con nuestro compuesto PM1183. Uno de ellos para el tratamiento de cáncer de ovario resistente a platino, iniciado recientemente, y otro para el tratamiento de pulmón de células pequeñas. Así pues, el total de inversión en I+D durante los primeros seis meses del año ha sido de 30,5 millones (vs. 23,8 millones en la primera mitad del año anterior).
Por otra parte, a junio de 2015, bajo el epígrafe de otros ingresos de explotación, el grupo Zeltia registró un total de 11,7 millones de euros frente a los 19,8 millones registrados en el primer semestre del año anterior.
Hay que recordar que PharmaMar ha registrado este año un pago de 10 millones de dólares correspondientes al último hito del acuerdo firmado en 2011 con Janssen Products LP y que compara con el hito correspondiente al año anterior el cual estaba fijado en 25 millones de dólares.
A lo largo de este año podrían producirse otros cobros por cumplimiento de hitos como la aprobación de Yondelis® para el tratamiento de sarcoma de tejido blando tanto en EEUU como en Japón. La fecha límite (PDUFA date) para la potencial aprobación de Yondelis® en EEUU por parte de la FDA es el 24 de Octubre 2015.
Con todo ello, el grupo ha registrado un resultado neto atribuible de 3,3 millones de euros (vs 16,7 millones de euros).
28 julio 2015
Zeltia , Resultados Primer Semestre : Las Ventas Netas Totales del Grupo Ascienden a 84,4 millones de euros (+7,8%). .
Madrid, a 28 de julio de 2015 .
HITOS JUNIO 2015 .
Corporativos :
Las ventas netas totales del Grupo ascienden a 84,4 millones de euros (+7,8%).
De ellas 43,6 millones (+11,4%) corresponden a Yondelis®, (40,3 millones de ventas comerciales más 3,3 millones de venta de materia prima a Janssen) .
El segmento de Química de Gran Consumo mejora las ventas un 3%, alcanzando los 37,1 millones de euros.
El EBITDA del Grupo asciende a 9,5 millones de euros, (22,1 millones a junio de 2014). Como ya ocurría en el primer trimestre, esta diferencia en el EBITDA se produce porque el pago por cumplimiento de hito del contrato de 2011 con Janssen Products acordado para 2015 asciende a 10 millones de dólares frente a los 25 millones acordados para el ejercicio 2014.
El pasado 30 de junio, la Junta General de Accionistas de Zeltia y el accionista único de PharmaMar aprobaron la fusión inversa de PharmaMar (sociedad absorbente) y Zeltia (sociedad absorbida).
El 7 de julio fueron suscritos y desembolsados Bonos simples emitidos por Zeltia por un importe de 17 millones de euros, que se incorporaron a negociación en el Mercado Alternativo de Renta Fija (“MARF”) el día 8 de julio de 2015.
Oncología .
Finalizó el reclutamiento de pacientes del ensayo pivotal y de registro de fase III con Aplidin para la indicación de mieloma múltiple.
Se inicia el reclutamiento de pacientes en el ensayo pivotal y de registro de fase III (CORAIL) de PM1183 en pacientes con cáncer de ovario platino-resistente.
En el mes de febrero de 2015 la FDA otorgó revisión prioritaria/acelerada (priority review) a la solicitud de autorización de comercialización de Yondelis para tratamiento de sarcoma de tejidos blandos presentada por Janssen. Posteriormente, el pasado mes de mayo, la FDA comunicó a Janssen que ampliaba hasta en tres meses el plazo para finalizar la evaluación prioritaria de la solicitud de registro de Yondelis®.
En el Congreso Anual de la Sociedad Americana de Oncología Clínica celebrado en Chicago durante los días 29 de mayo a 2 de junio se realizó una presentación oral de los datos del ensayo clínico de fase III SAR3007 realizado por nuestro socio Janssen, que muestran una mejora significativa de la supervivencia libre de progresión con Yondelis® frente a dacarbazina en pacientes con liposarcoma o leiomiosarcoma avanzado tratados previamente con antraciclina y al menos otra quimioterapia.
...
Márgenes: Margen bruto y Resultado bruto de explotación (EBITDA) :
El margen bruto del Grupo experimenta un ligero descenso del entorno de 1% con respecto al primer semestre de 2014, debido a que en el primer semestre de 2015 la cifra de ventas incluye 3,3 millones de materia prima a Janssen, venta que, como es lógico, tiene un menor margen que la venta comercial.
El EBITDA del Grupo, a junio de 2015 asciende a 9,5 millones de euros, (22,1 millones de euros en 2014). Esta diferencia se produce como consecuencia del cobro del acuerdo firmado en 2011 con Janssen Products LP, ya que el cobro correspondiente a 2015 se estableció en 10 millones de dólares, mientras que el correspondiente a 2014 se había establecido en 25 millones de dólares. Si a lo largo del año se produjeran las aprobaciones de registro de Yondelis en Estados Unidos y Japón para la indicación de sarcoma de tejidos blandos, se recibirían otros ingresos por cumplimiento de hitos acordados en los contratos de licencia que PharmaMar tiene firmados con sus socios Janssen y Taiho, que mitigarían este efecto del primer semestre.
(EBITDA, o Resultado bruto de explotación, incluye todos los ingresos y gastos excepto amortizaciones, provisiones, gastos financieros e impuestos).-
**************************************
Inversión en I+D :
La inversión en I+D ha aumentado un 28,5% entre periodos, pasando de 23,8 millones de euros a junio 2014 a 30,6 millones de euros en junio 2015. En el área de Oncología, durante el primer semestre de 2015 se han invertido 26,2 millones de euros (20,2 millones en 2014), en las áreas de Diagnóstico y RNA de interferencia se han invertido 4,1 millones de euros (3,0 millones en 2014).
En el área de oncología; este incremento de la inversión en I+D, proviene principalmente del desarrollo de PM1183, en concreto del ensayo pivotal y de registro para la indicación de ovario platino resistente, cuyo reclutamiento se ha iniciado en el segundo semestre de este año. En dicho ensayo participan 112 centros de 13 países de Europa y Norteamérica. Adicionalmente, se están realizando con PM1183 ensayos de fase I y II, así como ensayos en preclínica y de desarrollo químico del compuesto, con el fin de obtener el máximo de información sobre el mismo.
*************************************
Tesorería y Deuda :
La caja y equivalentes sumadas a las inversiones financieras corrientes y no corrientes, alcanza los 31,9 millones de euros (36,6 a 31 de diciembre de 2014). La deuda financiera total del Grupo (corriente y no corriente) asciende a 93,6 millones de euros (91,5 millones de euros en diciembre 2014).
En la primera mitad del año se ha iniciado un proceso de reorganización de la deuda tendente a alargar los vencimientos de los préstamos bancarios, para así dar una mayor flexibilidad a la compañía mediante la liberación de flujos de caja que pueden ser utilizados en la financiación del I+D. El inicio de dicha reorganización se puede apreciar en la tabla de estructura de la deuda que se presenta más adelante.
En este sentido, Zeltia emitió bonos simples por un importe de 17 millones de euros y a un plazo de 12 años, vencimiento bullet, que fueron suscritos y desembolsados el pasado día 7 de julio y se incorporaron a negociación en el Mercado Alternativo de Renta Fija (“MARF”) el día 8 de julio. El efecto de esta emisión de bonos, no se recoge en la tabla que se muestra a continuación ya que dicha tabla contiene datos hasta 30 de junio.
De la misma forma, en este primer semestre se aprecia un incremento en la utilización de las pólizas de crédito, habitual en este periodo del año. El límite de las pólizas de crédito del Grupo asciende a 35,9 millones de euros, quedando, en consecuencia, disponibles 16,2 millones de euros.
*******************************************+
Oncología: PharmaMar
En el mes de enero, Taiho Pharmaceutical, socio Japonés de PhamaMar para Yondelis, presentó ante la agencia reguladora japonesa, PMDA, la solicitud de autorización de comercialización de Yondelis (trabectedina) para el tratamiento de varios subtipos de sarcoma de tejidos blandos, en base al beneficio clínico obtenido en el estudio pivotal de Fase II. La solicitud será revisada en modo “priority review” ya que trabectedina había sido designada previamente medicamento huérfano en Japón.
En el mes de febrero, la Agencia reguladora americana, FDA, comunicó a nuestro socio Janssen Research&Development, que revisará en modo prioritatio “priority review” la solicitud de autorización de comercialización de Yondelis® (trabectedin) para sarcomas de tejidos blandos. El pasado mes de mayo, la FDA comunicó a Janssen que ampliaba hasta en tres meses el plazo para finalizar la evaluación prioritaria de la solicitud de registro de Yondelis®. Esta ampliación del plazo proporcionará a la Agencia el tiempo necesario para completar la evaluación prioritaria de la solicitud de autorización de comercialización.
*********************************************
PM060184 :
Tras la definición de la dosis recomendada para ensayos clínicos fase II, y tras el análisis de la actividad observada en los estudios ya finalizados de fase I, se han diseñado los primeros estudios de fase II del compuesto. El primero será un estudio en cáncer de mama avanzado en el subgrupo de receptores hormonales positivos y her2 neu negativo. Este estudio se llevará a cabo en España, Bélgica y Francia. El segundo estudio fase II se realizará en pacientes con cáncer colorectal avanzado que hayan recibido tratamiento estándar y se llevará a cabo en Estados Unidos, Canadá y España.
Continúa además el reclutamiento del estudio fase I en combinación con gemcitabina en dos centros en España y Estados Unidos.
...
Zeltia una de las cotizadas españolas que más mejorarán en 2016 en cuestión de Ingresos ( + 25 % ) .
Borja Jiménez de Francisco /// Martes, 28. Julio 2015 -
Amper, Vidrala, Zeltia, Gamesa, Cie Automotive, DIA, Cementos Portland o Zeltia registrarán mejores beneficios.
De los cientos de empresas que cotizan en España, se pueden extraer aquellas cuyos ingresos tengan unas mejores previsiones de cara al próximo curso. Desde NEGOCIOS.COM hemos seleccionado las diez que el consenso de Reuters ve con mejores ojos para 2016.
Todas ellas engrosarán sus ingresos, según la citada agencia, por encima del 20%.
...
Cementos Portland se ve cada vez con mejores ojos. El cambio de estrategia impulsado por Carlos Slim en la filial de FCC y la recuperación de la demanda de cemento, tanto en España como en Estados Unidos, hacen que las perspectivas auguren un crecimiento de sus ingresos próximo al 25%. Crecimiento idéntico al que se espera de Zeltia, sobre todo debido a la recuperación de su negocio de química de gran consumo.
...
Amper, Vidrala, Zeltia, Gamesa, Cie Automotive, DIA, Cementos Portland o Zeltia registrarán mejores beneficios.
De los cientos de empresas que cotizan en España, se pueden extraer aquellas cuyos ingresos tengan unas mejores previsiones de cara al próximo curso. Desde NEGOCIOS.COM hemos seleccionado las diez que el consenso de Reuters ve con mejores ojos para 2016.
Todas ellas engrosarán sus ingresos, según la citada agencia, por encima del 20%.
...
Cementos Portland se ve cada vez con mejores ojos. El cambio de estrategia impulsado por Carlos Slim en la filial de FCC y la recuperación de la demanda de cemento, tanto en España como en Estados Unidos, hacen que las perspectivas auguren un crecimiento de sus ingresos próximo al 25%. Crecimiento idéntico al que se espera de Zeltia, sobre todo debido a la recuperación de su negocio de química de gran consumo.
...
Yondelis and Irinotecan in Pediatric Refractory Sarcomas .
Administrative Data :
Organization name : Technische Universität München
Organization study ID TrI.PReSarc V150429
Sponsor : Technische Universität München
Health Authority Germany : Ethics Commission
...
Sarcoma de Ewing :
Es un tumor óseo maligno (canceroso) que afecta a los niños.
El sarcoma de Ewing se puede presentar en cualquier momento durante la niñez y comienzos de la edad adulta, pero generalmente se desarrolla en la pubertad, cuando los huesos están creciendo rápidamente. Es 10 veces tan común en niños de raza blanca como en niños afroamericanos, africanos y asiáticos.
El tumor puede originarse en cualquier parte del cuerpo. Generalmente empieza en los huesos largos de los brazos y las piernas, la pelvis o el tórax, al igual que en el cráneo o en los huesos planos del tronco.
El tumor a menudo se disemina (hace metástasis) a los pulmones y a otros huesos. Al momento del diagnóstico, la metástasis se observa en aproximadamente un tercio de los niños con este tipo de sarcoma.
En raras ocasiones, el sarcoma de Ewing ocurre en adultos.
...
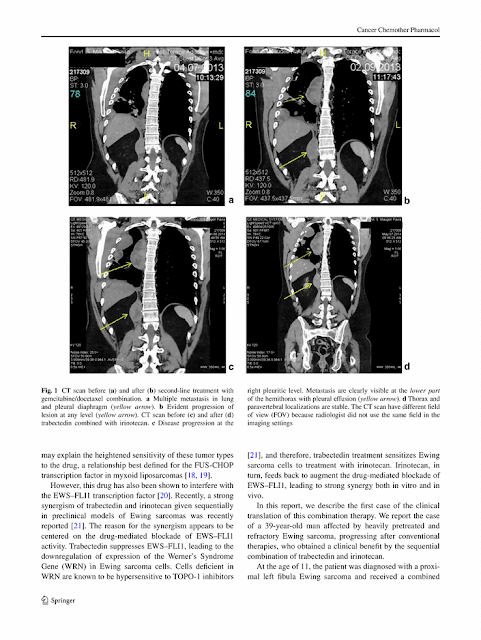
Yondelis // Irinotecan : Fuerte Sinergia de Acción Contra el Sarcoma de Ewing .
En esta Foto se apreciar la actuación del Yondelis // Irinotecan :
Organization name : Technische Universität München
Organization study ID TrI.PReSarc V150429
Sponsor : Technische Universität München
Health Authority Germany : Ethics Commission
...
Sarcoma de Ewing :
Es un tumor óseo maligno (canceroso) que afecta a los niños.
El sarcoma de Ewing se puede presentar en cualquier momento durante la niñez y comienzos de la edad adulta, pero generalmente se desarrolla en la pubertad, cuando los huesos están creciendo rápidamente. Es 10 veces tan común en niños de raza blanca como en niños afroamericanos, africanos y asiáticos.
El tumor puede originarse en cualquier parte del cuerpo. Generalmente empieza en los huesos largos de los brazos y las piernas, la pelvis o el tórax, al igual que en el cráneo o en los huesos planos del tronco.
El tumor a menudo se disemina (hace metástasis) a los pulmones y a otros huesos. Al momento del diagnóstico, la metástasis se observa en aproximadamente un tercio de los niños con este tipo de sarcoma.
En raras ocasiones, el sarcoma de Ewing ocurre en adultos.
...
Yondelis // Irinotecan : Fuerte Sinergia de Acción Contra el Sarcoma de Ewing .
En esta Foto se apreciar la actuación del Yondelis // Irinotecan :
Hernández: «No hay que obsesionarse con el cáncer, pero sí adherirse a planes de detección precoz» .
No todos los cánceres pueden diagnosticarse con antelación, pero sí es importante acudir al médico ante síntomas extraños o anomalías», asegura.
ANA VOZMEDIANO | SAN SEBASTIÁN /// 28 julio 2015 .
Hace seis años que Amaia Hernández trabaja como oncóloga, los últimos cinco en Onkologikoa de San Sebastián. Dentro del Aula de Educación Sanitaria, la doctora Hernández ofreció recientemente en la sede del Colegio Oficial de Médicos una charla sobre la detección precoz del cáncer con un título sugerente: '¿Cómo puedo detectar que tengo cáncer?' El mensaje que quiso lanzar es claro: «No hay que obsesionarse, ni intentar matar mosquitos a cañonazos», pero sí acogerse a los programas de diagnostico precoz que existen. Y sobre todo, saber que cada patología es diferente.
- El título de su charla no podía ser más directo. Pero dígame: ¿Cómo puedo detectar que tengo cáncer?
-No se trata de utilizar métodos caseros y mucho menos de obsesionarse, porque eso no conduce a nada. Lo que quiero explicar a la gente es la importancia de acogerse a los planes que lanza Osakidetza para determinadas dolencias, los que tienen que ver con la patología de mama y el de colon. Hay tumores que tienen programas de detección precoz y otros que no, porque no tiene sentido organizar planes que no van a ser efectivos y someter a pruebas a la población sin más.
- Alguien podría pensar que su charla iba a tratar de pequeñas pruebas caseras que puedan aliviar alguna sospecha de haber contraído esta enfermedad.
- En casa es complicado detectarse nada y mucho menos diagnosticarse a uno mismo, pero sí podemos percibir sangre en las heces o un bulto en la mama, por ejemplo. Eso no quiere decir que por tener ese síntoma la persona tenga cáncer. Será el especialista el que lo averigüe y el que haga el diagnóstico. Creo que también hay que insistir en eso, que un síntoma no es un cáncer.
...
ANA VOZMEDIANO | SAN SEBASTIÁN /// 28 julio 2015 .
Hace seis años que Amaia Hernández trabaja como oncóloga, los últimos cinco en Onkologikoa de San Sebastián. Dentro del Aula de Educación Sanitaria, la doctora Hernández ofreció recientemente en la sede del Colegio Oficial de Médicos una charla sobre la detección precoz del cáncer con un título sugerente: '¿Cómo puedo detectar que tengo cáncer?' El mensaje que quiso lanzar es claro: «No hay que obsesionarse, ni intentar matar mosquitos a cañonazos», pero sí acogerse a los programas de diagnostico precoz que existen. Y sobre todo, saber que cada patología es diferente.
- El título de su charla no podía ser más directo. Pero dígame: ¿Cómo puedo detectar que tengo cáncer?
-No se trata de utilizar métodos caseros y mucho menos de obsesionarse, porque eso no conduce a nada. Lo que quiero explicar a la gente es la importancia de acogerse a los planes que lanza Osakidetza para determinadas dolencias, los que tienen que ver con la patología de mama y el de colon. Hay tumores que tienen programas de detección precoz y otros que no, porque no tiene sentido organizar planes que no van a ser efectivos y someter a pruebas a la población sin más.
- Alguien podría pensar que su charla iba a tratar de pequeñas pruebas caseras que puedan aliviar alguna sospecha de haber contraído esta enfermedad.
- En casa es complicado detectarse nada y mucho menos diagnosticarse a uno mismo, pero sí podemos percibir sangre en las heces o un bulto en la mama, por ejemplo. Eso no quiere decir que por tener ese síntoma la persona tenga cáncer. Será el especialista el que lo averigüe y el que haga el diagnóstico. Creo que también hay que insistir en eso, que un síntoma no es un cáncer.
...
Una terapia génica puede mejorar la supervivencia al cáncer de ovario .
Madrid, 27 jul (EFE).-
El uso una terapia génica para administrar una proteína que suprime el desarrollo de los órganos reproductivos femeninos pude mejorar la supervivencia de mujeres con cáncer recurrente de ovario tal y como se ha probado en ratones, señala un estudio publicado hoy por PNAS.
Expertos del estadounidense Hospital General de Massachusetts lograron eliminar en ratones el crecimiento de tumores de ovario resistentes a la quimioterapia, para lo que les inyectaron una versión modificada de una proteína, la MIS, imprescindible para el desarrollo sexual.
Aunque no todos los tumores en los que se ensayó -crecidos a partir de células injertadas de pacientes- respondieron al tratamiento, los investigadores también han descrito una manera no invasiva de examinar células cancerosas "in vitro".
"Nuestros descubrimientos son importantes por en la actualidad no hay opciones terapéuticas para los cánceres de ovario recurrentes y resistentes a la quimioterapía", indicó David Pepin, autor principal del estudio.
...
El uso una terapia génica para administrar una proteína que suprime el desarrollo de los órganos reproductivos femeninos pude mejorar la supervivencia de mujeres con cáncer recurrente de ovario tal y como se ha probado en ratones, señala un estudio publicado hoy por PNAS.
Expertos del estadounidense Hospital General de Massachusetts lograron eliminar en ratones el crecimiento de tumores de ovario resistentes a la quimioterapia, para lo que les inyectaron una versión modificada de una proteína, la MIS, imprescindible para el desarrollo sexual.
Aunque no todos los tumores en los que se ensayó -crecidos a partir de células injertadas de pacientes- respondieron al tratamiento, los investigadores también han descrito una manera no invasiva de examinar células cancerosas "in vitro".
"Nuestros descubrimientos son importantes por en la actualidad no hay opciones terapéuticas para los cánceres de ovario recurrentes y resistentes a la quimioterapía", indicó David Pepin, autor principal del estudio.
...
EEUU investiga una denuncia sobre casos de cáncer entre el personal de la prisión de Guantánamo .
NUEVA YORK, 28 Jul. (Reuters/EP) -
La Marina de Estados Unidos está investigando una denuncia que busca la evacuación de abogados civiles y militares de partes de la base del país en la Bahía de Guantánamo, Cuba, tras las informaciones sobre casos de cáncer entre el personal que trabaja en los juicios de detenidos en ese lugar.
Al menos a siete miembros civiles y militares que trabajaron en juicios de detenidos en prisión han sido diagnosticados con cáncer, según la denuncia, presentada ante la Oficina del Inspector General del Departamento de Defensa de Estados Unidos.
La queja pide a los oficiales militares estadounidenses que retiren al personal de las instalaciones de la corte y que se les realicen pruebas en busca de agentes cancerígenos en la propia base.
La denuncia asegura que un número inusualmente alto de personas relativamente sanas y jóvenes que trabajaron en la base ha sido diagnosticada con cáncer. En la última década, casi 200 fiscales, abogados defensores y otros funcionarios judiciales han trabajado en la base.
La denuncia dice que los pacientes pudieron haber estado expuestos a agentes cancerígenos cuando vivieron y trabajaron en un lugar de Guantánamo que fue anteriormente utilizado para almacenar combustible de aviones, ubicado cerca de una pista de aterrizaje abandonada.
...
La Marina de Estados Unidos está investigando una denuncia que busca la evacuación de abogados civiles y militares de partes de la base del país en la Bahía de Guantánamo, Cuba, tras las informaciones sobre casos de cáncer entre el personal que trabaja en los juicios de detenidos en ese lugar.
Al menos a siete miembros civiles y militares que trabajaron en juicios de detenidos en prisión han sido diagnosticados con cáncer, según la denuncia, presentada ante la Oficina del Inspector General del Departamento de Defensa de Estados Unidos.
La queja pide a los oficiales militares estadounidenses que retiren al personal de las instalaciones de la corte y que se les realicen pruebas en busca de agentes cancerígenos en la propia base.
La denuncia asegura que un número inusualmente alto de personas relativamente sanas y jóvenes que trabajaron en la base ha sido diagnosticada con cáncer. En la última década, casi 200 fiscales, abogados defensores y otros funcionarios judiciales han trabajado en la base.
La denuncia dice que los pacientes pudieron haber estado expuestos a agentes cancerígenos cuando vivieron y trabajaron en un lugar de Guantánamo que fue anteriormente utilizado para almacenar combustible de aviones, ubicado cerca de una pista de aterrizaje abandonada.
...
El lado oscuro del ADN potencia el cáncer .
* Un consorcio español secuencia el genoma de 500 pacientes y desvela que una de cada cinco leucemias se debe a mutaciones en el mal llamado 'ADN basura' .
* La ‘basura’ genética se convierte en un arma contra el cáncer .
Nuño Domínguez 27 JUL 2015 -
En el interior de cada una de sus células hay descomunales extensiones genéticas sin explorar. Se trata del llamado ADN oscuro, antes conocido como basura, y que compone hasta el 98% de todo el genoma. Estos vastos jardines sin aurora habían sido poco interesantes para los científicos porque no contienen genes y, por tanto, no producen proteínas. Es por eso que se pensó erróneamente que no tenían ninguna importancia para entender las claves de la salud y la enfermedad. Pero eso se acabó.
En 2012, un consorcio internacional demostró que el ADN basura regula funciones fisiológicas y puede contribuir a la aparición de muchas enfermedades, desde la diabetes a la esclerósis múltiple pasando por el cáncer. En un estudio publicado hoy en Nature, un consorcio español demuestra que ese ADN oscuro tiene un papel clave en la aparición de la leucemia linfática crónica, la forma de cáncer sanguíneo más común.
...
* La ‘basura’ genética se convierte en un arma contra el cáncer .
Nuño Domínguez 27 JUL 2015 -
En el interior de cada una de sus células hay descomunales extensiones genéticas sin explorar. Se trata del llamado ADN oscuro, antes conocido como basura, y que compone hasta el 98% de todo el genoma. Estos vastos jardines sin aurora habían sido poco interesantes para los científicos porque no contienen genes y, por tanto, no producen proteínas. Es por eso que se pensó erróneamente que no tenían ninguna importancia para entender las claves de la salud y la enfermedad. Pero eso se acabó.
En 2012, un consorcio internacional demostró que el ADN basura regula funciones fisiológicas y puede contribuir a la aparición de muchas enfermedades, desde la diabetes a la esclerósis múltiple pasando por el cáncer. En un estudio publicado hoy en Nature, un consorcio español demuestra que ese ADN oscuro tiene un papel clave en la aparición de la leucemia linfática crónica, la forma de cáncer sanguíneo más común.
...
26 julio 2015
Dr. George D. Demetri on Trabectedin for Sarcomas : Yondelis Ha Demostrado Muy Buenas Respuestas y Estabilidad Duradera de la Enfermedad que se Prolonga Incluso de 4 a 5 Años .
"" The sarcoma community is particularly interested in this drug because it has been showed to produce extremely good response and durable disease stability, sometimes lasting four to five years, said Demetri "".
OncLiveTV /// Publicado el 24 jul. 2015 .
George D. Demetri, MD, Director, Center for Sarcoma and Bone Oncology Senior Vice President for Experimental Therapeutics, Professor of Medicine, Harvard Medical School, Dana Farber Cancer Center, discusses a phase III study of trabectedin verus dacarbazine for the treatment of patients with advanced liposarcoma (LPS) or leiomyosarcoma (LMS).
Trabectedin is a multifunctional drug derived from a sea squirt, which is now manufactured synthetically. The sarcoma community is particularly interested in this drug because it has been showed to produce extremely good response and durable disease stability, sometimes lasting four to five years, said Demetri.
However, there is no predictive biomarker to determine which patients will benefit from this drug. The aim of the study was to determine which patients responded more favorably to trabectedin versus the standard of care dacarbazine.
The study is ongoing, however an interim analysis presented at ASCO 2015, showed that trabectedin had a significant benefit over dacarbazine in terms of disease control and progression-free survival.
25 julio 2015
Científicos Revelan por qué el Cáncer se hace más Invencible .
24 jul 2015 /// Eric Gaillard / Reuters .
El envejecimiento y los malos hábitos debilitan el organismo humano y permiten al cáncer triunfar sobre el tejido sano: esta es la razón principal de la formación de tumores malignos y no la mutación genética, revela una nueva teoría confirmada experimentalmente por científicos de EE.UU. Para explicar su hipótesis, han recurrido a una comparación inusual del cuerpo humano con el medioambiente, y nuestras células con los dinosaurios.
El hecho de que hace 65 millones de años los dinosaurios se extinguieron no significa que se volvieron más débiles o menos aptos para la vida, o que los mamíferos de alguna manera les ganaron. Debido al supuesto impacto de un meteorito se alteró su hábitat, lo cual fue un impulso natural para un cambio del "líder". Procesos similares ocurren en el cuerpo humano: como resultado del envejecimiento y los hábitos nocivos el estado de los tejidos sanos se deteriora y en algún momento el cuerpo se rinde ante las células cancerígenas que resultan ser más fuertes, opinan los científicos Andrii I. Rozhok y James DeGregori de la Facultad de Medicina de la Universidad de Colorado en Denver, en su estudio publicado en la revista 'PNAS'.
...
El envejecimiento y los malos hábitos debilitan el organismo humano y permiten al cáncer triunfar sobre el tejido sano: esta es la razón principal de la formación de tumores malignos y no la mutación genética, revela una nueva teoría confirmada experimentalmente por científicos de EE.UU. Para explicar su hipótesis, han recurrido a una comparación inusual del cuerpo humano con el medioambiente, y nuestras células con los dinosaurios.
El hecho de que hace 65 millones de años los dinosaurios se extinguieron no significa que se volvieron más débiles o menos aptos para la vida, o que los mamíferos de alguna manera les ganaron. Debido al supuesto impacto de un meteorito se alteró su hábitat, lo cual fue un impulso natural para un cambio del "líder". Procesos similares ocurren en el cuerpo humano: como resultado del envejecimiento y los hábitos nocivos el estado de los tejidos sanos se deteriora y en algún momento el cuerpo se rinde ante las células cancerígenas que resultan ser más fuertes, opinan los científicos Andrii I. Rozhok y James DeGregori de la Facultad de Medicina de la Universidad de Colorado en Denver, en su estudio publicado en la revista 'PNAS'.
...
24 julio 2015
Aplidin , Segundo Farmaco de PharmaMar , Salta una Vez Más a los Titulares Oncologicos Mundiales . Siete Puntos a tener en Cuenta que dan a Pensar que lo Mejor de este Farmaco esta por Llegar .
Pharma Jonpi , 24 Julio 2015 .
1º .- Junio de 2015 - PharmaMar Anunciaba que el reclutamiento de pacientes del ensayo pivotal de Fase III con APLIDIN® (plitidepsin) para el tratamiento del mieloma múltiple, denominado ADMYRE, se ha completado con éxito. El estudio, para el que se había previsto en un inicio incluir 250 pacientes, han reclutado 255 pacientes en 71 centros médicos en todo el mundo, incluyendo EE.UU., Europa, Asia, Australia y Nueva Zelanda. La presentación de la solicitud de autorización de comercialización en Europa está prevista en 2016.
*- ADMYRE es un estudio prospectivo, de registro, randomizado (2:1), abierto y multicéntrico que compara plitidepsin en combinación con dexametasona frente dexametasona como tratamiento único en pacientes con mieloma múltiple refractario o que han recaído después de, al menos, tres tratamientos previos, pero no más de seis. Los pacientes deben haber recibido previamente tratamiento con bortezomib y lenalidomida.
*.- En un análisis interino llevado a cabo por el Comité Independiente de Monitorización de Datos (IDMC por sus siglas en inglés) se recomendó la finalización del ensayo de Fase III (ADMYRE) sin modificaciones ya que no se reportaron problemas de seguridad y que se superó con holgura el nivel mínimo de eficacia exigido tras la evaluación de los datos de 60 pacientes evaluables
**************************************
2º .- Julio 2014 llegaba el Primer Acuerdo de Comercialización alcanzado con Chugai Pharma que bien sabida es su relación con el Gigante Suizo Roche :
Según se establece en los términos del acuerdo, PharmaMar recibe un pago inicial de 5 millones de euros por la firma del acuerdo; se contemplan asimismo pagos adicionales que podrían alcanzar una cifra total de más de 30 millones de euros si se consiguen determinados hitos relativos al desarrollo del compuesto así como otros objetivos regulatorios y comerciales referentes al mismo.
*.- Zeltia y Chugai Pharmaceutical Co., Ltd. han anunciado que PharmaMar SA, filial oncológica íntegramente participada por Zeltia, y Chugai Pharma Marketing Ltd, participada íntegramente por Chugai Pharmaceutical Co., Ltd, han firmado un acuerdo de licencia en función del cual Chugai Pharma Marketing comercializaría Aplidin®, producto de PharmaMar para el tratamiento de mieloma múltiple, en ocho países europeos(Francia, Alemania, Reino Unido, Benelux, Irlanda y Austria).
*.- PharmaMar mantendrá los derechos de producción en exclusiva y venderá el producto a Chugai para su comercialización en los territorios objeto del acuerdo.
****************************************
3º .- 23 Julio del 2015 llega el Segundo acuerdo de licencia y comercialización de su compuesto antitumoral Aplidin con TTY Biopharm en Taiwán.
*.- Pharmamar recibirá un pago por adelantado por la firma del acuerdo, pagos recurrentes por ventas, y remuneraciones adicionales por los hitos regulatorios alcanzados por el fármaco, cuyo principio activo es la plitidepsina.
*.- Un acuerdo que bien podría abrir la puerta a la consecución de mas acuerdos en el area Asiatica ... con China // Japón a la Cabeza .
*****************************************
4º .- Aplidin según los resultados presentados en los últimos congresos esta demostrando que es un “first in class drug” destacando por primera vez su mecanismo de acción que muestra que su diana terapéutica en las células tumorales es la proteína eEF1a .
*****************************************
5º .- La Food and Drug Administration (FDA) ha aceptado la propuesta de PharmaMar sobre el proceso de producción del fármaco.
*****************************************
6º .- Aplidin® Tiene el Status de Fármaco Huérfano por la Comisión Europea (CE) y la FDA para Mieloma Múltiple (MM).
*****************************************
7º .- Aplidin Nano-Encapsulada ... Mucho Mejor ya que va dirijida directamente al Tumor .
*****************************************
8º .- Una vez terminada la Fase III para el tratamiento de Mieloma Multiple se esta ya elaborando el Dossier el cual podria ser presentado este mismo año o a principios del 2016 y de ser aprobado podría ser el Segundo Farmaco de Pharma Mar en salir al Mercado .
1º .- Junio de 2015 - PharmaMar Anunciaba que el reclutamiento de pacientes del ensayo pivotal de Fase III con APLIDIN® (plitidepsin) para el tratamiento del mieloma múltiple, denominado ADMYRE, se ha completado con éxito. El estudio, para el que se había previsto en un inicio incluir 250 pacientes, han reclutado 255 pacientes en 71 centros médicos en todo el mundo, incluyendo EE.UU., Europa, Asia, Australia y Nueva Zelanda. La presentación de la solicitud de autorización de comercialización en Europa está prevista en 2016.
*- ADMYRE es un estudio prospectivo, de registro, randomizado (2:1), abierto y multicéntrico que compara plitidepsin en combinación con dexametasona frente dexametasona como tratamiento único en pacientes con mieloma múltiple refractario o que han recaído después de, al menos, tres tratamientos previos, pero no más de seis. Los pacientes deben haber recibido previamente tratamiento con bortezomib y lenalidomida.
*.- En un análisis interino llevado a cabo por el Comité Independiente de Monitorización de Datos (IDMC por sus siglas en inglés) se recomendó la finalización del ensayo de Fase III (ADMYRE) sin modificaciones ya que no se reportaron problemas de seguridad y que se superó con holgura el nivel mínimo de eficacia exigido tras la evaluación de los datos de 60 pacientes evaluables
**************************************
2º .- Julio 2014 llegaba el Primer Acuerdo de Comercialización alcanzado con Chugai Pharma que bien sabida es su relación con el Gigante Suizo Roche :
Según se establece en los términos del acuerdo, PharmaMar recibe un pago inicial de 5 millones de euros por la firma del acuerdo; se contemplan asimismo pagos adicionales que podrían alcanzar una cifra total de más de 30 millones de euros si se consiguen determinados hitos relativos al desarrollo del compuesto así como otros objetivos regulatorios y comerciales referentes al mismo.
*.- Zeltia y Chugai Pharmaceutical Co., Ltd. han anunciado que PharmaMar SA, filial oncológica íntegramente participada por Zeltia, y Chugai Pharma Marketing Ltd, participada íntegramente por Chugai Pharmaceutical Co., Ltd, han firmado un acuerdo de licencia en función del cual Chugai Pharma Marketing comercializaría Aplidin®, producto de PharmaMar para el tratamiento de mieloma múltiple, en ocho países europeos(Francia, Alemania, Reino Unido, Benelux, Irlanda y Austria).
*.- PharmaMar mantendrá los derechos de producción en exclusiva y venderá el producto a Chugai para su comercialización en los territorios objeto del acuerdo.
****************************************
3º .- 23 Julio del 2015 llega el Segundo acuerdo de licencia y comercialización de su compuesto antitumoral Aplidin con TTY Biopharm en Taiwán.
*.- Pharmamar recibirá un pago por adelantado por la firma del acuerdo, pagos recurrentes por ventas, y remuneraciones adicionales por los hitos regulatorios alcanzados por el fármaco, cuyo principio activo es la plitidepsina.
*.- Un acuerdo que bien podría abrir la puerta a la consecución de mas acuerdos en el area Asiatica ... con China // Japón a la Cabeza .
*****************************************
4º .- Aplidin según los resultados presentados en los últimos congresos esta demostrando que es un “first in class drug” destacando por primera vez su mecanismo de acción que muestra que su diana terapéutica en las células tumorales es la proteína eEF1a .
*****************************************
5º .- La Food and Drug Administration (FDA) ha aceptado la propuesta de PharmaMar sobre el proceso de producción del fármaco.
*****************************************
6º .- Aplidin® Tiene el Status de Fármaco Huérfano por la Comisión Europea (CE) y la FDA para Mieloma Múltiple (MM).
*****************************************
7º .- Aplidin Nano-Encapsulada ... Mucho Mejor ya que va dirijida directamente al Tumor .
*****************************************
8º .- Una vez terminada la Fase III para el tratamiento de Mieloma Multiple se esta ya elaborando el Dossier el cual podria ser presentado este mismo año o a principios del 2016 y de ser aprobado podría ser el Segundo Farmaco de Pharma Mar en salir al Mercado .
23 julio 2015
Primera extracción en España de un tumor pulmonar marcado con radiotrazador .
MADRID, 23 Jul. (EUROPA PRESS) -
El Hospital Universitario Quirón Madrid ha realizado la primera extracción en España de un tumor pulmonar marcado con radiotrazador a través del robot quirúrgico 'Da Vinci', lo que reduce las incisiones que sufre el paciente y acelera su recuperación.
Las lesiones tumorales en los pulmones son en ocasiones difícilmente localizables en quirófano porque no son visibles y, a veces, tampoco palpables. Para que la parte del pulmón que se pierda sea la menor posible, en este centro se ha practicado un marcaje radioactivo del tumor, de modo que sea localizado con más facilidad durante la cirugía a través de una gamma-sonda.
"El marcaje con radiotrazador delimita la lesión con una precisión de un centímetro, de modo que se hacen extirpaciones conservadoras y se sacrifica la mínima parte de tejido pulmonar", ha explicado Javier Moradiellos, jefe asociado del servicio de Cirugía Torácica de Hospital Universitario Quirón Madrid.
...
El Hospital Universitario Quirón Madrid ha realizado la primera extracción en España de un tumor pulmonar marcado con radiotrazador a través del robot quirúrgico 'Da Vinci', lo que reduce las incisiones que sufre el paciente y acelera su recuperación.
Las lesiones tumorales en los pulmones son en ocasiones difícilmente localizables en quirófano porque no son visibles y, a veces, tampoco palpables. Para que la parte del pulmón que se pierda sea la menor posible, en este centro se ha practicado un marcaje radioactivo del tumor, de modo que sea localizado con más facilidad durante la cirugía a través de una gamma-sonda.
"El marcaje con radiotrazador delimita la lesión con una precisión de un centímetro, de modo que se hacen extirpaciones conservadoras y se sacrifica la mínima parte de tejido pulmonar", ha explicado Javier Moradiellos, jefe asociado del servicio de Cirugía Torácica de Hospital Universitario Quirón Madrid.
...
PharmaMar Firma un Acuerdo de Licencia y Comercialización Para APLIDIN® con TTY Biopharm en Oncología .
PharmaMar announces license agreement with TTY Biopharm for APLIDIN® (plitidepsin) in hematological cancers .
Madrid, 23 de julio de 2015 -
PharmaMar ha Anunciado hoy un Acuerdo de licencia con la farmacéutica TTY Biopharm para comercializar el compuesto antitumoral de origen marino APLIDIN® (plitidepsina) en Taiwan.
Según los términos del acuerdo, PharmaMar recibirá un pago por adelantado por la firma del acuerdo, pagos recurrentes por ventas, y remuneraciones adicionales por los hitos regulatorios alcanzados por APLIDIN® (plitidepsina). PharmaMar conservará los derechos de producción en exclusiva y suministrará el producto a TTY Biopharm para su uso comercial en Taiwan.
APLIDIN® (plitidepsina) es el segundo fármaco antitumoral obtenido de un organismo marino que desarrolla PharmaMar y el cual se encuentra actualmente en fase de desarrollo para el tratamiento del mieloma múltiple y un tipo de linfoma de células T. La compañía anunció en junio que el reclutamiento de pacientes del ensayo pivotal de fase III internacional (ADMYRE) de APLIDIN® (plitidepsina) para el tratamiento de mieloma múltiple refractario o en recaída se completó con éxito[i]
"Hay miles de pacientes que viven con esta enfermedad y es parte de nuestro compromiso y dedicación el llevar este nuevo fármaco first-in-class hasta aquellos que lo necesitan. Estamos encantados de colaborar con uno de los líderes de gran tradición en el campo de la oncología y la hematología en Taiwán para poder conseguirlo". dijo Heiner Pieper, Vicepresidente de Desarrollo de Negocios y Licencias de PharmaMar.
"Nuestro conocimiento del mercado asiático y nuestra capacidad para comercializar plitidepsina junto con el valor terapéutico de este innovador compuesto representan factores importantes para el éxito de esta colaboración”, dijo Hsiao Ying- Chun , Presidente de TTY Biopharm. “Esperamos poder contribuir al bienestar de estos pacientes al proporcionar a los médicos un fármaco novedoso".
Sobre TTY Biopharm :
TTY está comprometido a establecerse como una compañía farmacéutica biotecnológica enfocada en el desarrollo de fármacos y la comercialización internacional. Por un lado, TTY continúa mejorando su capacidad de desarrollar proyectos de ámbito internacional como los formatos internacionales de documentación técnica (CMC, CTD), ejecución de ensayos clínicos a nivel global y procesos de fabricación siguiendo las especificaciones de la EMEA y FDA. Por otro lado, TTY establece alianzas con los socios de colaboración más adecuados para el desarrollo de nuevos medicamentos en todo el mundo y en diversos mercados. Aparte de operación de manera continuada en las áreas centrales (centros médicos, hospitales regionales y hospitales de distrito con potenciales de desarrollo) en Taiwán, TTY entrará en el mercado internacional mediante el desarrollo de nuevos fármacos con prueba de concepto y medicamentos biológicos de formulaciones innovadoras con liposomas inyectables y microesferas PLA / PLGA. Actualmente, TTY ha tenido éxito en la introducción de sus propios productos de investigación y desarrollo en regiones como la Unión Europea, el Asia Pacífico, las regiones de Medio Oriente, África y América del Sur, y se ha convertido en el mejor aliado para las empresas que son fuertes en la comercialización de medicamentos. En el futuro, TTY continuará su trabajo en los mercados de Asia (mercado interno) para desarrollar su fuerza local para convertirse en el principal socio con las mejores capacidades de desarrollo de fármacos y de marketing para las empresas internacionales de innovación y de biotecnología en el mercado.
Madrid, 23 de julio de 2015 -
PharmaMar ha Anunciado hoy un Acuerdo de licencia con la farmacéutica TTY Biopharm para comercializar el compuesto antitumoral de origen marino APLIDIN® (plitidepsina) en Taiwan.
Según los términos del acuerdo, PharmaMar recibirá un pago por adelantado por la firma del acuerdo, pagos recurrentes por ventas, y remuneraciones adicionales por los hitos regulatorios alcanzados por APLIDIN® (plitidepsina). PharmaMar conservará los derechos de producción en exclusiva y suministrará el producto a TTY Biopharm para su uso comercial en Taiwan.
APLIDIN® (plitidepsina) es el segundo fármaco antitumoral obtenido de un organismo marino que desarrolla PharmaMar y el cual se encuentra actualmente en fase de desarrollo para el tratamiento del mieloma múltiple y un tipo de linfoma de células T. La compañía anunció en junio que el reclutamiento de pacientes del ensayo pivotal de fase III internacional (ADMYRE) de APLIDIN® (plitidepsina) para el tratamiento de mieloma múltiple refractario o en recaída se completó con éxito[i]
"Hay miles de pacientes que viven con esta enfermedad y es parte de nuestro compromiso y dedicación el llevar este nuevo fármaco first-in-class hasta aquellos que lo necesitan. Estamos encantados de colaborar con uno de los líderes de gran tradición en el campo de la oncología y la hematología en Taiwán para poder conseguirlo". dijo Heiner Pieper, Vicepresidente de Desarrollo de Negocios y Licencias de PharmaMar.
"Nuestro conocimiento del mercado asiático y nuestra capacidad para comercializar plitidepsina junto con el valor terapéutico de este innovador compuesto representan factores importantes para el éxito de esta colaboración”, dijo Hsiao Ying- Chun , Presidente de TTY Biopharm. “Esperamos poder contribuir al bienestar de estos pacientes al proporcionar a los médicos un fármaco novedoso".
Sobre TTY Biopharm :
TTY está comprometido a establecerse como una compañía farmacéutica biotecnológica enfocada en el desarrollo de fármacos y la comercialización internacional. Por un lado, TTY continúa mejorando su capacidad de desarrollar proyectos de ámbito internacional como los formatos internacionales de documentación técnica (CMC, CTD), ejecución de ensayos clínicos a nivel global y procesos de fabricación siguiendo las especificaciones de la EMEA y FDA. Por otro lado, TTY establece alianzas con los socios de colaboración más adecuados para el desarrollo de nuevos medicamentos en todo el mundo y en diversos mercados. Aparte de operación de manera continuada en las áreas centrales (centros médicos, hospitales regionales y hospitales de distrito con potenciales de desarrollo) en Taiwán, TTY entrará en el mercado internacional mediante el desarrollo de nuevos fármacos con prueba de concepto y medicamentos biológicos de formulaciones innovadoras con liposomas inyectables y microesferas PLA / PLGA. Actualmente, TTY ha tenido éxito en la introducción de sus propios productos de investigación y desarrollo en regiones como la Unión Europea, el Asia Pacífico, las regiones de Medio Oriente, África y América del Sur, y se ha convertido en el mejor aliado para las empresas que son fuertes en la comercialización de medicamentos. En el futuro, TTY continuará su trabajo en los mercados de Asia (mercado interno) para desarrollar su fuerza local para convertirse en el principal socio con las mejores capacidades de desarrollo de fármacos y de marketing para las empresas internacionales de innovación y de biotecnología en el mercado.
Investigadores españoles descifran el genoma de la leucemia linfática crónica .
El Confidencial /// 23.07.2015 .
Investigadores españoles han sido los primeros en descifrar el genoma de más de 500 pacientes con leucemia linfática crónica, consiguiendo identificar hasta 60 genes distintos cuyas mutaciones -dos de ellas en el 'lado oscuro' del genoma- son responsables del 90 por ciento de los cáncer de este tipo, lo que supone una "revolución" que permitirá "cambiar" la forma de tratar a estos pacientes.
El trabajo, que ha sido publicado este miércoles por la revista Nature, supone un hito en la investigación en España, y en el mundo, ya que forma parte del mayor proyecto internacional para el estudio del genoma del cáncer, el Consorcio Internacional del Genoma de Cáncer (ICGC), que tiene como objetivo descifrar, para cada uno de los 50 tipos de cáncer más frecuentes, el genoma de las células tumorales de al menos 500 pacientes.
"Es la primera vez que se consigue hacer una cosa así", explica el profesor Xose Suárez Puente, investigador de la Universidad de Oviedo y primer firmante del artículo de esta investigación, que está dirigida por los doctores Carlos López-Otín, de la Universidad de Oviedo, y Elías Campo, del Hospital Clínic y la Universidad de Barcelona.
...
Investigadores españoles han sido los primeros en descifrar el genoma de más de 500 pacientes con leucemia linfática crónica, consiguiendo identificar hasta 60 genes distintos cuyas mutaciones -dos de ellas en el 'lado oscuro' del genoma- son responsables del 90 por ciento de los cáncer de este tipo, lo que supone una "revolución" que permitirá "cambiar" la forma de tratar a estos pacientes.
El trabajo, que ha sido publicado este miércoles por la revista Nature, supone un hito en la investigación en España, y en el mundo, ya que forma parte del mayor proyecto internacional para el estudio del genoma del cáncer, el Consorcio Internacional del Genoma de Cáncer (ICGC), que tiene como objetivo descifrar, para cada uno de los 50 tipos de cáncer más frecuentes, el genoma de las células tumorales de al menos 500 pacientes.
"Es la primera vez que se consigue hacer una cosa así", explica el profesor Xose Suárez Puente, investigador de la Universidad de Oviedo y primer firmante del artículo de esta investigación, que está dirigida por los doctores Carlos López-Otín, de la Universidad de Oviedo, y Elías Campo, del Hospital Clínic y la Universidad de Barcelona.
...
Zeltia , Su Filial Biotecnologica Genómica SAU y la Fundación ECO Anuncian Un Acuerdo Marco de Colaboración en Oncología .
Este convenio busca promover la calidad de la atención oncológica en España mediante el fomento de proyectos de investigación, el uso optimizado de las técnicas de diagnóstico de GENOMICA, la divulgación científica y la formación de oncólogos .
Madrid, 22 de Julio de 2015 –
GENOMICA, empresa española líder en el diagnóstico molecular ha entrado en un acuerdo marco de colaboración con la Fundación para la Excelencia y Calidad en la Oncología (Fundación ECO) centrado en mejorar el tratamiento del cáncer fomentando proyectos de investigación y la optimización de la gestión clínica en oncología.
Este acuerdo es el primero llevado a cabo entre una empresa de biotecnología española y la prestigiosa Fundación. El fin de esta colaboración es fortalecer la actividad que realiza GENOMICA para facilitar herramientas de diagnóstico molecular fiables y optimizadas en la práctica clínica y estar alineado con los objetivos de la Fundación ECO para impulsar avances en la Oncología española y, así, ofrecer a los pacientes los mejores recursos.
Entre las diferentes actividades que se llevarán a cabo con este acuerdo, GENOMICA y la Fundación ECO se comprometen a promover proyectos y estudios de investigación centrados en la salud, cursos de formación y conferencias, foros de divulgación científica, así como la publicación de artículos científicos.
"Estamos orgullosos de comenzar esta colaboración con la Fundación ECO, la cual será clave para iniciar distintos proyectos centrados en el diagnóstico molecular con servicios de oncología médica de toda España", dijo Rosario Cospedal, Directora General de GENOMICA. "Nuestro objetivo es poder compartir con los oncólogos y los investigadores nuestra experiencia en detección de biomarcadores con la tecnología CLART® para llevar a cabo nuevos estudios que mejoren la calidad del diagnóstico y asistencia a los pacientes oncológicos.”
El presidente de la Fundación ECO, el doctor Vicente Guillem, se mostró muy satisfecho por el acuerdo firmado, el cual permitirá intensificar los trabajos de la entidad en el campo de los análisis genéticos y la medicina de precisión en Oncología. La Fundación ECO ha realizado varias iniciativas científicas en esta línea, las cuales considera una vía clave para el futuro en el tratamiento del cáncer. Con el objetivo de promover pautas para mejorar la calidad de la Oncología española desde todas sus vertientes, “este convenio permitirá abrir nuevos foros de debate y análisis que nos permitan avanzar en la nueva era de la medicina personalizada”, indicó el prestigioso oncólogo, el Dr. Guillem.
En la imagen: Dr. Vicente Guillem, Presidente de la Fundación ECO; y Rosario Cospedal, Directora General de GENOMICA.
**************************************
Sobre GENOMICA :
GENOMICA es la primera compañía española en diagnóstico molecular y con gran experiencia en la realización de análisis de Identificación Genética. Fundada en 1990, se ubica en la Comunidad de Madrid y está participada al 100% por Zeltia (ZEL). Nuestra misión es mejorar los métodos actuales de diagnóstico molecular e identificación genética con herramientas fiables, automáticas y de acuerdo a los más altos estándares de calidad. El principal objetivo de la compañía es continuar liderando las aplicaciones genómicas en el mercado español y extender internacionalmente nuestras actividades en el área del diagnóstico molecular, mediante el diseño, desarrollo y comercialización de nuevas aplicaciones diagnósticas de nuestra innovadora plataforma tecnológica CLINICAL ARRAYS TECHNOLOGY, CLART®. GENOMICA ha desarrollado tests de diagnóstico de numerosas enfermedades infecciosas y varios tipos de tumores así como tests para la detección de regiones génicas en humanos asociadas a respuestas a terapias, en concreto en el campo de la oncología. Otro campo donde GENOMICA apuesta con fuerza, es llevando a cabo servicios de análisis de ADN en Medicina Legal y Forense, y en transferencia de tecnología. Para más información, visite nuestra web: http://www.genomica.es.
Sobre la Fundación ECO :
Fundación ECO es una plataforma de expertos formada por jefes de servicio oncología médica de los principales hospitales españoles. Está orientada a conseguir la excelencia y la calidad en la Oncología, buscando y desarrollando soluciones y herramientas que permitan conseguir este fin. Así, esta red de expertos, fomenta la calidad en tres ámbitos: asistencia al paciente, tanto recibida como percibida, formación especializada e impulso de la investigación.
22 julio 2015
Yondelis Meningioma . EORTC ( European Organisation for Research and Treatment of Cancer ) Ya Ha Iniciado la Fase II con Trabectedin for Recurrent Grade II or III Meningioma : A Randomized Phase II Study of the EORTC Brain Tumor Group . Son ya Varios los Paises Europeos Que Han Autorizado Dicho Ensayo .
P.J. : Emerging clinical studies will evaluate novel medical treatment approaches including the tetra-hydroisoquinoline alkaloid Yondelis (European Organisation for Research and Treatment of Cancer (EORTC) phase II trial 1320) and SMO or AKT inhibitors in molecularly selected cases.
************************************
ClinicalTrials Identifier: NCT02234050 /// Updated: 2015_07_16 .
Descriptive Information :
Brief title : Trabectedin for Recurrent Grade II/III Meningioma .
Official title : Trabectedin for Recurrent Grade II or III Meningioma: a Randomized Phase II Study of the EORTC Brain Tumor Group
Brief summary :
The aim of this study is to collect data on activity, toxicity and quality of life of trabectedin therapy in patients with recurrent high-grade meningioma.
Detailed description :
This is a randomized open label multicenter comparative phase II trial.
The objective of the study is to investigate whether trabectedin demonstrates sufficient antitumor activity against recurrent grade II or III to justify further investigation in phase III or as adjuvant therapy for newly diagnosed disease after resection and radiotherapy.
***************************************
Recruitment Information :
Status : Recruiting
Start date : 2015-07
Primary completion date : 2017-07 (Anticipated)
***************************************
Administrative Data :
Organization name European Organisation for Research and Treatment of Cancer - EORTC
Organization study ID EORTC-1320 .
Sponsor : European Organisation for Research and Treatment of Cancer - EORTC .
Health Authority Austria: Austrian Medicines and Medical Devices Agency .
Health Authority Belgium: Federal Agency for Medicinal Products and Health Products .
Health Authority France: Committee for the Protection of Personnes .
Health Authority Germany: Paul-Ehrlich-Institut .
Health Authority Italy: The Italian Medicines Agency .
Health Authority Switzerland: Federal Office of Public Health .
Health Authority United Kingdom: Medicines and Healthcare Products Regulatory Agency .
Health Authority Netherlands: The Central Committee on Research Involving Human Subjects (CCMO).
Abby de cuatro años, cumplió su sueño de casarse con su enfermero favorito, Matt Hiclkling .
Para los que alcanzaron a entrar en pánico, calma, esta es una historia de esas que tienen una esencia feliz. Esperamos de corazón que el final sea igual de alegre.
Abby está luchando contra las células pre-B de una leucemia linfoblástica aguda, que es una forma de leucemia que afecta principalmente a los niños.
Ella es Abby de Nueva York y tiene 4 añotes de edad ¡Casi toda una Mujercita !! .
Actualmente Abby es una paciente del Centro Melodies que se especializa en el cáncer infantil, ubicado en Albany, Nueva York. Pero ella siempre mantiene una perspectiva positiva mientras lucha como toda una guerrera contra una enfermedad sacaría corriendo de miedo a más de uno.
Como imaginarán, Abby empezó a hacer muchos amigos, entre esos su enfermero Matt Hickling, con quien desarrolló una dulce y bella relación de amistad.
Así que sin más miramientos a principios de esta semana, Abby le dijo a su mamá que planeaba casarse con Hickling a su próxima cita.
Así que el miércoles, su madre lo llamó y le contó sobre la proposición de Abby. Naturalmente, Hickling aceptó y de inmediato empezaron junto con su madre a planear esta bella boda.
Abby llevaba un hermoso vestido de princesa y como es normal en todas las novias, un lindo ramo de flores en su mano. Pero Matt no se quedó atrás, llevaba una elegante camisa de esmoquin bastante cool.
Después de este maravilloso evento, “el novio” escribió acerca de la boda en un post de Facebook:
“¡Espero que este día sea para nuestra paciente y su familia uno en el que puedan mirar hacia atrás y sonreír cuando los días sean duros! ¡Sé que así será!”
Abby está luchando contra las células pre-B de una leucemia linfoblástica aguda, que es una forma de leucemia que afecta principalmente a los niños.
Ella es Abby de Nueva York y tiene 4 añotes de edad ¡Casi toda una Mujercita !! .
Actualmente Abby es una paciente del Centro Melodies que se especializa en el cáncer infantil, ubicado en Albany, Nueva York. Pero ella siempre mantiene una perspectiva positiva mientras lucha como toda una guerrera contra una enfermedad sacaría corriendo de miedo a más de uno.
Como imaginarán, Abby empezó a hacer muchos amigos, entre esos su enfermero Matt Hickling, con quien desarrolló una dulce y bella relación de amistad.
Así que sin más miramientos a principios de esta semana, Abby le dijo a su mamá que planeaba casarse con Hickling a su próxima cita.
Así que el miércoles, su madre lo llamó y le contó sobre la proposición de Abby. Naturalmente, Hickling aceptó y de inmediato empezaron junto con su madre a planear esta bella boda.
Abby llevaba un hermoso vestido de princesa y como es normal en todas las novias, un lindo ramo de flores en su mano. Pero Matt no se quedó atrás, llevaba una elegante camisa de esmoquin bastante cool.
Después de este maravilloso evento, “el novio” escribió acerca de la boda en un post de Facebook:
“¡Espero que este día sea para nuestra paciente y su familia uno en el que puedan mirar hacia atrás y sonreír cuando los días sean duros! ¡Sé que así será!”
Cáncer de mama y turno de noche: enemigos íntimos .
Una investigación refleja que trabajar durante las horas sin luz solar multiplica el riesgo de tumor mamario .
Redacción. Madrid /// 21-7-2015 .
Los problemas a la hora de dormir no solo influyen en nuestro humor. Un reciente estudio publicado en la revista Current Biology ha demostrado que los patrones de sueño irregular asociados a los turnos nocturnos de trabajo multiplican el riesgo de padecer cáncer de mama.
La investigación, que analiza el efecto sobre ratones, apunta a varios factores relacionados con los horarios laborales de noche que explican tal causalidad: la desincronización interna, las alteraciones del estilo de vida, la disminución de los niveles de vitamina D por la falta de luz y, en definitiva, una alteración de nuestro reloj biológico, son algunos de los parámetros que explican tal causalidad.
“Este es el primer estudio que muestra de manera inequívoca una relación entre las inversiones de luz-oscuridad crónicas y el desarrollo del cáncer de mama”, destacan los autores. Uno de ellos, Gijsbetus van der Horst, de la Universidad Erasmus Centro Médico, en los Holanda incide en que “las mujeres con riesgo genético de cáncer de mama no debería trabajar por turnos o como asistente de vuelo”.
Los ratones, que fueron sometidos a a un retraso de su reloj corporal por 12 horas a la semana durante un año, no solo reflejaron un mayor peligro de padecer tal tumor hasta ocho semanas antes que el resto, sino que también mostraron un 20 por ciento más de peso en comparación al resto y siguiendo la misma dieta.
Van der Host y el resto del quipo esperan ahora realizar ensayos más amplios para probar el efecto sobe humanos. No obstante, estiman que, en el caso de las mujeres, las secuelas pueden equivaler a una media de 10 kg más y aa un riesgo de sufrir el tumor mamario unos cinco años antes que el resto.
Redacción. Madrid /// 21-7-2015 .
Los problemas a la hora de dormir no solo influyen en nuestro humor. Un reciente estudio publicado en la revista Current Biology ha demostrado que los patrones de sueño irregular asociados a los turnos nocturnos de trabajo multiplican el riesgo de padecer cáncer de mama.
La investigación, que analiza el efecto sobre ratones, apunta a varios factores relacionados con los horarios laborales de noche que explican tal causalidad: la desincronización interna, las alteraciones del estilo de vida, la disminución de los niveles de vitamina D por la falta de luz y, en definitiva, una alteración de nuestro reloj biológico, son algunos de los parámetros que explican tal causalidad.
“Este es el primer estudio que muestra de manera inequívoca una relación entre las inversiones de luz-oscuridad crónicas y el desarrollo del cáncer de mama”, destacan los autores. Uno de ellos, Gijsbetus van der Horst, de la Universidad Erasmus Centro Médico, en los Holanda incide en que “las mujeres con riesgo genético de cáncer de mama no debería trabajar por turnos o como asistente de vuelo”.
Los ratones, que fueron sometidos a a un retraso de su reloj corporal por 12 horas a la semana durante un año, no solo reflejaron un mayor peligro de padecer tal tumor hasta ocho semanas antes que el resto, sino que también mostraron un 20 por ciento más de peso en comparación al resto y siguiendo la misma dieta.
Van der Host y el resto del quipo esperan ahora realizar ensayos más amplios para probar el efecto sobe humanos. No obstante, estiman que, en el caso de las mujeres, las secuelas pueden equivaler a una media de 10 kg más y aa un riesgo de sufrir el tumor mamario unos cinco años antes que el resto.
Tras décadas de investigación sobre el Alzheimer sin avances, incluidos 123 fármacos que fallaron ... los principales investigadores del campo aseguran que ahora están mucho más confiados en poder desarrollar un tratamiento efectivo.
Por Bill Berkrot y Ransdell Pierson /// NUEVA YORK (Reuters) /// 21-7-2015 .
Con este optimismo, se anticiparon a la Conferencia Internacional de la Asociación de Alzheimer (AAIC, por su nombreen inglés), que comenzó en la ciudad de Washington.
Nuevos fármacos experimentales de Eli Lilly & Co y de Biogen demostraron que podrían llegar a retrasar el avance de la enfermedad, lo que atrajo la atención de inversores y pacientes.
Si bien su desarrollo aún está en una etapa muy preliminar,el campo ahora comprende mucho mejor los cambios cerebrales que produce el Alzheimer y cómo intervenir médicamente.
"Estamos a cinco años de contar con un tratamiento realmente efectivo", celebró Steven Ferris, director del programa deensayos clínicos sobre el Alzheimer del Centro Médico Langone,en Nueva York.
"Sería prematuro decir que ya lo logramos, pero hay muchos fármacos en desarrollo bastante promisorios", agregó Ferris, que participa de ensayos clínicos desde hace 40 años.
Los productos de Lilly y Biogen bloquean la proteína betaamiloide, productora de las placas cerebrales tóxicas que caracterizan a esta enfermedad neurodegenerativa.
Solanezumab, de Lilly, demostró en el 2012 que genera signos de mejoría en pacientes con una forma leve de Alzheimer.
En marzo, aducanumab, de Biogen, se convirtió en el primer medicamento experimental en reducir significativamente el nivel de la proteína en el cerebro y retrasar el deterioro cognitivo en la enfermedad leve. Ambas empresas presentarán sus datos la próxima semana.
...
Con este optimismo, se anticiparon a la Conferencia Internacional de la Asociación de Alzheimer (AAIC, por su nombreen inglés), que comenzó en la ciudad de Washington.
Nuevos fármacos experimentales de Eli Lilly & Co y de Biogen demostraron que podrían llegar a retrasar el avance de la enfermedad, lo que atrajo la atención de inversores y pacientes.
Si bien su desarrollo aún está en una etapa muy preliminar,el campo ahora comprende mucho mejor los cambios cerebrales que produce el Alzheimer y cómo intervenir médicamente.
"Estamos a cinco años de contar con un tratamiento realmente efectivo", celebró Steven Ferris, director del programa deensayos clínicos sobre el Alzheimer del Centro Médico Langone,en Nueva York.
"Sería prematuro decir que ya lo logramos, pero hay muchos fármacos en desarrollo bastante promisorios", agregó Ferris, que participa de ensayos clínicos desde hace 40 años.
Los productos de Lilly y Biogen bloquean la proteína betaamiloide, productora de las placas cerebrales tóxicas que caracterizan a esta enfermedad neurodegenerativa.
Solanezumab, de Lilly, demostró en el 2012 que genera signos de mejoría en pacientes con una forma leve de Alzheimer.
En marzo, aducanumab, de Biogen, se convirtió en el primer medicamento experimental en reducir significativamente el nivel de la proteína en el cerebro y retrasar el deterioro cognitivo en la enfermedad leve. Ambas empresas presentarán sus datos la próxima semana.
...
21 julio 2015
Zeltia . Carlos Doblado ( Bolsagora ) : Hemos Tomado Posiciones en Zeltia ... Largos Abiertos Vía Alerta con Objetivo 5,6/6,5 euros. Stop loss bajo 3,5. .
Carlos Doblado /// 21.07.2015 .
Doble suelo para la biotecnológica española sobre un soporte decreciente desplegado en el proceso de ajuste del movimiento que la llevaba verticalmente de la zona de los 3 a los 4 euros. Entendemos que éste es suficiente para reabrir un proceso de recuperación de fondo que nos parece difícil de cuestionar.
Doble suelo para la biotecnológica española sobre un soporte decreciente desplegado en el proceso de ajuste del movimiento que la llevaba verticalmente de la zona de los 3 a los 4 euros. Entendemos que éste es suficiente para reabrir un proceso de recuperación de fondo que nos parece difícil de cuestionar.
Carolina Pola, Directora de Comunicación de PharmaMar ... Entrevistada por Federación Española de Padres Niños con Cáncer .
Entrevista a Empresas Mágicas: PharmaMar Lunes, 20 de julio de 2015 .
PharmaMar, fundada en 1986 y perteneciente al Grupo Zeltia, es una compañía biofarmacéutica decidida a avanzar en el tratamiento del cáncer mediante el descubrimiento, desarrollo, producción y comercialización de fármacos innovadores de origen marino.
PharmaMar figura entre las principales compañías farmacéuticas españolas que más invierten en Investigación, Desarrollo e innovación. PharmaMar ha invertido cerca de 600 millones de euros en I+D+i desde su fundación hasta hoy.
Hoy, tenemos el placer de entrevistar a Carolina Pola, directora de Comunicación de PharmaMar, una de nuestras “Empresas Mágicas” con una serie de preguntas:
¿De qué forma colabora su empresa con Niños con Cáncer?
Por ahora estamos colaborando mediante donaciones que provienen del reciclaje del material informático (en concreto material HW) que IT tiene programado cada cierto tiempo.
¿Por qué eligieron ayudar a nuestro colectivo?
PharmaMar es una compañía comprometida con la investigación y el desarrollo de medicamentos de origen marino para ayudar a transformar y mejorar los tratamientos contra el cáncer. El cáncer infantil en particular requiere una atención especializada desde el punto de vista médico, así como un apoyo incondicional en su entorno familiar y escolar. Este aspecto es muy importante para ayudar a los niños a entender y superar su situación. Poder colaborar y apoyar a entidades como la vuestra forma parte de nuestro compromiso con los pacientes que conviven con esta enfermedad.
Además de la ayuda a niños y adolescentes con cáncer, ¿cómo desarrolláis la responsabilidad social?
La adopción de una estrategia de Empresa Responsable ha sido uno de los pilares fundamentales de PharmaMar desde su creación. Primero como empresa biotecnológica nuestro compromiso se centró en la investigación y el desarrollo (I+D) de nuevos fármacos antitumorales para avanzar el campo de la biomedicina. Nuestra inversión en I+D e innovación ha ido creciendo hasta haber llegado a un total de 645 millones de euros desde que comenzamos nuestro camino. A día de hoy PharmaMar ha evolucionado y con ello se han añadido proyectos de responsabilidad social. Ahora tenemos unos programas e iniciativas de desarrollo social y económico, siempre con el objetivo de crear procesos innovadores para la formación científica y tecnológica, así como de educación de la sociedad con el objetivo de elevar su competitividad y promover su participación en materia de ciencia. Dado nuestro modelo de investigación enfocado en el desarrollo de medicamentos de origen marino, un proceso que comienza con nuestras expediciones marinas a nivel global, hemos implementado un fuerte compromiso con la sostenibilidad medioambiental y el respeto por la biodiversidad. PharmaMar contribuye al cuidado y protección del medioambiente, cumpliendo con los tratados internacionales como el Convenio de Biodiversidad Biológica de Río de Janeiro y el reciente Protocolo de Nagoya, y además está adherida al Grupo Español de Crecimiento Verde (GECV) y a la Declaración de Barcelona y Asociación Euromediterránea de cooperación multilateral para la estabilidad y desarrollo de la región
La RSC tiene beneficios para nosotros, pero también puede ser muy buena para la empresa. ¿Cómo benefician estas políticas a su organización?
Ser una Empresa Responsable tiene muchos beneficios para PharmaMar puesto que nos ayuda a conseguir nuestros objetivos como grupo. Las iniciativas de RSC puestas en marcha por la compañía contribuyen a alcanzar muchos de los objetivos de la empresa como son la optimización de la inversión que dedicamos a I+D y el desarrollo de proyectos innovadores que podemos finalmente trasladar a los pacientes y a la sociedad en su conjunto. Como empresa española, desarrollamos prácticas de empresa responsable que fomenten el crecimiento personal y profesional de nuestros empleados, el cual es el motor de nuestra compañía, y que contribuyan a construir la reputación y credibilidad de nuestro trabajo.
¿Quiere lanzar algún mensaje a nuestros niños y adolescentes con cáncer?
El futuro de la investigación, y sobre todo de aquella que se hace en España, son precisamente estos niños y adolescentes, que serán quienes ayuden a avanzar en el campo de la biomedicina. Son ellos los que cogerán el relevo en la carrera contra el cáncer y continuarán con el trabajo que han empezado otros, como el de empresas como la nuestra. Es nuestra obligación y de la sociedad en general ayudar a que no solamente salgan adelante y comprendan lo que significa esta enfermedad, sino a que se involucren activamente en combatirla desde diferentes frentes como es el de la investigación, las sociedades médicas y el trabajo tan importante que se hace de las asociaciones de pacientes. Nuestro mensaje es que entiendan que son el futuro, que luchen por él y que sepan que no están solos, ya que desde empresas como PharmaMar se trabaja para que nuevos avances en investigación se conviertan en avances clínicos, y contribuir así a que un día ellos puedan liderar iniciativas contra el cáncer.
“¿Ves eso en mi pulgar?, ¿sabes lo que es? Es cáncer de piel. Esto creció de la nada en cuestión de semanas. Pensé que solo era una infección por hongos o una verruga. Lamentablemente no. He tenido la suerte de que no haya propagación. Ya no habrá cáncer porque será eliminado la próxima semana junto con la mitad de mi pulgar”.
20/07/2015 |
El testimonio de una joven inglesa de 36 años ha conmovido a las redes sociales por ser un ejemplo de esfuerzo y superación frente a la adversidad y además como una señal de advertencia para las personas.
De acuerdo a informaciones reveladas por ABC.es, todo comenzó cuando Melanie Williams descubrió una mancha en su dedo, a la cual no le dio ninguna importancia. El problema es que finalmente se convirtió en un síntoma de un complejo diagnóstico: Era una neuplasia, un tipo de cáncer contra el que ahora lucha.
William escribió al respecto lo siguiente en su cuenta de Facebook: “¿Ves eso en mi pulgar?, ¿sabes lo que es? Es cáncer de piel. Esto creció de la nada en cuestión de semanas. Pensé que solo era una infección por hongos o una verruga. Lamentablemente no. He tenido la suerte de que no haya propagación. Ya no habrá cáncer porque será eliminado la próxima semana junto con la mitad de mi pulgar”.
El texto que ha sido compartido más de 100 mil veces en dicha red social, prosigue señalando que “no quiero tu compasión, quiero más conciencia. Por favor, si ves algún cambio raro en tu piel ve a chequearte”.
Finalmente, el texto de la joven inglesa concluye pidiendo que “no dejes comentarios acerca de lo valiente que soy, en vez de tomar ese tiempo para compartir esto y ayudar a otros o para sacar una cita con sus médicos”.
El testimonio de una joven inglesa de 36 años ha conmovido a las redes sociales por ser un ejemplo de esfuerzo y superación frente a la adversidad y además como una señal de advertencia para las personas.
De acuerdo a informaciones reveladas por ABC.es, todo comenzó cuando Melanie Williams descubrió una mancha en su dedo, a la cual no le dio ninguna importancia. El problema es que finalmente se convirtió en un síntoma de un complejo diagnóstico: Era una neuplasia, un tipo de cáncer contra el que ahora lucha.
William escribió al respecto lo siguiente en su cuenta de Facebook: “¿Ves eso en mi pulgar?, ¿sabes lo que es? Es cáncer de piel. Esto creció de la nada en cuestión de semanas. Pensé que solo era una infección por hongos o una verruga. Lamentablemente no. He tenido la suerte de que no haya propagación. Ya no habrá cáncer porque será eliminado la próxima semana junto con la mitad de mi pulgar”.
El texto que ha sido compartido más de 100 mil veces en dicha red social, prosigue señalando que “no quiero tu compasión, quiero más conciencia. Por favor, si ves algún cambio raro en tu piel ve a chequearte”.
Finalmente, el texto de la joven inglesa concluye pidiendo que “no dejes comentarios acerca de lo valiente que soy, en vez de tomar ese tiempo para compartir esto y ayudar a otros o para sacar una cita con sus médicos”.
Oryzon presenta sus resultados de eficacia preclínica de su tratamiento del Alzheimer en Estados Unidos .
MADRID, 20 (EUROPA PRESS)
Oryzon va a presentar esta semana sus últimos resultados de eficacia preclínica de su fármaco en estadio preclínico avanzado para el tratamiento del Alzheimer, ORY-2001, en la Conferencia Internacional de la Asociación de Alzheimer 2015, que se celebrará en Washington DC (Estados Unidos).
En concreto, la compañía presentará estos datos el próximo miércoles 22 de julio en una comunicación titulada: 'Ory-2001 un inhibidor dual LSD1/MAO B- detiene el desarrollo del Deficit de Memoria en ratones Samp-8.
...
Oryzon va a presentar esta semana sus últimos resultados de eficacia preclínica de su fármaco en estadio preclínico avanzado para el tratamiento del Alzheimer, ORY-2001, en la Conferencia Internacional de la Asociación de Alzheimer 2015, que se celebrará en Washington DC (Estados Unidos).
En concreto, la compañía presentará estos datos el próximo miércoles 22 de julio en una comunicación titulada: 'Ory-2001 un inhibidor dual LSD1/MAO B- detiene el desarrollo del Deficit de Memoria en ratones Samp-8.
...
20 julio 2015
MI130004, A Novel Antibody-Drug Conjugate ( ADC ) With a Marine Payload, Shows Outstanding in Vivo Activity . 20 al 23 Julio en Cambridge ( UK ) .
PharmaMar ( Carmen Cuevas ) realizara el proximo Jueves 23 de Julio una Nueva Presentación del Anticuerpo Conjugado, MI130004, que combina el Anticuerpo Monoclonal Trastuzumab (que se une a la proteína de superficie HER-2) y el Compuesto de Origen Marino PM050489 .
Los resultados estan demostrando que el tratamiento con MI130004 produce un marcado y duradero efecto antitumoral en modelos preclínicos de tumores de mama que sobreexpresan HER2. Los datos destacan el incremento de la supervivencia de los animales tratados y demuestran el potencial de este nuevo producto.
09.55 – 10.50
Pablo Avilés, María José Guillén, Juan Manuel Domínguez, María José Muñoz-Alonso, Luis Francisco García-Fernández, María Garranzo, Andrés Francesch, Simon Munt, Carlos M. Galmarini and Carmen Cuevas .
PharmaMar, Spain.
Grifols paga a 5.300 médicos en EEUU para promocionar sus medicamentos .
Alberto Vigario . 20/07/2015
La Farmacéutica catalana Grifols pagó entre agosto de 2013 y diciembre de 2014 un total de 1,15 millones de euros a 5.339 médicos en EEUU por actividades de promoción y consultoría relacionados con medicamentos de su propiedad.
Estos pagos incluyen conceptos como conferencias, participación en simposios o actividades de formación de la compañía, así como gastos de alojamiento, comida y bebida en estos cursos.
Estos ingresos, de manera detallada, deben enviarse para su conocimiento a las autoridades sanitarias de EEUU, que los hace públicos posteriormente a través de la web del Centers for Medicare & Medicaid Services (CMS), la agencia federal dependiente del Departamento de Salud estadounidense, encargada de gestionar diversos servicios de salud, así como los procesos regulatorios e informativos para los profesionales de la salud, las administraciones locales y los consumidores.
En España, el laboratorio no tiene esta obligación, aunque la patronal Farmaindustria ha cambiado este año su código de buenas prácticas para que también sea obligatorio hacerlo público a partir del año que viene.
...
La Farmacéutica catalana Grifols pagó entre agosto de 2013 y diciembre de 2014 un total de 1,15 millones de euros a 5.339 médicos en EEUU por actividades de promoción y consultoría relacionados con medicamentos de su propiedad.
Estos pagos incluyen conceptos como conferencias, participación en simposios o actividades de formación de la compañía, así como gastos de alojamiento, comida y bebida en estos cursos.
Estos ingresos, de manera detallada, deben enviarse para su conocimiento a las autoridades sanitarias de EEUU, que los hace públicos posteriormente a través de la web del Centers for Medicare & Medicaid Services (CMS), la agencia federal dependiente del Departamento de Salud estadounidense, encargada de gestionar diversos servicios de salud, así como los procesos regulatorios e informativos para los profesionales de la salud, las administraciones locales y los consumidores.
En España, el laboratorio no tiene esta obligación, aunque la patronal Farmaindustria ha cambiado este año su código de buenas prácticas para que también sea obligatorio hacerlo público a partir del año que viene.
...
Grifols logra prorrogar hasta 2026 su contrato con Abbott para la producción de antígenos .
EL GLOBAL / Madrid // lunes, 20 de julio de 2015 .
Grifols, la farmacéutica española con más implantación en Estados Unidos , ha firmado junto a la estadounidense Ortho Clinical Diagnostics la prórroga hasta 2026 de su contrato con la también estadounidense Abbott para la producción de antígenos para reactivos de diagnóstico inmunológico por 700 millones de dólares (unos 646 millones de euros).
Grifols produce para Abbott más de cinco tipos de antígenos que son utilizados en pruebas diagnósticas para la detección de retrovirus como el VIH, los virus de la hepatitis o los que causan enfermedades como la sífilis. La compañía lleva a cabo la producción en una planta del complejo industrial de Emeryville, situado en San Francisco (Estados Unidos).
Esta prolongación del acuerdo refuerza la apuesta de Grifols por este campo, ya que la compañía catalana construye una nueva planta de producción también en Emeryville. Dicho complejo cuenta con una inversión de 59 millones de euros y se espera que a principios de 2017 entre en funcionamiento con el objetivo de modernizar y ampliar la fabricación de antígenos. Esta operación denominada 'Proyecto Horizon', será la encargada de soportar el volumen la producción de antígenos para Abbott que se traspasará íntegramente a este nuevo centro.
El 'Proyecyo Horizon' se enmarca en el plan de inversiones de capital 2014-2016 de Grifols, dotado con cerca de 600 millones de euros.
Grifols, la farmacéutica española con más implantación en Estados Unidos , ha firmado junto a la estadounidense Ortho Clinical Diagnostics la prórroga hasta 2026 de su contrato con la también estadounidense Abbott para la producción de antígenos para reactivos de diagnóstico inmunológico por 700 millones de dólares (unos 646 millones de euros).
Grifols produce para Abbott más de cinco tipos de antígenos que son utilizados en pruebas diagnósticas para la detección de retrovirus como el VIH, los virus de la hepatitis o los que causan enfermedades como la sífilis. La compañía lleva a cabo la producción en una planta del complejo industrial de Emeryville, situado en San Francisco (Estados Unidos).
Esta prolongación del acuerdo refuerza la apuesta de Grifols por este campo, ya que la compañía catalana construye una nueva planta de producción también en Emeryville. Dicho complejo cuenta con una inversión de 59 millones de euros y se espera que a principios de 2017 entre en funcionamiento con el objetivo de modernizar y ampliar la fabricación de antígenos. Esta operación denominada 'Proyecto Horizon', será la encargada de soportar el volumen la producción de antígenos para Abbott que se traspasará íntegramente a este nuevo centro.
El 'Proyecyo Horizon' se enmarca en el plan de inversiones de capital 2014-2016 de Grifols, dotado con cerca de 600 millones de euros.
Desvelan un misterio de décadas que ha desentrañado la causa genética de algunos cánceres .
■ Proteínas clave pueden activar una proteína llamada RAD51, lo que le permite reparar el daño del ADN que causa cáncer en las células.
■ Las mujeres con RAD51 defectuosa y genes BRCA1 y BRCA2 tienen un riesgo mayor de desarrollar cáncer de mama y de ovario.
Han sido un enigma 30 años, pero ahora sabemos que están justo en el corazón de la reparación de daño celular . EP. 20.07.2015 -
Científicos del Francis Crick Institute, financiado por el Cancer Research UK, han resuelto un misterio de décadas que ha permitido desentrañar la causa genética de algunos cánceres de mama y de ovario, según un nuevo estudio publicado en la revista Cell. A raíz de un estudio de cinco años en los gusanos nematodos, los investigadores han descubierto cómo proteínas clave pueden activar una proteína llamada RAD51, lo que le permite reparar el daño del ADN que causa cáncer en las células.
Las mujeres con RAD51 defectuosa y genes BRCA1 y BRCA2 tienen un riesgo mayor de desarrollar cáncer de mama y de ovario. Los científicos ya sabían cómo las proteínas producidas por estos genes trabajan mano a mano para arreglar los daños del ADN, y por qué determinados fallos pueden conducir a la enfermedad.
Los defectos en los "primos" de la proteína de RAD51 (conocidos como paralogs) también aumentan el riesgo de estos cánceres. Pero los científicos no sabían cómo. El equipo ahora ha puesto de manifiesto cómo estos paralogs trabajan para encender el RAD51 cambiando su forma, lo que aumenta drásticamente sus facultades de reparación del ADN.
El doctor Simon Boulton, autor principal y líder del grupo en el Instituto Francis Crick, ha señalado que "estos paralogs han sido un enigma durante unos 30 años, pero ahora sabemos que están justo en el corazón de la reparación de daño celular y ayudando a frenar el desarrollo del cáncer de mama y ovario. De hecho, tienen un papel tan vital como los genes BRCA, más conocidos, en la prevención de la enfermedad".
...
■ Las mujeres con RAD51 defectuosa y genes BRCA1 y BRCA2 tienen un riesgo mayor de desarrollar cáncer de mama y de ovario.
Han sido un enigma 30 años, pero ahora sabemos que están justo en el corazón de la reparación de daño celular . EP. 20.07.2015 -
Científicos del Francis Crick Institute, financiado por el Cancer Research UK, han resuelto un misterio de décadas que ha permitido desentrañar la causa genética de algunos cánceres de mama y de ovario, según un nuevo estudio publicado en la revista Cell. A raíz de un estudio de cinco años en los gusanos nematodos, los investigadores han descubierto cómo proteínas clave pueden activar una proteína llamada RAD51, lo que le permite reparar el daño del ADN que causa cáncer en las células.
Las mujeres con RAD51 defectuosa y genes BRCA1 y BRCA2 tienen un riesgo mayor de desarrollar cáncer de mama y de ovario. Los científicos ya sabían cómo las proteínas producidas por estos genes trabajan mano a mano para arreglar los daños del ADN, y por qué determinados fallos pueden conducir a la enfermedad.
Los defectos en los "primos" de la proteína de RAD51 (conocidos como paralogs) también aumentan el riesgo de estos cánceres. Pero los científicos no sabían cómo. El equipo ahora ha puesto de manifiesto cómo estos paralogs trabajan para encender el RAD51 cambiando su forma, lo que aumenta drásticamente sus facultades de reparación del ADN.
El doctor Simon Boulton, autor principal y líder del grupo en el Instituto Francis Crick, ha señalado que "estos paralogs han sido un enigma durante unos 30 años, pero ahora sabemos que están justo en el corazón de la reparación de daño celular y ayudando a frenar el desarrollo del cáncer de mama y ovario. De hecho, tienen un papel tan vital como los genes BRCA, más conocidos, en la prevención de la enfermedad".
...
California universities battle over Alzheimer's research .
Investigación sobre Alzheimer detona batalla jurídica /// AP 19.07.2015
El esfuerzo de una universidad para incorporar a un importante catedrático de otra universidad del sur de California se convirtió en una batalla jurídica que algunos temen podría detener una investigación sobre la enfermedad de Alzheimer.
La Universidad de California en San Diego presentó una demanda por la deserción de Paul Aisen, un experto en la enfermedad de Alzheimer, y otros empleados para incorporarse a la Universidad del Sur de California, la cual ha trabajado para fortalecer su reputación en Medicina y Ciencias, y ha ofrecido lucrativos paquetes de compensación a los catedráticos de universidad pública.
UC San Diego argumenta que la USC, Aisen y ocho colegas conspiraron para llevar un millón de dólares en fondos federales y privados, así como datos de investigación respecto a más de 1.000 pacientes, a un nuevo centro de estudio de Alzheimer de la USC, reportó el domingo el periódico The Los Angeles Times (http://lat.ms/1SvE5ZR ).
Aisen y la USC niegan haber actuado contra la ley, y señalaron que UC San Diego está tratando de limitar su capacidad para cambiar de empleo y está amenazando la seguridad de la información.
Un juez de Tribunal Superior en San Diego rechazó la semana pasada la solicitud de la USC de impedir que UC San Diego tenga acceso a los datos de la investigación.
Aisen ha dirigido desde 2007 el Estudio Cooperativo sobre la Enfermedad de Alzheimer y está manejando un ensayo clínico para determinar si un medicamento desarrollado por Eli Lilly and Co. puede disminuir o prevenir el Alzheimer en personas que aún no presenta problemas de memoria.
María Carrillo, directora de Ciencias de la Asociación del Alzheimer --organización internacional sin fines de lucro_, dijo que si la batalla jurídica no es resulta rápidamente podría "desacelerar el avance e incluso interrumpir" el ensayo clínico y estudios relacionados. La asociación otorgó recientemente una subvención de ocho millones de dólares a cuatro años para un estudio con sede en Harvard vinculado al trabajo de UC San Diego.
Carrillo subrayó que la asociación quiere una pronta resolución de la demanda para mantener en curso la investigación.
Richard Seligman, vicepresidente asociado de gerencia de investigación en Caltech y quien tiene más de cuatro décadas de experiencia en manejo de subvenciones, dijo que nunca había escuchado de una demanda semejante. Es común que investigadores salten de una escuela a otra y que reciban permiso de sus instituciones académicas y fundadores originales para llevar los subsidios con ellos, señaló.
"Las universidades son extremadamente colegiadas y colaborativas, y rara vez se involucran en disputas" respecto a esos movimientos, con una noción de que la ciencia trasciende las fronteras de las ciudades universitarias, comentó Seligman.
Los Institutos Nacionales de Salud y su subsidiario Instituto Nacional sobre Envejecimiento proporcionan aproximadamente 11 millones de dólares anuales al centro de Alzheimer de la UC.
El esfuerzo de una universidad para incorporar a un importante catedrático de otra universidad del sur de California se convirtió en una batalla jurídica que algunos temen podría detener una investigación sobre la enfermedad de Alzheimer.
La Universidad de California en San Diego presentó una demanda por la deserción de Paul Aisen, un experto en la enfermedad de Alzheimer, y otros empleados para incorporarse a la Universidad del Sur de California, la cual ha trabajado para fortalecer su reputación en Medicina y Ciencias, y ha ofrecido lucrativos paquetes de compensación a los catedráticos de universidad pública.
UC San Diego argumenta que la USC, Aisen y ocho colegas conspiraron para llevar un millón de dólares en fondos federales y privados, así como datos de investigación respecto a más de 1.000 pacientes, a un nuevo centro de estudio de Alzheimer de la USC, reportó el domingo el periódico The Los Angeles Times (http://lat.ms/1SvE5ZR ).
Aisen y la USC niegan haber actuado contra la ley, y señalaron que UC San Diego está tratando de limitar su capacidad para cambiar de empleo y está amenazando la seguridad de la información.
Un juez de Tribunal Superior en San Diego rechazó la semana pasada la solicitud de la USC de impedir que UC San Diego tenga acceso a los datos de la investigación.
Aisen ha dirigido desde 2007 el Estudio Cooperativo sobre la Enfermedad de Alzheimer y está manejando un ensayo clínico para determinar si un medicamento desarrollado por Eli Lilly and Co. puede disminuir o prevenir el Alzheimer en personas que aún no presenta problemas de memoria.
María Carrillo, directora de Ciencias de la Asociación del Alzheimer --organización internacional sin fines de lucro_, dijo que si la batalla jurídica no es resulta rápidamente podría "desacelerar el avance e incluso interrumpir" el ensayo clínico y estudios relacionados. La asociación otorgó recientemente una subvención de ocho millones de dólares a cuatro años para un estudio con sede en Harvard vinculado al trabajo de UC San Diego.
Carrillo subrayó que la asociación quiere una pronta resolución de la demanda para mantener en curso la investigación.
Richard Seligman, vicepresidente asociado de gerencia de investigación en Caltech y quien tiene más de cuatro décadas de experiencia en manejo de subvenciones, dijo que nunca había escuchado de una demanda semejante. Es común que investigadores salten de una escuela a otra y que reciban permiso de sus instituciones académicas y fundadores originales para llevar los subsidios con ellos, señaló.
"Las universidades son extremadamente colegiadas y colaborativas, y rara vez se involucran en disputas" respecto a esos movimientos, con una noción de que la ciencia trasciende las fronteras de las ciudades universitarias, comentó Seligman.
Los Institutos Nacionales de Salud y su subsidiario Instituto Nacional sobre Envejecimiento proporcionan aproximadamente 11 millones de dólares anuales al centro de Alzheimer de la UC.
18 julio 2015
Semana de Ganancias Elevadas dentro del Sector Farmacéutico .
... Zeltia se movió en la misma línea, anotándose en estos últimos días una subida del 7,8 por ciento que le lleva a cotizar en 3,9 euros, muy cerca ya de la referencia de cuatro euros que Zeltia llegó a superar temporalmente unos meses atrás.
Zeltia corrige, al menos momentáneamente, la senda de suave caída que venía dibujando.
...
Zeltia corrige, al menos momentáneamente, la senda de suave caída que venía dibujando.
...
Hepatocarcinoma . CIC bioGUNE investiga un fármaco que permitiría frenar la progresión del cáncer de hígado .
MADRID, 17 Jul. (EUROPA PRESS) -
El Centro de Investigación Cooperativa (CIC) bioGUNE de Vizcaya ha puesto en marcha una investigación para crear un fármaco que permita frenar el desarrollo del cáncer de hígado a través del estudio de los factores no genéticos que intervienen en su progresión.
"Con este estudio se pretende analizar el papel de unas modificaciones no genéticas de proteínas que tienen un papel muy relevante en la progresión del cáncer", ha afirmado la doctora del CIC bioGUNE de Vizcaya y responsable del proyecto, Teresa Cardoso.
El equipo de Cardoso ya ha obtenido algunos resultados que permiten postular la creación de un fármaco dirigido a inhibir esas modificaciones no genéticas, como la nedilización, que permitiría mejorar la calidad de vida de los pacientes con cáncer de hígado. Este fármaco ya ha sido utilizado en modelos preclínicos y se ha observado una reducción de los tumores hepáticos.
El carcinoma hepatocelular o hepatocarcinoma es el principal cáncer de hígado, presente en entre el 85 y el 90 por ciento de los casos, y es la tercera causa de muerte por cáncer en todo el mundo. Su tasa de supervivencia a los 5 años es inferior al 10 por ciento y afecta a más hombres que a mujeres, con un 12 casos de cáncer de hígado por cada 100 hombres. Según Cardoso, su único tratamiento es "el trasplante de hígado, pero debido a la limitada disponibilidad y las largas listas de espera de trasplantes, el paciente fallece antes".
El objetivo del laboratorio es "seguir estudiando los efectos beneficiosos de este fármaco no solo en el cáncer de hígado, sino también en el tratamiento de las fases más iniciales de la enfermedad, como la fibrosis y la cirrosis, que es un problema que en los próximos años será más relevante", ha señalado Cardoso, a lo que ha añadido que "nuestro objetivo es mejorar la supervivencia y la calidad de vida de los pacientes con cáncer de hígado".
UN PROYECTO FINANCIADO A TRAVÉS DE LAS REDES SOCIALES
...
El Centro de Investigación Cooperativa (CIC) bioGUNE de Vizcaya ha puesto en marcha una investigación para crear un fármaco que permita frenar el desarrollo del cáncer de hígado a través del estudio de los factores no genéticos que intervienen en su progresión.
"Con este estudio se pretende analizar el papel de unas modificaciones no genéticas de proteínas que tienen un papel muy relevante en la progresión del cáncer", ha afirmado la doctora del CIC bioGUNE de Vizcaya y responsable del proyecto, Teresa Cardoso.
El equipo de Cardoso ya ha obtenido algunos resultados que permiten postular la creación de un fármaco dirigido a inhibir esas modificaciones no genéticas, como la nedilización, que permitiría mejorar la calidad de vida de los pacientes con cáncer de hígado. Este fármaco ya ha sido utilizado en modelos preclínicos y se ha observado una reducción de los tumores hepáticos.
El carcinoma hepatocelular o hepatocarcinoma es el principal cáncer de hígado, presente en entre el 85 y el 90 por ciento de los casos, y es la tercera causa de muerte por cáncer en todo el mundo. Su tasa de supervivencia a los 5 años es inferior al 10 por ciento y afecta a más hombres que a mujeres, con un 12 casos de cáncer de hígado por cada 100 hombres. Según Cardoso, su único tratamiento es "el trasplante de hígado, pero debido a la limitada disponibilidad y las largas listas de espera de trasplantes, el paciente fallece antes".
El objetivo del laboratorio es "seguir estudiando los efectos beneficiosos de este fármaco no solo en el cáncer de hígado, sino también en el tratamiento de las fases más iniciales de la enfermedad, como la fibrosis y la cirrosis, que es un problema que en los próximos años será más relevante", ha señalado Cardoso, a lo que ha añadido que "nuestro objetivo es mejorar la supervivencia y la calidad de vida de los pacientes con cáncer de hígado".
UN PROYECTO FINANCIADO A TRAVÉS DE LAS REDES SOCIALES
...
Demuestran que atezolizumab reduce el tamaño del tumor en cáncer de vejiga .
WASHINGTON, julio 15:
Un estudio fase II probó que Atezolizumab (Roche) reduce el tamaño del tumor en cáncer de vejiga en pacientes con la enfermedad localmente avanzada o metastásica que habían progresado a un tratamiento inicial.
La inmunoterapia en investigación atezolizumab (MPDL3280A, anti-PDL1) reduce el tamaño del tumor en pacientes con un tipo específico de cáncer de vejiga. Así lo ha mostrado el estudio fase II IMvigor210 al alcanzar su objetivo primario (tasa de respuesta objetiva), logrando reducir el tumor en pacientes con la enfermedad localmente avanzado o metastásico que habían progresado a un tratamiento inicial (segunda línea o posterior).
Esta terapia experimental actúa inhibiendo la proteína PD-L1 (siglas en inglés del ligando 1 muerte celular programada) expresada en células tumorales
...
Un estudio fase II probó que Atezolizumab (Roche) reduce el tamaño del tumor en cáncer de vejiga en pacientes con la enfermedad localmente avanzada o metastásica que habían progresado a un tratamiento inicial.
La inmunoterapia en investigación atezolizumab (MPDL3280A, anti-PDL1) reduce el tamaño del tumor en pacientes con un tipo específico de cáncer de vejiga. Así lo ha mostrado el estudio fase II IMvigor210 al alcanzar su objetivo primario (tasa de respuesta objetiva), logrando reducir el tumor en pacientes con la enfermedad localmente avanzado o metastásico que habían progresado a un tratamiento inicial (segunda línea o posterior).
Esta terapia experimental actúa inhibiendo la proteína PD-L1 (siglas en inglés del ligando 1 muerte celular programada) expresada en células tumorales
...
16 julio 2015
Los Océanos Serán en un Futuro la Farmacia de la Humanidad .
Madrid /// EFE /// 17/7/2015 .
En la actualidad, el 60% de los medicamentos tienen su origen en la naturaleza emergida, entre ellos, antitumorales, analgésicos o antibióticos, de ahí que la salud de las personas dependa del buen estado de conservación de la biodiversidad. La fuente principal de la que han emanado esos medicamentos han sido durante las últimas décadas, los bosques y la naturaleza. Aunque de momento la tecnología no permite la captación de muestras a grandes profundidades, en el futuro serán los océanos los que actúen como despensa y también como "farmacia" de la Humanidad.
Este jueves en la quinta edición del foro "Encuentros Verdes" se han expuesto algunos de estos argumentos que organiza el departamento de EFEverde y la Fundación Biodiversidad. La edición se ha centrado en la relación entre biodiversidad, salud e innovación sanitaria.
... Según Carmen Cuevas, “Pharmamar (empresa pionera en la investigación de fármacos procedentes de fondos marinos) se encuentra en el mejor momento de su historia” y ha destacado el valor de sus últimos fármacos, dirigidos a dianas terapéuticas específicas, las llamadas “balas mágicas”.
José María Fernández Sousa-Faro ha explicado que el 80% de los seres vivos se encuentran en el agua por lo que hay que apostar por la biodiversidad de este ecosistema marino, debido a que los recursos del medio terrestre ya generan muy pocos resultados.
“Tenemos que ser educados y responsables con el medio ambiente, y no hacer barbaridades”, ha defendido el vicepresidente primero de Asebio, quien ha resaltado que debemos tomar en cuenta la naturaleza “como nuestra profesora, porque nos ha enseñado dianas inimaginables”.
La lucha contra el cáncer
También ha subrayado Fernández Sousa-Faro que el cáncer es el área terapéutica donde hay más medicamentos en desarrollo: “Frente al cáncer hay que hacer uso de todas las armas; hace unos 50 años era casi como una condena de muerte, pero ahora se curan en muchos casos”.
...
En la actualidad, el 60% de los medicamentos tienen su origen en la naturaleza emergida, entre ellos, antitumorales, analgésicos o antibióticos, de ahí que la salud de las personas dependa del buen estado de conservación de la biodiversidad. La fuente principal de la que han emanado esos medicamentos han sido durante las últimas décadas, los bosques y la naturaleza. Aunque de momento la tecnología no permite la captación de muestras a grandes profundidades, en el futuro serán los océanos los que actúen como despensa y también como "farmacia" de la Humanidad.
Este jueves en la quinta edición del foro "Encuentros Verdes" se han expuesto algunos de estos argumentos que organiza el departamento de EFEverde y la Fundación Biodiversidad. La edición se ha centrado en la relación entre biodiversidad, salud e innovación sanitaria.
... Según Carmen Cuevas, “Pharmamar (empresa pionera en la investigación de fármacos procedentes de fondos marinos) se encuentra en el mejor momento de su historia” y ha destacado el valor de sus últimos fármacos, dirigidos a dianas terapéuticas específicas, las llamadas “balas mágicas”.
José María Fernández Sousa-Faro ha explicado que el 80% de los seres vivos se encuentran en el agua por lo que hay que apostar por la biodiversidad de este ecosistema marino, debido a que los recursos del medio terrestre ya generan muy pocos resultados.
“Tenemos que ser educados y responsables con el medio ambiente, y no hacer barbaridades”, ha defendido el vicepresidente primero de Asebio, quien ha resaltado que debemos tomar en cuenta la naturaleza “como nuestra profesora, porque nos ha enseñado dianas inimaginables”.
La lucha contra el cáncer
También ha subrayado Fernández Sousa-Faro que el cáncer es el área terapéutica donde hay más medicamentos en desarrollo: “Frente al cáncer hay que hacer uso de todas las armas; hace unos 50 años era casi como una condena de muerte, pero ahora se curan en muchos casos”.
...
Estados Unidos pide a España Transparencia en su política de Innovación Farmacéutica .
... La PhRMA no solo pide al Gobierno español que colabore con la industria para acabar con esta situación, sino que anima a los Estados Unidos a incluir a España en una "lista vigilada" por la administración de Barack Obama.
...
...
.Charles Sawyers, Premio BBVA Fronteras del conocimiento . “Cada tumor es único; la forma de tratarlo, también” .
*.- Sawyers cree que “se acabará venciendo la batalla contra el cáncer" .
*.- "Debemos entender mejor cómo se desarrolla el sistema de defensa de los quistes”.
Manuel G. Pascual /// Madrid /// 15-07-2015 .
“En España escasean los fondos para investigar”
Sawyers compagina su labor en el Memorial Sloan Kettering Cancer Center de Nueva York con el trabajo en la industria farmacéutica. Es miembro del comité de dirección de la suiza Novartis, que adquirió el año pasado el portfolio de oncología de la británica Glaxo SmithKline en esta materia.
Pese a ello, Sawyers no tiene reparos en hablar del buen trabajo que hace la competencia. “Roche está logrando importantes avances en cáncer. Bristol-Myers Squibb y Merck son las dos primeras compañías con medicamentos de inmunoterapia aprobados. Aunque no tengan un portfolio tan extenso, han logrado desarrollar fármacos importantes”.
Aunque también barre para casa. “Novartis invierte más que ninguna otra en I+D: en torno al 20% de los ingresos. Lo que hacen muchas empresas en vez de apostar por investigación básica es comprar compañías con tecnología testada”.
Sawyers alaba también el buen trabajo que están realizando pequeñas compañías biotecnológicas. Aunque opina que su investigación no se traducirá en medicamentos concretos hasta que sean absorbidas por compañías más grandes. “La realidad es que desarrollar y producir un medicamento cuesta tanto dinero que solo está al alcance de unas pocas”.
El científico tiene buena opinión del trabajo que se hace en España. “Estoy en contacto con algunos oncólogos españoles. Conozco el CNIO de Madrid y el departamento de Oncología del Hospital Vall d’Hebron de Barcelona. Y el director médico de mi hospital, José Baselga, también es español. Creo que es impresionante el trabajo que llevan a cabo. Aunque también sé que es muy difícil lograr fondos para investigar. No sé cómo arreglarán eso, pero hasta entonces los científicos seguirán emigrando”.
...
*.- "Debemos entender mejor cómo se desarrolla el sistema de defensa de los quistes”.
Manuel G. Pascual /// Madrid /// 15-07-2015 .
“En España escasean los fondos para investigar”
Sawyers compagina su labor en el Memorial Sloan Kettering Cancer Center de Nueva York con el trabajo en la industria farmacéutica. Es miembro del comité de dirección de la suiza Novartis, que adquirió el año pasado el portfolio de oncología de la británica Glaxo SmithKline en esta materia.
Pese a ello, Sawyers no tiene reparos en hablar del buen trabajo que hace la competencia. “Roche está logrando importantes avances en cáncer. Bristol-Myers Squibb y Merck son las dos primeras compañías con medicamentos de inmunoterapia aprobados. Aunque no tengan un portfolio tan extenso, han logrado desarrollar fármacos importantes”.
Aunque también barre para casa. “Novartis invierte más que ninguna otra en I+D: en torno al 20% de los ingresos. Lo que hacen muchas empresas en vez de apostar por investigación básica es comprar compañías con tecnología testada”.
Sawyers alaba también el buen trabajo que están realizando pequeñas compañías biotecnológicas. Aunque opina que su investigación no se traducirá en medicamentos concretos hasta que sean absorbidas por compañías más grandes. “La realidad es que desarrollar y producir un medicamento cuesta tanto dinero que solo está al alcance de unas pocas”.
El científico tiene buena opinión del trabajo que se hace en España. “Estoy en contacto con algunos oncólogos españoles. Conozco el CNIO de Madrid y el departamento de Oncología del Hospital Vall d’Hebron de Barcelona. Y el director médico de mi hospital, José Baselga, también es español. Creo que es impresionante el trabajo que llevan a cabo. Aunque también sé que es muy difícil lograr fondos para investigar. No sé cómo arreglarán eso, pero hasta entonces los científicos seguirán emigrando”.
...
15 julio 2015
Zeltia , Apoyo en Directriz y Rotura del Triangulo .
Graficos de Txarly /// Martes 14 Julio 2014 .
La entrada en soporte fue buena, ahora esperemos que nos de como mínimo el objetivo del triangulo ( sus máximos ) ...
La entrada en soporte fue buena, ahora esperemos que nos de como mínimo el objetivo del triangulo ( sus máximos ) ...
14 julio 2015
El 9 por ciento del PIB Español depende ya de la Biotecnología, destaca el Informe ASEBIO 2014 .
@ElGlobalNet /// martes, 14 de julio de 2015 .
La Asociación Española de Bioempresas (Asebio) presenta este martes el Informe Anual Asebio 2014 que recoge los últimos datos del sector biotecnológico español, acto que va a contar con la presencia de la Secretaria de Estado de Investigación, Desarrollo e Innovación, Carmen Vela Olmo.
El informe destaca el creciente peso de la facturación de las empresas de la llamada bioeconomía (las dedicadas a la biotecnología y las que se declaran usuarias) en el PIB español, que en 2013 –último dato analizado- alcanzó el 9,07 por ciento. La evolución en los años de la crisis, desde 2008, ha sido espectacular, ya que por entonces la bioeconomía apenas suponía el 2,98 por ciento del PIB.
La coyuntura económica en España ha provocado que 2013 arroje datos negativos para el sector, situación que Asebio alertó en los últimos años instando a las administraciones a que desarrollaran políticas de choque para evitar la destrucción del tejido innovador.
El empleo ha disminuido el 14,8 por ciento hasta los 172.939 trabajadores en 2013. Frente a esta cifra, destaca el aumento de la cifra de negocios del sector, que alcanzó los 95.152 millones de euros en 2013, el 18,48 por ciento más respecto al año anterior, según datos del módulo de biotecnología de la Encuesta sobre Innovación Tecnológica en las empresas 2013 del Instituto Nacional de Estadística recogidos en el informe.
En relación a la cifra de negocios, un 65,68 por ciento del total se atribuye a las empresas que consideran que la biotecnología es una línea de negocio secundaria, mientras que un 26,85 por ciento es generado por empresas donde la biotecnología supone una herramienta necesaria para la producción y el 7,47 por ciento restante tiene que ver con las empresas estrictamente biotecnológicas.
El número de empresas que realizan actividades relacionadas con la biotecnología descendió el 7,77 por ciento hasta las 2.831 en 2013. De ellas, 554 empresas han desarrollado la biotecnología como actividad principal y/o exclusiva –las llamadas biotechs-, que contabilizan una caída del 11,42 por ciento respecto al año anterior. En estas empresas, el empleo cae el 14,95 por ciento y la facturación el 19,2 por ciento hasta los 7.111 millones de euros.
La Asociación Española de Bioempresas (Asebio) presenta este martes el Informe Anual Asebio 2014 que recoge los últimos datos del sector biotecnológico español, acto que va a contar con la presencia de la Secretaria de Estado de Investigación, Desarrollo e Innovación, Carmen Vela Olmo.
El informe destaca el creciente peso de la facturación de las empresas de la llamada bioeconomía (las dedicadas a la biotecnología y las que se declaran usuarias) en el PIB español, que en 2013 –último dato analizado- alcanzó el 9,07 por ciento. La evolución en los años de la crisis, desde 2008, ha sido espectacular, ya que por entonces la bioeconomía apenas suponía el 2,98 por ciento del PIB.
La coyuntura económica en España ha provocado que 2013 arroje datos negativos para el sector, situación que Asebio alertó en los últimos años instando a las administraciones a que desarrollaran políticas de choque para evitar la destrucción del tejido innovador.
El empleo ha disminuido el 14,8 por ciento hasta los 172.939 trabajadores en 2013. Frente a esta cifra, destaca el aumento de la cifra de negocios del sector, que alcanzó los 95.152 millones de euros en 2013, el 18,48 por ciento más respecto al año anterior, según datos del módulo de biotecnología de la Encuesta sobre Innovación Tecnológica en las empresas 2013 del Instituto Nacional de Estadística recogidos en el informe.
En relación a la cifra de negocios, un 65,68 por ciento del total se atribuye a las empresas que consideran que la biotecnología es una línea de negocio secundaria, mientras que un 26,85 por ciento es generado por empresas donde la biotecnología supone una herramienta necesaria para la producción y el 7,47 por ciento restante tiene que ver con las empresas estrictamente biotecnológicas.
El número de empresas que realizan actividades relacionadas con la biotecnología descendió el 7,77 por ciento hasta las 2.831 en 2013. De ellas, 554 empresas han desarrollado la biotecnología como actividad principal y/o exclusiva –las llamadas biotechs-, que contabilizan una caída del 11,42 por ciento respecto al año anterior. En estas empresas, el empleo cae el 14,95 por ciento y la facturación el 19,2 por ciento hasta los 7.111 millones de euros.
Biopsia Liquida . Identifican Mutaciones de Tumores de Colon y Recto con un Análisis de Sangre .
BARCELONA, 14 Jul. (EUROPA PRESS) -
Un estudio internacional liderado por el jefe del Servicio de Oncología Médica del Hospital Vall d'Hebron de Barcelona, Josep Tabernero, ha demostrado que la biopsia líquida --mediante un análisis de sangre-- permite identificar mutaciones relevantes de los tumores de colon y recto que no son detectadas con la biopsia de tejidos.
Un estudio, aleatoritzado y de fase III, ha analizado mediante biopsia líquida el ADN de 503 pacientes con cáncer colorrectal metastásico para detectar mutaciones de los genes KRAS, PIK3CA y BRAF en los tumores, ha informado el Vall d'Hebron en un comunicado.
A los pacientes seleccionados, que ya habían recibido diversas líneas de tratamiento, se les administró el fármaco 'regorafenib' --un inhibidor de proteínas implicadas en el tumor-- o bien placebo.
Mediante biopsia líquida se logró detectar de forma fácil diferentes mutaciones asociadas al tumor: en concreto, en un subgrupo de 41 pacientes que habían recibido terapia anti-EGFR se identificó que tenían mutaciones KRAS adquiridas durante el curso de su enfermedad.
...
Un estudio internacional liderado por el jefe del Servicio de Oncología Médica del Hospital Vall d'Hebron de Barcelona, Josep Tabernero, ha demostrado que la biopsia líquida --mediante un análisis de sangre-- permite identificar mutaciones relevantes de los tumores de colon y recto que no son detectadas con la biopsia de tejidos.
Un estudio, aleatoritzado y de fase III, ha analizado mediante biopsia líquida el ADN de 503 pacientes con cáncer colorrectal metastásico para detectar mutaciones de los genes KRAS, PIK3CA y BRAF en los tumores, ha informado el Vall d'Hebron en un comunicado.
A los pacientes seleccionados, que ya habían recibido diversas líneas de tratamiento, se les administró el fármaco 'regorafenib' --un inhibidor de proteínas implicadas en el tumor-- o bien placebo.
Mediante biopsia líquida se logró detectar de forma fácil diferentes mutaciones asociadas al tumor: en concreto, en un subgrupo de 41 pacientes que habían recibido terapia anti-EGFR se identificó que tenían mutaciones KRAS adquiridas durante el curso de su enfermedad.
...
13 julio 2015
PM060184 .
Han finalizado los dos estudios en fase I que iniciaron el programa de desarrollo de este compuesto.
Además de la determinación de la dosis y el esquema para los estudios de Fase II, los resultados de actividad observados en estos estudios de Fase I han orientado las indicaciones para los estudios de fase II, concretamente, durante el año 2015 se iniciarán estudios específicos en las indicaciones de Cáncer de Mama y Cáncer Colorectal.
Continúa además el reclutamiento del estudio fase I en combinación con Gemcitabina en dos centros en España y Estados Unidos.
***************************************************+
PM060184 is a marine-derived synthetically-produced compound with strong in vitro and in vivo antitumour activity and a favorable safety profile. In Phase I studies.
Situation Overview
PM060184 belongs to a new family of tubulin-binding agents originally isolated from the marine sponge Lithoplocamia lithistoides. This compound is currently produced by total synthesis and is under evaluation in clinical studies in patients with advanced cancer diseases.
Mechanism of Action
PM060184 has a potent antitumor activity in a panel of different tumor xenograft models. PM060184 induces disorganization and disruption of the microtubule network as well as aberrant mitotic spindle multipolarization and chromosome missegregation. These effects give rise to prometaphase arrest and formation of multinucleated cells. Then, cells enter to caspase-driven apoptosis or are arrested in a pseudo-senescent state.
Además de la determinación de la dosis y el esquema para los estudios de Fase II, los resultados de actividad observados en estos estudios de Fase I han orientado las indicaciones para los estudios de fase II, concretamente, durante el año 2015 se iniciarán estudios específicos en las indicaciones de Cáncer de Mama y Cáncer Colorectal.
Continúa además el reclutamiento del estudio fase I en combinación con Gemcitabina en dos centros en España y Estados Unidos.
***************************************************+
PM060184 is a marine-derived synthetically-produced compound with strong in vitro and in vivo antitumour activity and a favorable safety profile. In Phase I studies.
Situation Overview
PM060184 belongs to a new family of tubulin-binding agents originally isolated from the marine sponge Lithoplocamia lithistoides. This compound is currently produced by total synthesis and is under evaluation in clinical studies in patients with advanced cancer diseases.
Mechanism of Action
PM060184 has a potent antitumor activity in a panel of different tumor xenograft models. PM060184 induces disorganization and disruption of the microtubule network as well as aberrant mitotic spindle multipolarization and chromosome missegregation. These effects give rise to prometaphase arrest and formation of multinucleated cells. Then, cells enter to caspase-driven apoptosis or are arrested in a pseudo-senescent state.
Suscribirse a:
Entradas (Atom)