El Internista Pablo Guisado Publica un Caso de Éxito y Lamenta Que la Población Inmunodeprimida Sea la Gran Olvidada Ante el Levantamiento de Restricciones.
La Plitidepsina Como Tratamiento de Rescate Exitoso Para la Replicación Viral Prolongada del SARS-CoV-2 en un Paciente con Agotamiento Previo de Células B Mediadas por Anticuerpos Monoclonales Anti-CD20 y Leucemia Linfocítica Crónica .
ABSTRACT
Existe una necesidad urgente de terapias antivirales altamente eficaces en huéspedes inmunodeprimidos que desarrollan la enfermedad por coronavirus (COVID-19), con especial preocupación por aquellos afectados por neoplasias hematológicas malignas.
Presentación del caso
Aquí, presentamos el caso de un varón de 75 años con leucemia linfocítica crónica que fue deficiente en poblaciones de linfocitos B CD19CD20 debido al tratamiento previo con anticuerpos monoclonales anti-CD20. El paciente presentó neumonía grave por COVID-19 debido a una infección prolongada por coronavirus 2 (SARS-CoV-2) del síndrome respiratorio agudo grave y fue tratado con dos ciclos del antiviral plitidepsina sobre una base de uso compasivo. Posteriormente, el paciente alcanzó una carga viral indetectable y su neumonía se resolvió.++
Conclusiones
El tratamiento con plitidepsina fue bien tolerado sin ninguna otra toxicidad hematológica o cardiovascular. Este caso apoya además la plitidepsina como un posible fármaco antiviral en pacientes con SARS-CoV-2 afectados por inmunodeficiencias y neoplasias hematológicas malignas .
Los pacientes afectados por neoplasias hematológicas malignas constituyen una población única con respecto a la infección por coronavirus 2 del síndrome respiratorio agudo grave (SARS-CoV-2). Esta población ha demostrado un mayor riesgo de infección persistente con SARS-CoV-2, y resultados graves y mortalidad debido a la enfermedad por coronavirus 2019 (COVID-19) [1, 2].
Además de la neoplasia maligna en sí, los tratamientos contra el cáncer pueden producir efectos a corto y largo plazo en las poblaciones linfocíticas. El impacto del tratamiento en el sistema inmunitario es de particular importancia en el caso de los anticuerpos monoclonales anti-CD20 (rituximab, obinutuzumab), que, a pesar de la variabilidad entre los pacientes, generalmente conducen a la reducción (o agotamiento) de las subpoblaciones de linfocitos B que persisten durante meses.
Aquí, informamos el curso clínico y virológico de una infección viral prolongada por SARS-CoV-2 en un paciente adulto previamente tratado por LLC con obinutuzumab, que estaba en remisión completa de su neoplasia hematológica maligna. El tratamiento con plitidepsina se concedió para uso compasivo según lo autorizado por la Agencia Española de Medicamentos (AEMPS) (AUT334100148189/21) [3]. El paciente firmó el consentimiento informado para el tratamiento y antes de la preparación del manuscrito.
Un hombre de 75 años con antecedentes de LLC llegó al departamento de emergencias (DE) con 1 semana de tos seca y cansancio en enero de 2021. La infección por SARS-CoV-2 se confirmó mediante muestras de hisopo nasofaríngeo (NP) y una reacción en cadena de la polimerasa con transcripción inversa en tiempo real (RT-PCR; consulte el archivo adicional 1: Material complementario). Se registraron morbilidades cardiovasculares adicionales, incluida la fibrilación auricular permanente y la cardiopatía isquémica estable.
Después de 22 días de enfermedad continuada, el paciente ingresó en nuestro hospital por fiebre persistente, fatiga, aparición de insuficiencia respiratoria y opacidades bilaterales en curso por radiografía de tórax. El paciente tenía niveles indetectables de anticuerpos contra el SARS-CoV-2, y la citometría de flujo sanguíneo periférico mostró niveles indetectables de células B CD19 y CD20.++
El paciente experimentó una progresión adicional de la gravedad clínica y de la imagen 48 días después del inicio de la enfermedad, lo que provocó el uso compasivo de plitidepsina 2,5 mg c.d. durante tres días de acuerdo con los protocolos disponibles. El umbral del ciclo RT-PCR (Ct) valor era 23 en el momento en que se inició la plitidepsina (Archivo adicional 1: Fig. 1S-2S, tabla 1S-4S).
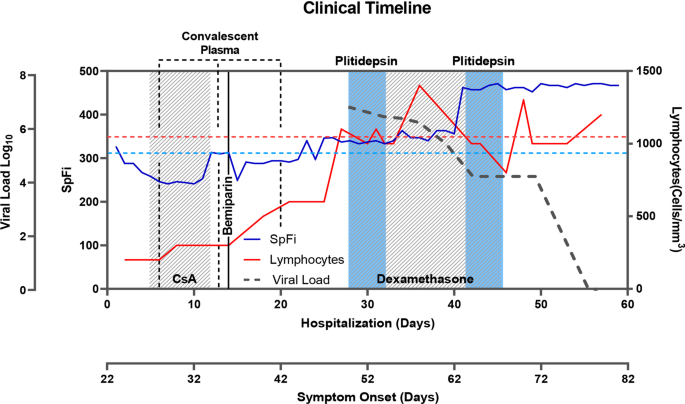
Cronología de los principales parámetros de laboratorio y microbiológicos durante y después del tratamiento con plitidepsina. Se han tomado como referencia dos puntos temporales: el número de días desde el inicio de los síntomas del SARS-CoV-2 y el número de días desde el ingreso hospitalario. La plitidepsina se administró en los días 49-51 y 65-67 después del inicio de los síntomas. Los parámetros mostrados en el curso clínico son los siguientes: Una carga viral cuantitativa (log10 copias/ml) utilizando muestras de hisopos nasofaríngeos (línea de puntos grises). Línea azul B SpFI (AU). Recuento total de linfocitos C (células/mm3) (línea roja). Unidades arbitrarias au, CsA ciclosporina A, relación SpFi de saturación de oxígeno en sangre (SpO2)/fracción de oxígeno inspirado (FiO2) igual o inferior a 300 UA
La mejoría clínica fue evidente en una semana, lo que llevó a la retirada de la oxigenoterapia 7 días después de la primera dosis de plitidepsina. Sin embargo, la RT-PCR continuó mostrando valores positivos para sars-CoV-2, con una Ct valor de 34 (Fig. 1).
El día 61, se administró una dosis única de 20 g de inmunoglobulina humana por vía intravenosa; 24 horas más tarde (y dos semanas después del primer ciclo de plitidepsina), se inició un segundo ciclo equivalente de plitidepsina. El día 74, el paciente recibió su primera prueba RT-PCR negativa y posteriormente fue negativo para SARS-CoV-2 en tres muestras consecutivas. El paciente fue dado de alta del hospital el día 82 y no experimentó ningún signo de recaída del SARS-CoV-2 durante el seguimiento ambulatorio.
La replicación viral prolongada del SARS-CoV-2 se reconoce cada vez más como un problema clínico emergente entre las personas inmunocomprometidas. La neumonía subaguda o crónica por COVID-19 puede causar daño pulmonar persistente y puede provocar fenómenos de escape viral [4,5,6,7]. Un defecto subyacente en la respuesta inmune es la razón principal de la replicación viral en curso y el aclaramiento viral defectuoso en pacientes con neoplasias hematológicas malignas debido a la ausencia de precursores de células B. Además, las deficiencias del sistema inmunitario secundarias al tratamiento con anticuerpos monoclonales anti-CD20 pueden perjudicar el desarrollo de anticuerpos neutralizantes después de dos dosis de vacunas de ARNm contra el SARS-CoV-2 [8].
La plitidepsina es un inhibidor conocido de la replicación del SARS-CoV-2, cuyo mecanismo de acción antiviral se ha descrito recientemente utilizando un modelo mutante resistente a los medicamentos [9]. En resumen, la actividad antiviral de la plitidepsina está mediada por la inhibición del factor de elongación de la proteína eucariota huésped 1α (eEF1A). A través de la inhibición de eEF1A, la plitidepsina previene la expresión de la proteína nucleocápside (N) del SARS-CoV-2, particularmente temprano durante la infección, probablemente inhibiendo la traducción del ARN viral (10).
El informe actual tiene limitaciones obvias. Aunque solo describe a un paciente, el resultado exitoso observado aquí debe evaluarse en el contexto del mal pronóstico para los pacientes inmunocomprometidos con neoplasias malignas hematológicas. Otra limitación de este estudio es que no pudimos amplificar y secuenciar el ARN viral a partir de muestras de hisopo recogidas, por lo que la variante precisa del SARS-CoV-2 que infectó a este paciente sigue siendo desconocida. Tampoco fue posible capturar los cambios en el perfil de citoquinas del paciente durante el ingreso hospitalario y durante las infusiones de plitidepsina.
Hasta donde sabemos, esta es la primera evidencia del uso exitoso de un potencial antiviral contra el SARS-CoV-2 en un paciente con neoplasia hematológica maligna y células B agotadas debido a la terapia previa con LLC y con replicación viral prolongada. El paciente fue seguido durante seis meses desde que fue dado de alta del hospital sin signos de recaída o reinfección por SARS-CoV-2.