Zeltia ya no es solo Yondelis ... la propia PharmaMar dispone ya de otros Farmacos en ensayo clinico avanzado con Más Potencial y Espectativas .
Esta misma semana hemos visto como un Segundo Farmaco ( Aplidin ) alcanzaba un Acuerdo por 35 Millones de euros con la Suiza Roche a traves de su Filial Chugai .
Tambien hay que poner el Foco de Atención en la BioFarmaceutica Sylentis , la cual con muy poco ruido ha colocado ya un Farmaco en Fase IIb para el tratamiento del Glaucoma y la Hipertensión Ocular tras los buenos resultados obtenidos en la Fase IIa ... se trata del Bamosiran ( SYL040012 ) del que se tiene más seguimiento fuera que dentro de España tal y como se puede observar en el informe publicado recientemente ( https://www.asdreports.com/news.asp?pr_id=2385# ) , un informe que situa al Bamosiran ( SYL040012 ) entre los 11 Farmacos capaces de Generar unas Ventas muy relevantes en caso de conseguir salir al Mercado .
*****************************************************************************
CNMV . Madrid, 17 de julio del 2014 :
 El Grupo Zeltia (MC:ZEL) ha anunciado hoy que Sylentis, pionera en la investigación y desarrollo de nuevos fármacos basados en la tecnología del silenciamiento génico de ARN de interferencia (RNAi), ha recibido autorización de las autoridades de Estonia para comenzar el ensayo de fase IIb con bamosiran (SYL040012), para el tratamiento del glaucoma y la hipertensión ocular.
El Grupo Zeltia (MC:ZEL) ha anunciado hoy que Sylentis, pionera en la investigación y desarrollo de nuevos fármacos basados en la tecnología del silenciamiento génico de ARN de interferencia (RNAi), ha recibido autorización de las autoridades de Estonia para comenzar el ensayo de fase IIb con bamosiran (SYL040012), para el tratamiento del glaucoma y la hipertensión ocular. Esta es la primera autorización de la lista de países donde se llevará a cabo este ensayo y permite el inicio del reclutamiento de pacientes.
El ensayo denominado SYLTAG es un estudio clínico de búsqueda de dosis, con 5 grupos (4 dosis de bamosiran y timolol), paralelo aleatorizado, enmascarado para el evaluador, con control activo (Timolol).
Se realizará en un total de 21 centros repartidos entre España, Estonia, Alemania y Estados Unidos y reclutará a 180 pacientes.
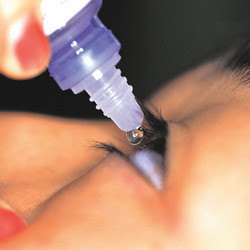
El objetivo principal de este estudio de fase IIb es establecer la dosis más eficaz sobre la presión intraocular de bamosiran administrado una vez al día en forma de gotas oculares tras 28 días de tratamiento.
Los objetivos secundarios incluyen:
*.- Objetivos secundarios de eficacia: Evaluación del efecto del tratamiento en comparación con el comparador (timolol) y cambios en la calidad de vida de los pacientes tratados con ambos fármacos.
*.- Objetivos secundarios de seguridad: evaluación de la tolerabilidad local (molestia ocular), agudeza visual, biomicroscopia, paquimetría, oftalmoscopía, tolerabilidad sistémica y aparición de efectos adversos.
Este estudio forma parte del desarrollo de bamosiran como fármaco de aplicación tópica para el tratamiento de la hipertensión ocular y glaucoma. Permitirá seleccionar la dosis óptima para así poder continuar con los ensayos en fase III.
*****************************************************************************
Sobre Sylentis / SYL040012 :
 Sylentis S.A. es una compañía Bio-Farmacéutica englobada dentro del Grupo Zeltia y participada por éste al 100%, centrada en la investigación y desarrollo de nuevos fármacos basados en la tecnología de silenciamiento génico del ARN de interferencia (RNAi).
Sylentis S.A. es una compañía Bio-Farmacéutica englobada dentro del Grupo Zeltia y participada por éste al 100%, centrada en la investigación y desarrollo de nuevos fármacos basados en la tecnología de silenciamiento génico del ARN de interferencia (RNAi). Sylentis se sitúa entre las firmas pioneras en investigación con el ARN (ácido ribonucleico) de interferencia, y es una de las siete empresas en el mundo que realizan ensayos clínicos en el desarrollo de medicamentos. Actualmente no existe ningún fármaco en el mercado que emplee la herramienta desarrollada por la compañía española.
Sylentis se sitúa entre las firmas pioneras en investigación con el ARN (ácido ribonucleico) de interferencia, y es una de las siete empresas en el mundo que realizan ensayos clínicos en el desarrollo de medicamentos. Actualmente no existe ningún fármaco en el mercado que emplee la herramienta desarrollada por la compañía española.El ARN es el mecanismo que emplean las células para sintetizar las proteínas que necesita el organismo. Sin embargo, en algunas ocasiones su funcionamiento erróneo es el origen de enfermedades. Las investigaciones de Sylentis tienen como diana este intermediario entre el ADN y las proteínas, para lo que utilizan moléculas diseñadas con herramientas bioinformáticas, que silencian la expresión del ARN de interferencia.
 Sylentis emplea un mecanismo diferente al de la mayoría de los fármacos que atacan las proteínas. La técnica de la firma española sólo ataca al intermediario, lo que permite eliminar muchos efectos secundarios de los medicamentos.
Sylentis emplea un mecanismo diferente al de la mayoría de los fármacos que atacan las proteínas. La técnica de la firma española sólo ataca al intermediario, lo que permite eliminar muchos efectos secundarios de los medicamentos.Sylentis tiene previsto llevar a cabo la Fase IIb del SYL040012 para el tratamiento del glaucoma en 21 Hospitales de la UE y EEUU .
